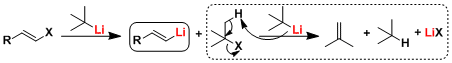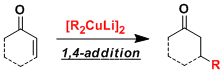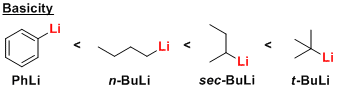- 概要
有机金属试剂的反应性大体由碳-金属键的极性差啦决定,碳-锂结合键具有最大的极化差(离子结合度)。正因为此性质,相比于 Grignard试剂、有机锌试剂, 有机锂化合物的反应活性更高。通常,有机锂试剂在空气 ・水中十分不稳定,反应时会放出大量热。所以在使用时,惰性气体 ・脱水溶剂 ・低温条件通常是缺一不可。有机锂试剂通常用作金属交换,亲核试剂,以及强碱。
- 基本文献
・Chalk, A. J.; Hoogeboom, T. J. J. Organomet. Chem. 1968, 11, 615. doi:10.1016/0022-328X(68)80091-9
・Review: Mallan, J. M.; Bebb, R. L. Chem. Rev. 1969, 69, 693. DOI: 10.1021/cr60261a006
・Review: Wu, G.; Huang, M. Chem. Rev. 2006, 106, 2596. DOI: 10.1021/cr040694k
・Review: Seyferth, D. Organometallics, 2006, 25, 2. DOI: 10.1021/om058054a
- 反应机理
锂-卤素交换反应是依照单电子移动(SET)机理或者是卤素位的亲核加成-消除机理进行的。(参考:J. Organomet. Chem. 1988, 352, 1.) 使用t-BuLi进行锂-卤素交换反应的时候,相对于卤代底物,二当量的锂试剂是必须的。(为了使得金属锂交换后生成的 t– 丁基卤化物与另一当量的 t-BuLi 反应消耗)
- 反应实例
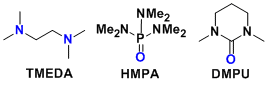
※通常锂试剂在溶液中都是以聚合态存在。如果加入配位性添加剂的话,可以使得其从聚合形态转化成单体形态,从而提高其反应性。使用频率较高的有:N,N,N’,N’-四甲基乙二胺(TMEDA)、六甲基磷酰三胺(HMPA)和N,N-二甲基丙烯基脲(DMPU)。
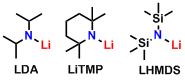
※有机锂试剂具有亲核性和强碱性两种形式,反应性高的同时,也比较容易产生副反应。作为碱使用的时候,通常会先与立体位阻大的二级胺反应以氨基锂的形式使用。该类氨基锂代表试剂有LDA(Lithium diisopropylamide)、LiTMP(Lithium 2,2,6,6-tetramethylpiperidide)、LHMDS(Lithium hexamethyldisilazide)。
※另外,作为亲核试剂使用的时候,可以转化成銅锂配合物(R2CuLi)、该试剂的碱性被有效抑制,而其亲核性不变,可以一哦那个与亲核加成或取代反应。锂试剂比较hard,与α,β不饱和羰基化合物进行反应的时候、1,2-加成往往优与1,4-加成。而形成銅锂配合物后,该试剂可以用于1,4-选择性加成反应。
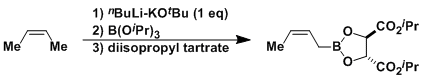
・nBuLi-KOtBu的组合通常被称为Schlosser-Lochmann碱、作为超强碱被使用。该碱可以拔去烯丙基位的氢原子 [1]。 该试剂常用于手性烯丙硼酸化合物的合成。 下图给出了Roush等人开发的应用反应[2]。
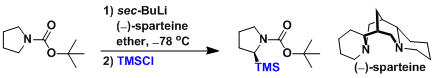
・(-)-Sparteine作为配位性添加剂使用,使得发生立体选择性的脱H化反应,得到手性产物。以下给出了一个应用实例。[3]
- 实验步骤
- 实验技巧
※经常使用的市售代表性锂试剂有MeLi、PhLi、n-BuLi、sec-BuLi、t-BuLi等。
※市售的锂试剂通常保存在 Sure-sealed 试剂瓶中,但是在用针筒抽取 2~3 回后,通过刺出的孔洞,试剂逐渐会与空气接触, 渐渐地其反应性就会下降。所以我们通常用过后就会用特氟龙胶带再密封一次。如果想更长时间保存的话最好把它移到 Schlenk管 中比较好。
※在适当的环境下用浓度滴定法 滴定(titration) 检查后使用比较好。简便且信赖度高的方法有,二苯基醋酸法和 2,2′-联吡啶法。
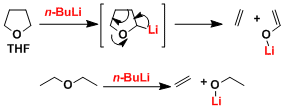
※有机锂试剂一般在正己烷这种碳氢系溶剂中比较稳定,在醚类溶剂中会渐渐发生 β 消除反应逐渐被分解。( 例如n-BuLi在THF中0℃的半衰期就是24小时)。分解容易度顺序:DME>THF>乙醚。
※t-BuLi的反应活性很高,经常会引起火灾。在使用时候得特别注意,尤其是用于大量反应的时候,手边必须准备好灭火器。
- 参考文献
[2] Roush, W. R.; Ando, K.; Powers, D. B.; Halterman, R. L.; Palkowitz, A. D. Tetrahedron Lett.
1988, 29, 5579. doi:10.1016/S0040-4039(00)80816-3
[3] Kerrik, S. T.; Beak, P. J. Am. Chem. Soc. 1991, 113, 9708. DOI: 10.1021/ja00025a066
[4] Kofron, W. G.; Baclawski, L. M. J. Org. Chem. 1976, 41, 1879. DOI: 10.1021/jo00872a047
[5] Watson, S. C.; Eastham, J. F. J. Organomet. Chem. 1967, 9, 165. doi:10.1016/S0022-328X(00)92418-5
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载