本文作者:杉杉
导读
近日,常州大学史一安教授课题组在Organic Letters上发表论文,报道了在钯催化下,由2-碘苯乙烯和二叔丁基二氮丙啶酮(diaziridinone)合成吲哚的策略,成功构建了两个新的C-N键。同时,该反应涉及将Pd氧化插入至芳基碘中,再将乙烯基C-H键活化为钯(II)环中间体,随后通过二叔丁基二氮丙啶酮将其进行双胺基化(bisaminated)的过程,从而得到吲哚产物。
Palladium-Catalyzed Sequential C−H Activation/Amination with Diaziridinone: An Approach to Indoles
Jing Li, Jinhua Chen, Luying Wang, and Yian Shi*
Org. Lett.ASAPDOI:10.1021/acs.orglett.1c01043
正文
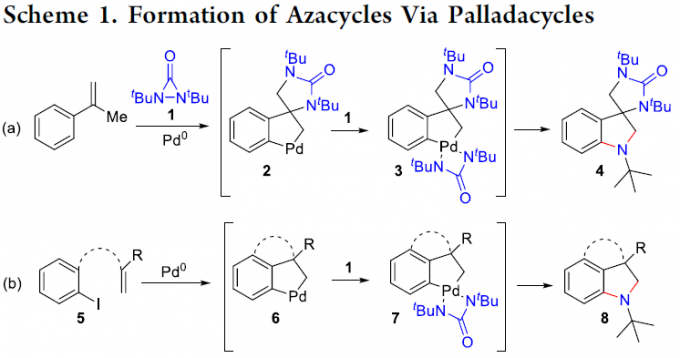
吲哚化合物广泛存在于生物活性分子、药物、材料等中。目前,已有大量文献报道了吲哚化合物的合成,其中金属催化C-H胺化反应作为合成吲哚的高效策略之一,可快速构建C-N新键。前期,该课题组[1]报道了在钯催化下,二叔丁基二氮丙啶酮(1)和α-甲基苯乙烯合成螺二氢吲哚4的策略,涉及烯丙基和芳基的C-H活化以形成钯(II)环中间体2,中间体2被二叔丁基二氮丙啶酮(1)拦截,通过钯(IV)环中间体3以生成螺二氢吲哚4(Scheme 1, eq a)。同时,由Heck/芳基C-H活化产生的钯环中间体 6也可被二叔丁基二氮丙啶酮(1)捕获,得到二氢吲哚8(Scheme 1, eq b)。值得注意的是,钯环的双胺基化反应可同时构建两个新的C-N键,可作为合成含氮杂环化合物的有效方法。
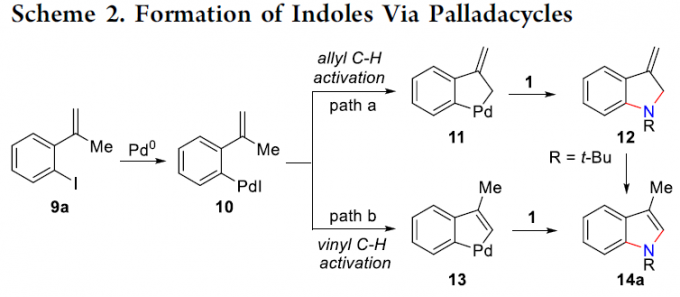
为了验证方案的可行性,作者以2-碘苯乙烯9a为底物,进行相关吲哚的合成(Scheme 2)。首先,9a与钯催化剂氧化加成生成中间体10。中间体10若通过烯丙基C-H键的活化,则可形成钯环中间体11,再与二叔丁基二氮丙啶酮(1)反应,生成二氢吲哚12,最后通过芳构化获得吲哚14(path a)。其次,中间体10若通过乙烯基C-H键的活化,则可形成钯环中间体13,再与二叔丁基二氮丙啶酮(1)反应,则可直接获得吲哚14(path b)。
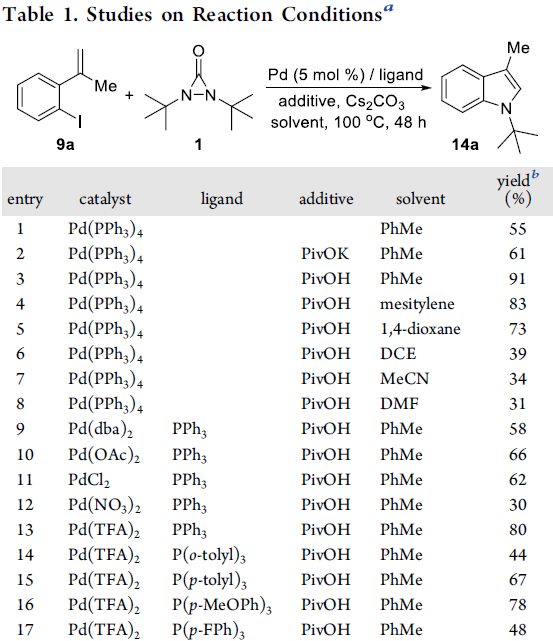
首先,作者以2-碘苯乙烯9a和二叔丁基二氮丙啶酮1作为模型底物,进行了相关反应条件的筛选(Table 1)。反应最佳条件为:以5 mol%的Pd(PPh3)4为催化剂,5 mol%的PivOH为添加剂,Cs2CO3(2.0当量)为碱,在甲苯溶剂中100 °C反应48 h,即可获得91%收率的吲哚产物14a。
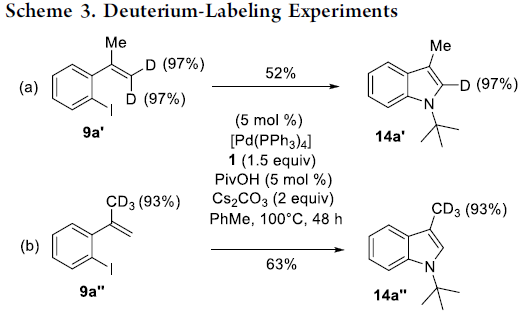
为了进一步了解反应的机理,作者进行了氘代实验(Scheme 3)。9a’在标准条件下反应,获得52%收率的14a’,并在吲哚的2-位上含有97%的D。9a″在标准条件下反应,获得63%收率的14a″,其中甲基含有93%的D。这些结果表明,反应是通过将Pd氧化加成至芳基碘化物并随后进行乙烯基C-H活化而选择性进行的(Scheme 2, path b)。
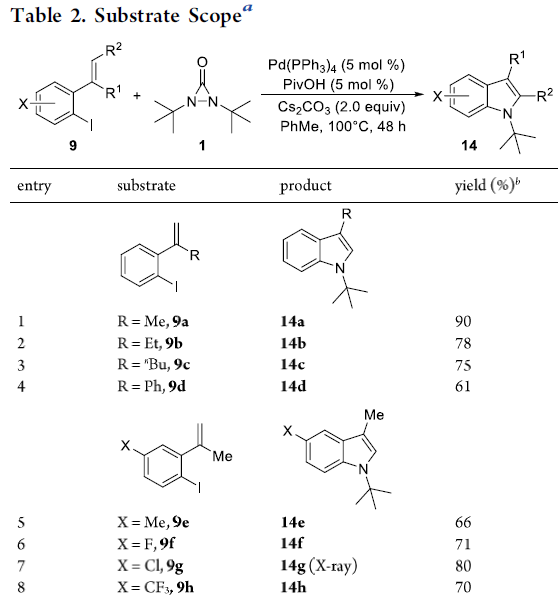
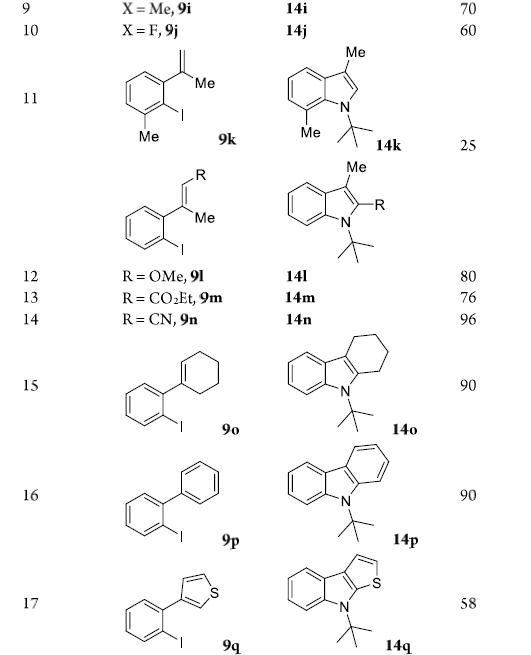
在获得上述最佳反应条件后,作者开始对2-碘苯乙烯底物9进行了扩展(Table 2)。对于二取代的末端烯烃,如-Me、-Et、-Bu和-Ph,以61-90%的收率获得吲哚14a–14d。同时,具有不同芳基取代的底物,如-Me、-F、-Cl、-CF3等,均可耐受,以60-80%的收率得到相应的产物14e–14j。值得注意的是,若将甲基取代基引入碘化物的邻位时,产物14k的收率很低(25%),可能与空间位阻有关。此外,对于三取代的烯烃,均可顺利反应,以76-96%的收率获得相应的产物141–14n。对于含有环状烯烃9o、咔唑基14p和噻吩基9q底物,均可耐受,获得相应的产物14o–14p。然而,含有呋喃基的底物未发生反应。
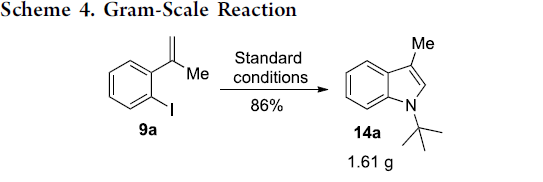
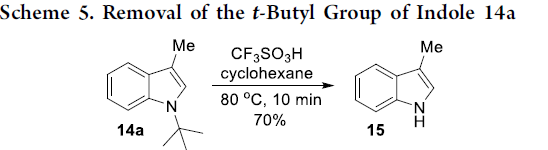
紧接着,作者对反应的实用性进行了研究。9a的克级实验,可获得86%收率的吲哚化合物14a(Scheme 4)。同时,化合物14a可在CF3SO3H的环己烷溶剂中反应,可轻松除去叔丁基,以70%的收率得到脱保护的吲哚15(Scheme 5)。
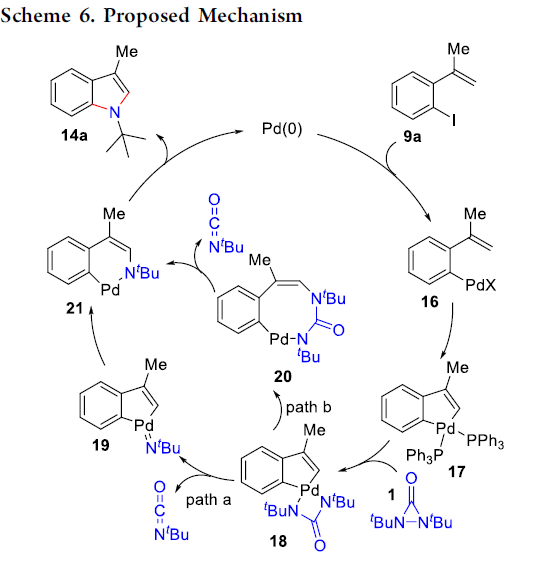
随后,作者提出了一种可能的反应机理(Scheme 6)。首先,Pd(0)催化剂氧化加成至芳基碘化物上,形成芳基Pd(II)配合物16,经分子内乙烯基C-H活化生成钯(II)环配合物17。随后,配合物17与二叔丁基二氮丙啶酮(1)反应,生成钯(IV)环配合物18。在Path a中,配合物18释放异氰酸叔丁基酯,生成Pd(IV)-氮杂环丁烷19,再经连续两次还原消除形成吲哚14a,并再生Pd催化。在Path b中,配合物18通过还原消除形成八元钯(II)环配合物20,再释放异氰酸叔丁酯以及经还原消除后,即可获得吲哚14a。
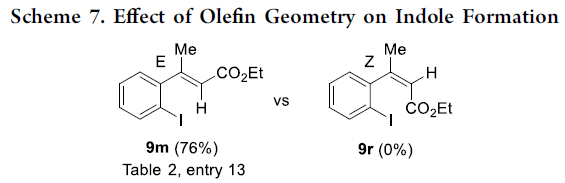
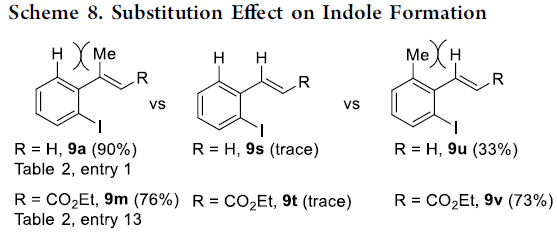
此外,作者还对空间位阻和取代效应进行了研究。当使用(E)-三取代烯烃9m和(Z)-三取代9r在标准条件下反应时,仅有(E)-9m顺利反应,获得76%收率的14m,从而表明吲哚形成涉及分子内乙烯基C-H键的活化(Scheme 7)。同时,烯烃取代基对反应也至关重要(Scheme 8)。当α-甲基苯乙烯中的甲基被去除时,收率从90%下降到不足5%(9a vs 9s)。但当将甲基邻位引入乙烯基时,会形成大量的吲哚(9u vs 9s)。在9m、9t和9v下也观察到了相同的趋势。这些结果表明乙烯基和苯基之间的空间排斥可以促进C-H键的活化。
总结
常州大学史一安教授课题组报道了一种高效的钯催化连续C-H活化/胺化反应的策略,以2-碘苯乙烯和二叔丁基二氮丙啶酮为底物,可获得一系列高收率的吲哚衍生物。同时,该反应涉及将Pd氧化加成至芳基碘中,再将乙烯基C-H键活化为钯(II)环中间体,随后通过二叔丁基二氮丙啶酮将其进行双胺基化反应,从而得到吲哚产物。


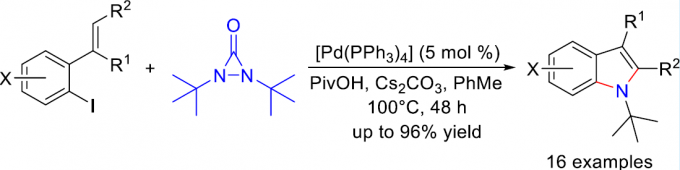

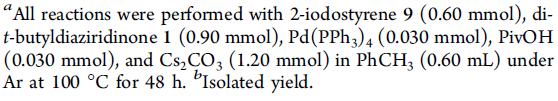
















No comments yet.