本文作者:孙苏赟
第四部分 Sharpless AD (1)
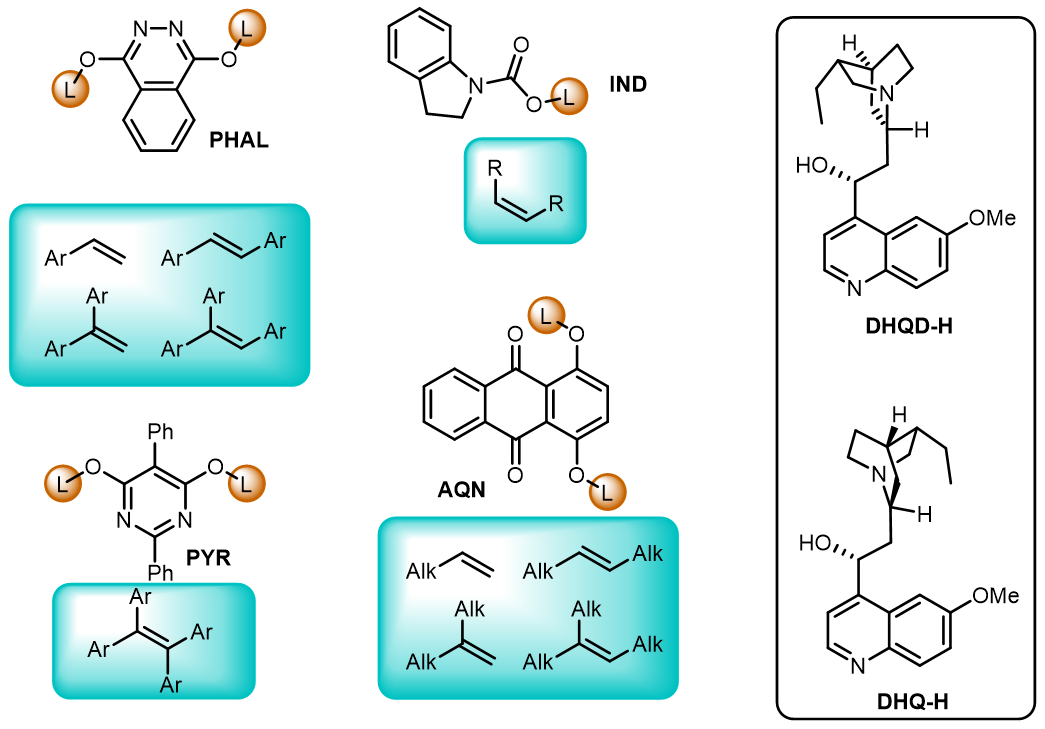
在发现了PHAL作为反应配体后,在后续的研究中还开发出了另外几种配体,他们分别适用于不同取代的双键:
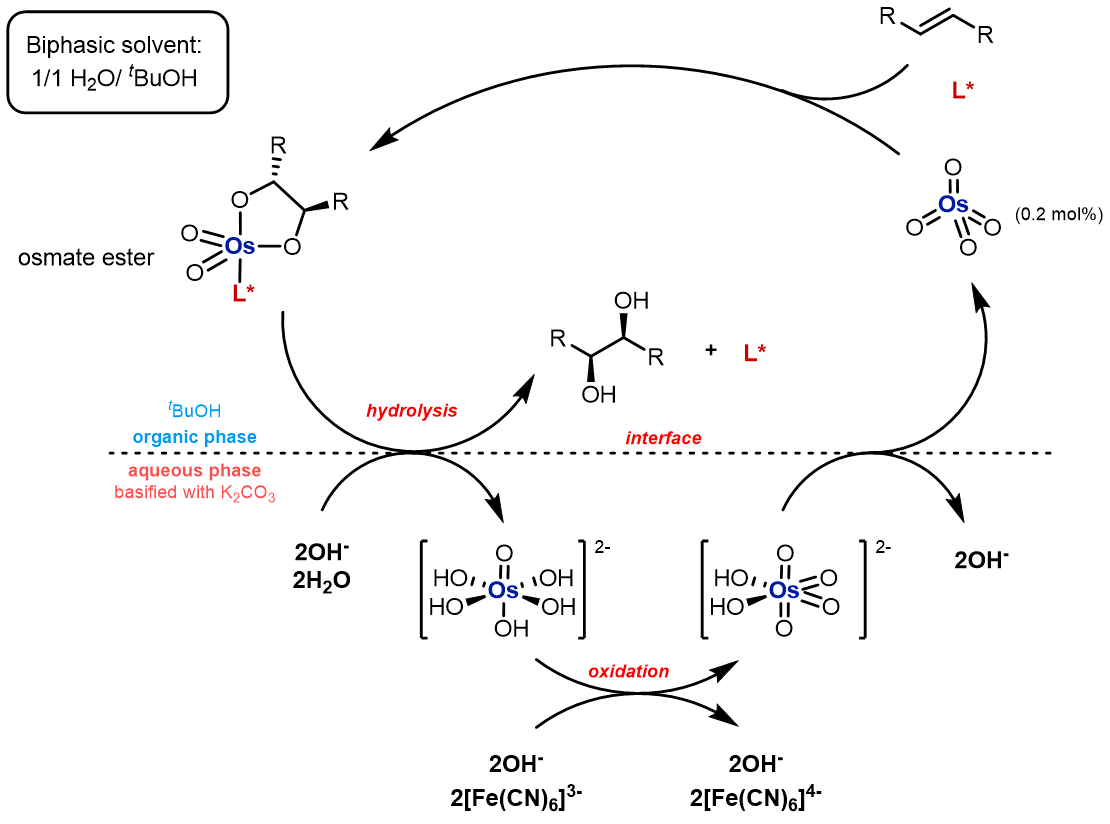
反应的过渡态是在U-形配合物的作用下和中心金属发生作用,以AD-mix-β为例:[1]
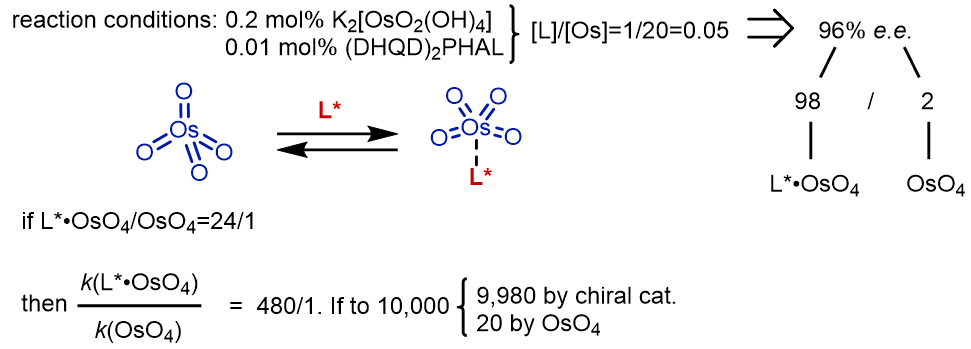
从过程上来看,反应中存在一个副反应:
由如上催化循环可见,反应体系主要分为两个循环,第一循环是理想的不对称催化,有含氮配体参与的反应产生ee值很高的双羟化产物;第二循环则是一个副反应,反应得到的低ee值很低的产物。
我们来做一个简单的计算:
如果Ti催化剂的效率是自行车,那么Os催化剂的效率则可以和法拉利媲美。
也有两相反应的例子[2]:
一些不对称催化的例子:
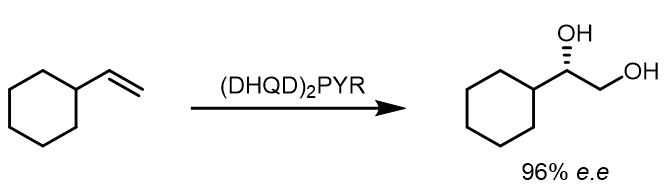
(1) 端位双键的AD一般因为大位阻很难进行,因此在这里使用了PYR最为配体,如果使用(DHQD)2PHAL作为配体仅有88%的ee值:[3]
(2) 一个选择性和立体化学模型相反的例子:[4]
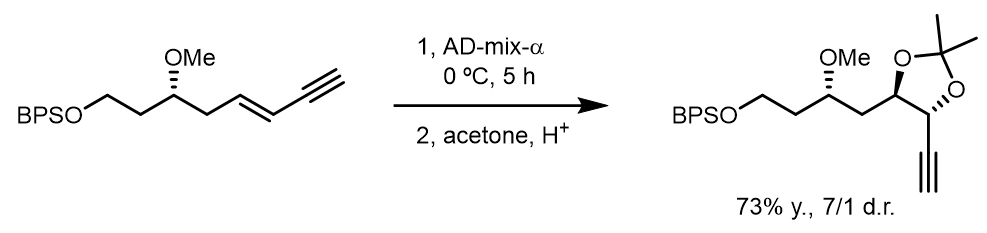
(3) 立体选择的双羟化反应-二醇保护的串联反应:[5]
而且反应不会影响炔烃。
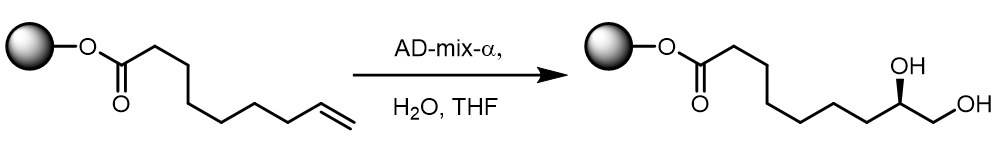
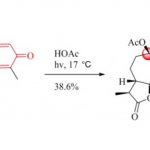
(4) 也可以用于固相合成:
此处使用THF而不是使用叔丁醇,是因为可以使得高分子发生溶胀而产生更大的表面积参与反应。
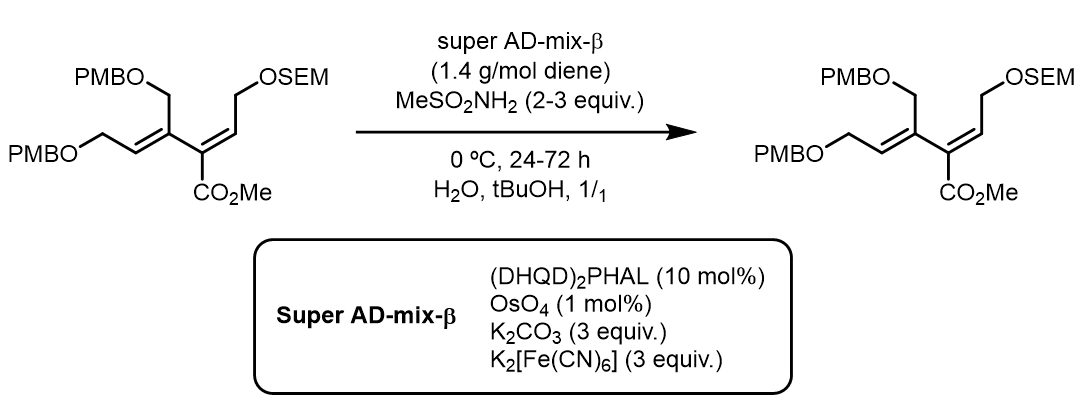
(5) Super AD-mix-β条件:[6]
这个反应中,选择性地发生在了有吸电基团取代的双键上,但是反应的ee值不是非常好。
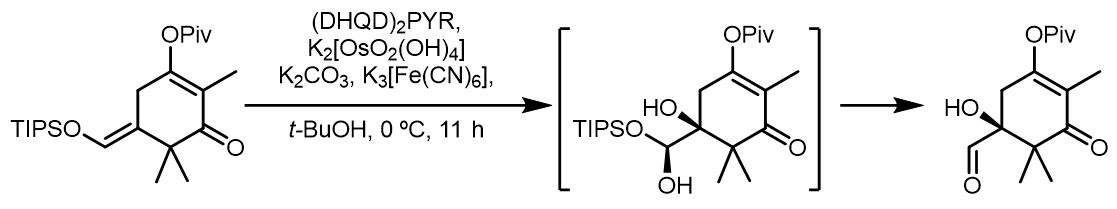
(6) 烯醇醚的反应:[7]
相同的,如果反应使用(DHQD)2PHAL作为配体,反应的立体选择很不好,只有26% ee值。
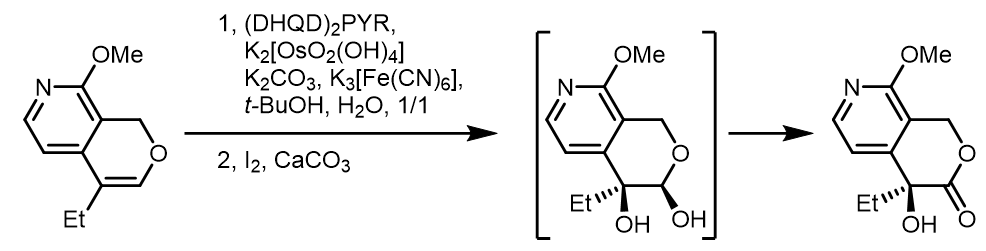
(7) 烯醇双羟化异构串联反应:[8]
这个反应和Rubottom氧化反应的过程类似。
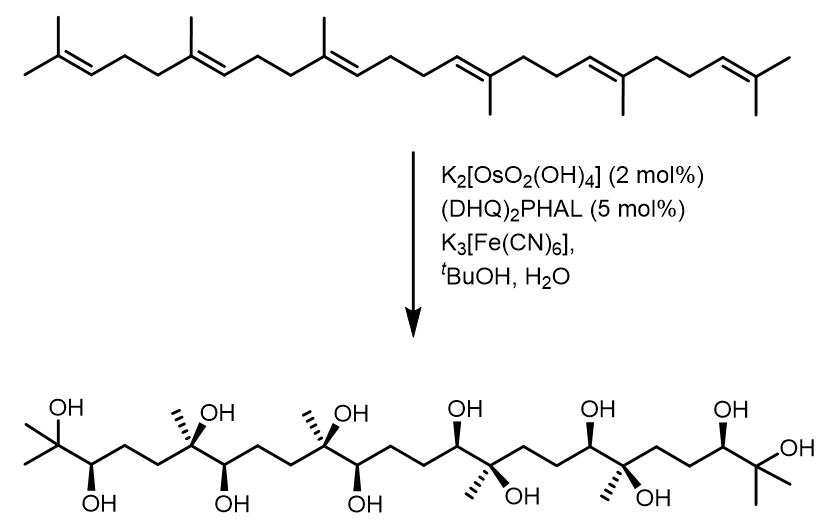
(8) 多烯烃的双羟化:[9]
References
- [1] Tetrahedron Lett. 1995, 36, 3481. DOI: /10.1016/0040-4039(95)00570-3
- [2] Tetrahedron Lett. 1990, 31, 2999. 1016/S0040-4039(00)89008-5
- [3] J. Org. Chem. 1993, 58, 3785-3786. DOI: 10.1021/jo00067a002
- [4] Angew. Chem. Int. Ed. 2008, 47, 3426. DOI: 10.1002/anie.200800253
- [5] J. Am. Chem. Soc. 2001, 123, 4834-4836. DOI: 10.1021/ja0105055
- [6} Chem. Eur. J. 1995, 1, 467. DOI: 10.1002/chem.19950010712
- [7] J. Org. Chem. 1994, 59, 6142-6143. DOI: 10.1021/jo00100a006
- [8] J. Am. Chem. Soc. 2000, 122, 3811-3820. DOI: 10.1021/ja9939439
- [9] Science, 1993, 259, 64. DOI: 10.1126/science.8418495
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!



















No comments yet.