概要
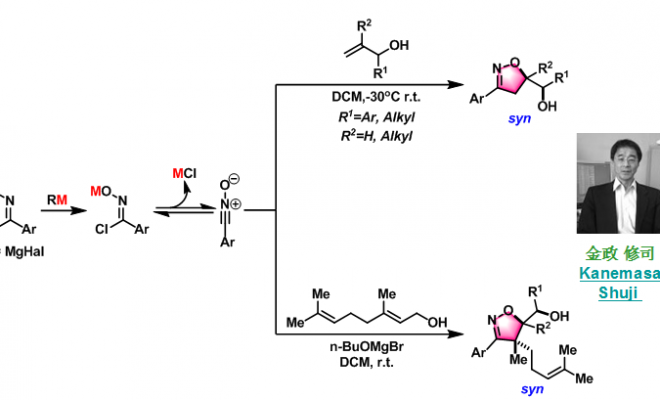
1991年由日本山口县立大学(Yamaguchi University)的金政修司(Kanemasa Shuji) 研究组报道了腈氧化物(通常由hydroximinoyl chlorides与Grignard 试剂原位反应产生)与烯丙醇或高烯丙醇之间进行的1,3-偶极环加成反应,称为Kanemasa反应。该反应为首例成功地通过金属配位控制而进行的1,3-偶极环加成,反应具有良好的区域及立体选择性(syn-选择性)。随后,该课题组将底物范围扩展至N-苯甲酰亚甲基苯胺-N-氧化物,成功获得异噁唑啉-5-醇及异噁唑啉-4-醇。该反应目前已广泛应用于4-取代-5-羟甲基二氢异噁唑及4,4-二取代-5-羟甲基二氢异噁唑类化合物及其相关衍生物的立体选择性合成。
基本文献
- S. Kanemasa, S. Kobayashi, M. Nishiuchi, H. Yamamoto, E. Wada, Tetrahedron Lett. 1991,32,6367. doi: 10.1016/0040-4039(91)80171-2.
- S. Kanemasa, M. Nishiuchi, E. Wada, Tetrahedron Lett. 1992, 33, 1357. doi: 10.1016/S0040-4039(00)91622-8.
- S. Kanemasa, T. Uemura, E. Wada, Tetrahedron Lett. 1992, 33, 7889. doi: 10.1016/S0040-4039(00)74770-8.
- S. Kanemasa, T. Uemura, E. Wada, Tetrahedron Lett. 1993, 34, 87. doi: 10.1016/S0040-4039(00)60064-3.
- S. Kanemasa, M. Nishiuchi, A. Kamimura, K. Hori, J. Am. Chem. Soc., 1994, 116, 2324. doi: 10.1021/ja00085a012.
- S. Kanemasa, T. Tsumoka, H. Yamamoto, Tetrahedron Letters 1995, 36, 5019. doi: 10.1016/0040-4039(95)00911-U.
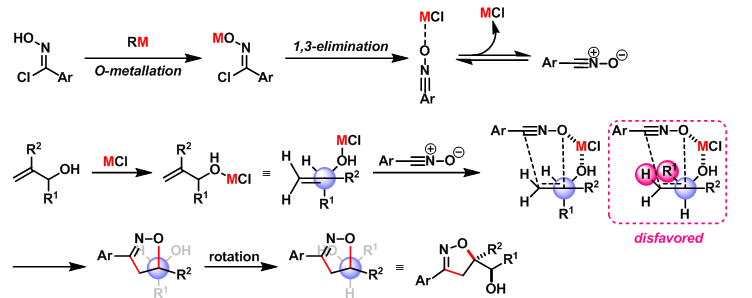
反应机理
[1] J. Tanaka, S. Kanemasa, Tetrahedron 2001, 57, 899. doi: 10.1016/S0040-4020(00)01045-0.反应实例
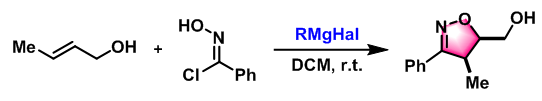
4-取代-5-羟甲基二氢异噁唑的合成[1]
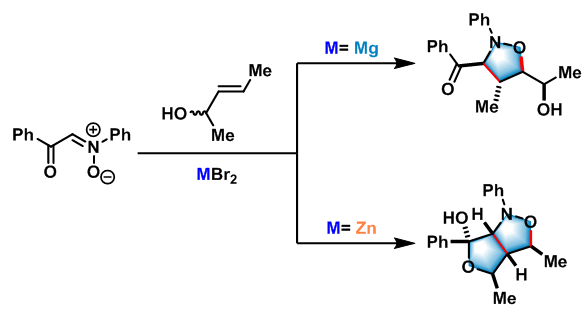
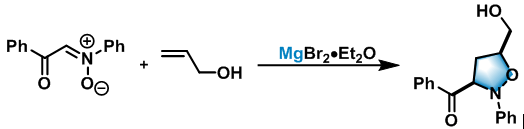
异噁唑啉-5-醇的合成[2]
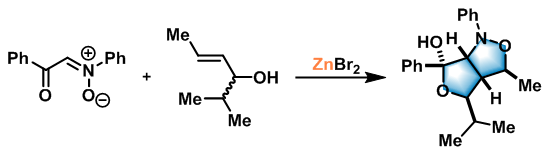
异噁唑啉-4-醇的合成[3]
实验步骤
氮气气氛下,在-78 oC,将EtMgBr (1 M的THF溶液, 1 eq.) 加入到benzohydroximinoyl chloride (1 eq.)的无水DCM (底物浓度为0.1 M)溶液中。维持-78 oC,搅拌for 10 min后,向上述混合物中加入烯丙醇 (1 eq.)。继续维持该温度,搅拌10 min后,将上述反应液升温至-30 oC,继续搅拌至反应完成。反应结束后,加入饱和氯化铵溶液淬灭反应,淬灭结束后,再加入DCM进行萃取。将合并的有机相采用无水MgSO4 进行干燥,并加压除去溶剂。粗产物采用硅胶柱色谱进行分离纯化(正己烷/乙醚 1: 1 v/v作为洗脱剂)获得相应二氢异噁唑类化合物。
实验技巧
参考文献
- S. Kanemasa, M. Nishiuchi, E. Wada, Tetrahedron Lett. 1992, 33, 1357. doi: 10.1016/S0040-4039(00)91622-8.
- S. Kanemasa, T. Uemura, E. Wada, Tetrahedron Lett. 1993, 34, 87. doi: 10.1016/S0040-4039(00)60064-3.
- S. Kanemasa, T. Tsumoka, H. Yamamoto, Tetrahedron Letters 1995, 36, 5019. doi: 10.1016/0040-4039(95)00911-U.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.