概要
在现有的肽合成中,随着分子量的增加,官能团之间的相互作用呈指数增长,并且当反应点”潜入”多肽结构内部,这样就使得后续修饰反应更难以进行。比如说,后续如果要进行缩合反应修饰的话,反应活性会大大降低,通常液相反应最大也只能连10个残基,即使是固相合成最大也就50个残基,就已经到了极限了。
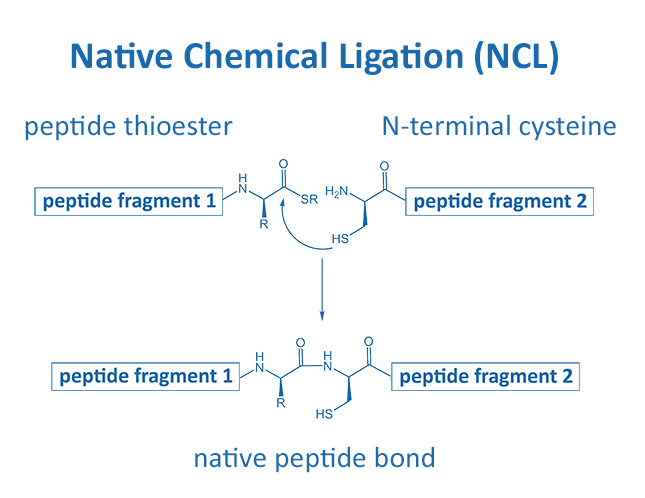
Native Chemical Ligation(NCL)法可以有效克服这种障碍 。
将在C-末端具有硫酯的肽和在N-末端具有未保护的半胱氨酸的肽,在生物相容性条件下(pH 7、20℃~37℃)混合就可以进行反应,并不需要加入多余的活化试剂。对于侧链无保护的多肽也能高效反应得到很好的产率。该反应利用多肽中本身就具有的官能团(Native Functional Group),这一点是非常有价值的。通过这种方法,可以化学合成高达约200个残基的肽链。
基本文献
- Dawson, P. E.; Muir, T. W.; Clark-Lewis, I.; Kent, S. B. H. Science 1994, 266, 776. DOI:10.1126/science.7973629
- Johnson, E. C. B.; Kent, S. B. H. J. Am. Chem. Soc. 2006, 128, 6640. DOI: 10.1021/ja058344i
<Review of NCL>
- Dawson, P. E.; Kent, S. B. H. Annu. Rev. Biochem. 2000, 69, 923.
- Clark, R. J.; Craik, D. J. Pept. Sci. 2009, 94, 414. DOI: 10.1002/bip.21372
- McGrath, N. A.; Raines, R. T. Acc. Chem. Res. 2011, 44, 752. DOI: 10.1021/ar200081s
- Raibaut, L.; Olivier, N.; Melnyk, O. Chem. Soc. Rev. 2012, 41, 7001. DOI: 10.1039/C2CS35147A
- Wong, C. T. T.; Tung, C. L.; Li, X. Mol. Biosys. 2013, 9, 826. DOI: 10.1039/C2MB25437A
<General Review of Chemical Synthesis of Peptides/Proteins
- Humphrey, J. M.; Chamberlin, A. R. Chem. Rev. 1997, 97, 2243. DOI: 10.1021/cr950005s
- Bray, B. L. Nat. Rev. Drug Discov. 2003, 2, 587. doi:10.1038/nrd1133
- Nilsson, B. L.; Soellner, M. B.; Raines, R. T. Annu. Rev. Biophys. Biomol. Struct.2005, 34, 91. DOI: 10.1146/annurev.biophys.34.040204.144700
- Kent, S. B. H. Chem. Soc. Rev. 2009, 38, 338. DOI: 10.1039/b700141j
- Pattabiraman, V. R.; Bode, J. W. Nature 2011, 480, 471. doi:10.1038/nature1070
- Stolzew, S. C.; Kaiser, M. Synthesis 2012, 44, 1755. DOI: 10.1055/s-0031-1289765
反应机理
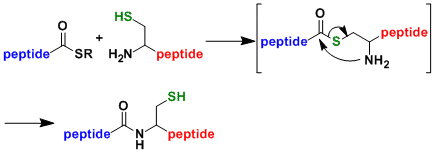
S-to-N酰基转移是本反应的关键过程。第一个硫酯交换过程是可逆的。即使在内部含有半胱氨酸以外的部位存在硫醇官能团,也不会影响反应。从不同的角度来看,一定程度上,也可以通过使用适当的硫醇作为催化剂来加速反应。
反应实例
通过还原脱硫反应、可以把Cys残基选择性的变换成Ala。[1]
4-巯基苯基乙酸(MPAA)、2-巯基乙磺酸(MESNa)可以作为催化剂进行作用。
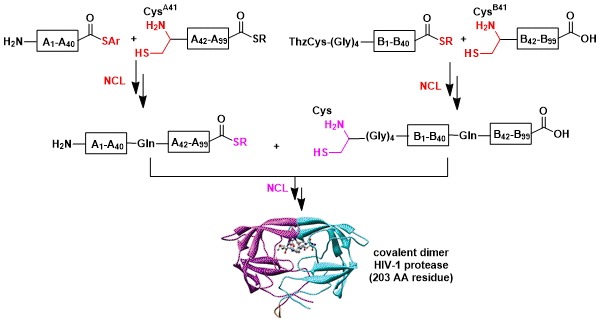
Kent等人,通过NCL法合成了、HIV-1蛋白酶Covalent Diverが[2]。它是当时用化学方法合成的最大的肽(2009年)。
实验步骤
实验技巧
参考文献
[1] Yan, L.Z.; Dawson, P.E. J. Am. Chem. Soc. 2001, 123, 526. DOI: 10.1021/ja003265m[2] Torbeev, V. Y.; Kent, S. B. H. Angew. Chem. Int. Ed. 2007, 46, 1667. DOI: 10.1002/anie.200604087
关联反应
外部链接
- 缩合反应(Wikipedia)
- Peptide(Wikipedia)
- Condensation Reaction(Wikjpedia)
- Native Chemical Ligation – Wikipedia
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!
















No comments yet.