2022年7月6日,日本京都大学大木靖弘(Yasuhiro Ohki)教授课题组在专业杂志Nature上在线发表了题为 「Nitrogen reduction by the Fe sites of synthetic [Mo3S4Fe] cubes」的科技论文,该研究设计了基于金属–硫磺团簇的高效化学催化剂,实现了高效的氮还原反应并解释了天然FeMoco酶活性中心的固氮分子机理。该成果开启了人工固氮催化反应的新思路,基于该思路可扩展更多高效的化学催化剂。

https://www.kyoto-u.ac.jp/sites/default/files/2022-07/220707_ohki 2003a48d75b165bb711a9354b7cc07f4.pdf
01研究亮点
- 基于FeMoco酶活性中心的结构设计并合成了新型的人工固金属-硫磺簇配体催化剂
- 讨论了N2如何与FeMoco结合的分子机理
- 试探性地解释了FeMoco在没有蛋白质保护的情况下不还原N2的原因
02研究概要
【背景】
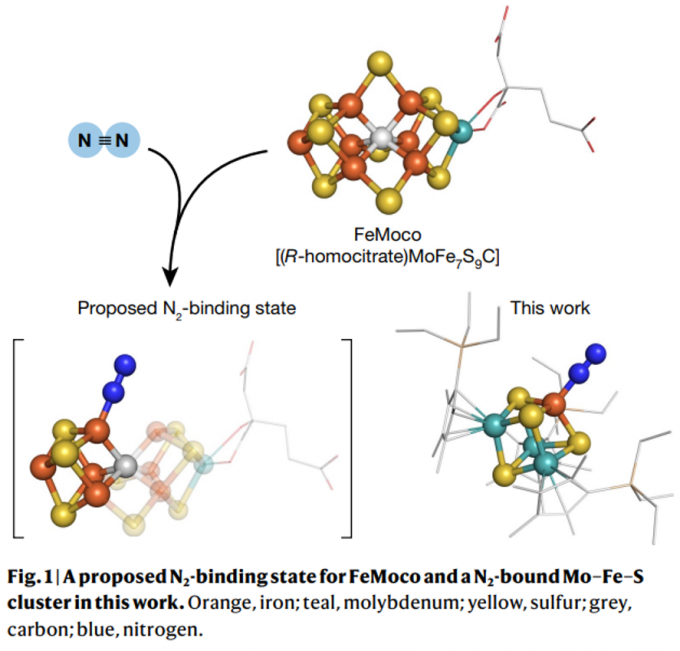
固氮作用(N2还原反应)将大气中的氮分子(N2)转化为氨(NH3)等生物体可利用的分子,可合成氨基酸和贡献DNA中所含的氮原子而维持生命活动。另一方面,N2具有对称结构,具有强 N≡N 三键,反应性极差,被称为惰性气体,因此N2的还原反应极难进行。在自然界中,存在于某些微生物中的固氮酶负责N2还原反应,但仅此反应无法涵盖能够支持地球上人口粮食生产的氮量。通常,NH3是由N2和氢分子(H2)在高温高压条件下通过Haber-Bosch法合成的,这是一种由铁和钌催化的工业反应。这种工业反应消耗化石燃料作为H2的原料,并产生大量的CO2。如果能够人工复制不依赖化石燃料的酶反应,就有可能为可持续社会提供一种新的N2还原技术。多年来,人们一直在尝试了解称为 FeMoco 的酶活性中心的功能(图1)并重现其结构和功能,它由铁(Fe)、钼(Mo)、硫(S ) 和碳 (C)构成。然而,由于金属原子和硫原子以三维排列的FeMoco结构复杂,很难解释它与N2还原的关系。此外,FeMoco对N2的还原受到蛋白质的保护。因此,由金属和硫合成的FeMoco金属-硫簇络合物不能还原N2,它是解开N2还原功能之谜的障碍。
【结果与讨论】
本文中,研究小组讨论(1)N2如何与FeMoco结合;(2)FeMoco在没有蛋白质保护的情况下为什么不还原N2。生化领域发现,在FeMoco的中心部分去除了一个交联两个FeS的S原子,合理地认为Fe中产生的空位(反应点)吸收了N2。但是,由于将所示的预测结构(图1左下)以完美的形式合成是不容易的,所以研究组大胆简化,重点关注预测结构的左半部分,然后重点关注预测结构的左半部分,通过含Mo,Fe和S的立方体的Fe来捕获N2。
由于N2更喜欢对称结构,例如,当它结合到称为 M 的金属中时,它倾向于像M-N2-M那样交联两个金属原子。结果表明:两个N原子都被金属M覆盖。因此,所需的N2转化反应不太可能发生。因此,重要的是形成末端N原子空置的Fe-N2结构,而不是N2交联的Fe-
N2-Fe结构。考虑到这些设计指南和结构要求,以及一些蛋白质功能,下一步重点是聚合问题。这是可预期的,没有蛋白质保护框架的FeMoco可以很容易在分子之间形成金属硫键并聚集。然而,这种聚合是实现N2还原功能的致命缺陷。这是因为反应性差的N2除非在Fe等金属中存在空位(反应点),否则无法吸收,但如果另一个分子中所含的S原子可以接近反应点,则 N2 会结合到金属中这是因为硫排出并形成新的强金属硫键,阻塞了反应点。在自然界中,将FeMoco深埋在蛋白质内部被认为可以避免聚集问题。
基于上述,研究组设计了一个以Fe为反应点的立方[Mo3S4Fe]簇络合物作为模拟FeMoco的分子,为了进一步抑制聚集,组建了三个在Mo上的配体(CpR,CpL和CpXL)。当根据设计指南合成的 [Mo3S4Fe] 簇络合物在充满N2的烧瓶中还原时,得到N2与Fe结合的簇络合物(图1右下)。此时,N2的结合方式会根据CpR配体而改变,使用CpR 配体时会改变Fe-N2-Fe结构,使用体积较大的CpL和CpXL配体时会使用末端。从分子结构和光谱测量证实产生了Fe-N2结构。随后,课题组以一系列[Mo3S4Fe]簇配合物为催化剂,研究了N2的还原反应。尽管NH3合成反应没有高效进行,但N (SiMe3) 3的转化反应(一种在溶液中进行的N2还原反应)却高效进行(封面)。揭示了每个Fe原子产生高达248当量的N (SiMe3) 3。这次实现的催化次数是使用铁络合物的传统记录的三倍以上。此外,即使将比较扩大到所有与过渡金属的配合物,本研究中的催化次数也与使用钴/钼配合物报道的最高值大致相同。
上述结果表明,研究小组报道的[Mo3S4Fe]簇络合物在简化的同时反映了FeMoco对N2还原作用的关键要素。研究组不仅在人工金属硫化合物的N2还原反应中迈出了第一步,而且还是一个很好的例子,表明可以通过学习酶和设计合适的分子来扩展金属硫化合物的可能性。
【研究意义及未来展望】
如上所述,课题组预测了负责固氮的复合酶活性中心FeMoco的结构与蛋白质的N2还原功能和部分功能之间的关系,并大胆地将这些点简化并体现在分子设计中。结果,研究组首次成功地用金属硫化合物还原了 N2。然而,这一成就只是第一步。今后,如果能够不经简化地合成的预测结构(图1左下),并且能够实现用于N2还原反应的最佳金属元素,从而实现超过酶的催化活性,则新的N2有助于将实现可持续发展的社会。
本研究由京都大学,名古屋大学,夏威夷大学,科伦坡大学和东京大学共同合作完成;第一作者和通讯作者为大木靖弘(Yasuhiro Ohki)教授。本文受到「JST CREST (JPMJCR21B1)、JSPS科学研究費補助金(19H02733, 20K21207, 21H00021, 21K20557)、武田科学振興財団、立松財団、矢崎科学技術振興記念財団、京都大学化学研究所 国際共同利用・共同研究拠点補助金、京都大学若手研究者スタートアップ支援」的研費经费支持。
03
—
作者介绍
大木靖弘(Yasuhiro Ohki)博士,京都大学化学研究所教授;Ohki教授致力于开发高效能量转换材料和合成工艺的基础研究,是分子团簇设计研究领域的青年学者;在Nature, Nature系列, PNAS,JACS等国际知名科学杂志发表研究型论文100余篇。其研究成果被引用近4000次,其中单篇最高引用数达220余次,h指数为37 (Google Scholar)。
————————————–华丽分割线———————————-
关注化学空间,追踪前沿方向!
文章投稿和合作请联系微信 ylyl5200




















No comments yet.