俯瞰有机反应前两回简单介绍了一些重排反应σ迁移反应,[1,2] 重排,这次,小编准备归纳下加成-消去反应。说到加成-消去反应,主要以亲核酰基化反应作为代表,常常局限于糖基化合物的芳香环亲核取代反应。接下来,让我们一起来看一下这类反应的电子转移机理,以及它们的共同点。
基本的机理画法 -攻击与离去
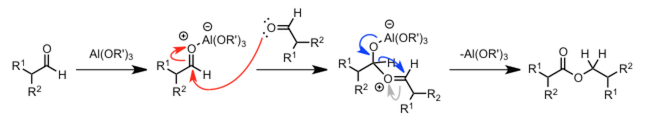
首先下图给出了最简单的一类反应-酯基的水解反应。
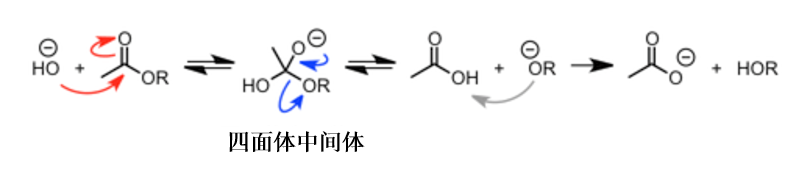
该反应的反应机理主要可以阐述为以下三步。
- 首先,羟基负离子供给羰基的碳。在这个阶段,羰基的π 键断裂,原来的 π 电子转移到电负性大的氧上,形成带有氧负电子的碳四面体结构的中间体。
- 通过醇羟基的离去,该四面体中间体重新形成含有羰基的羧酸产物。
- 生成的羧酸再与醇羟基进行质子交换,反应往最右边进行。
这一连串的反应中的电子流动的要点为
亲核剂进攻羰基碳、氧负离子推动离去基团的离去
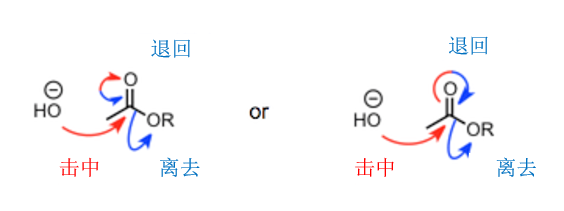
整体的慢动作回放可以看下面两个图,我们可以很明白的看出电子的流动首先是回到氧上形成氧负离子后,氧上面的孤对负电子再退回来,推动离去性更好的醇羟基的离去。
这种以「进攻(addition)、离去(elimination)」为基本形式的机理进行的反应,主要以羧酸衍生物的亲核酰基化取代反应(酰卤或者酸酐的酯基化,酰胺化,羧酸合成)等为代表。除此以外,另一类比较代表性的是芳香族亲核取代反应。
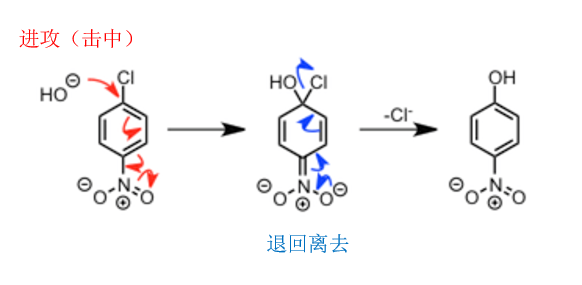
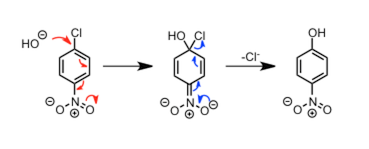
图中用了很多箭头表示电子的移动,但是仔细看苯环只是作为一个电子传导的媒介。该反应首先作为亲核试剂的羟基负离子进攻硝基的对位的苯环上π电子。接着电子按照一连串的红色箭头所示进行移动,最后电子停留在对负电子具有强力兼容性的强吸电性的硝基上。接下来,电子从硝基上开始退回,离去Cl负离子后,芳香环得到再生。这里重要的是,刚开始的羟基负离子是进攻的π电子,最后离去Cl负离子得到产物。简单的可以用下图表示。
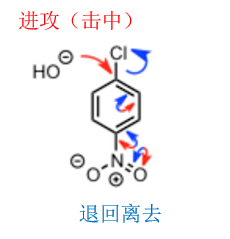
亲核试剂进攻哪里是个问题。
到此为止,小编主要介绍了一下电子的流动,很多人会发现最初的亲核试剂进攻哪里是反应发生的关键,那么接下来就主要来讲下怎么考虑某个反应是如何发生的,并且如何进行的。
首先第一阶段、亲核试剂的进攻对象
- 碳-杂原子的不饱和键 (C=O, C=N等)
- 与吸电子基团共轭的不饱和键
以上两种可能性比较大。对于1来说,最常见的就是羰基了。羧酸衍生物以外的话,还有进攻C=N 的碳的 Chichibabin 反应(具体请看最后的反应列表)。另外对于2.来说,需要注意的是,例如芳香族亲核取代反应的话,离去基团与吸电基团的相对位置的不同,需要区别考虑(比如说下图所示的硝基在间位的情况)。
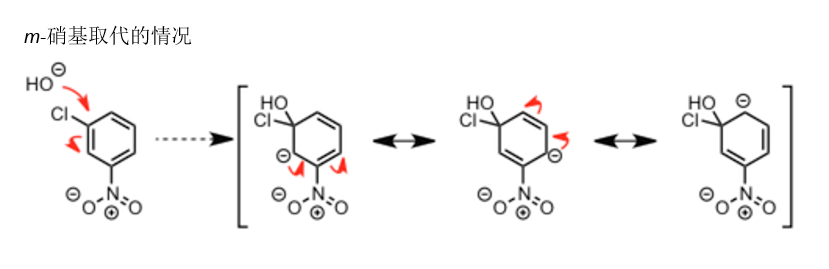
在该情况下,离去基团与吸电子的硝基并不共轭,亲核剂即使可以进攻苯环上的Cl旁的双键,但是由于硝基上的负电荷无法返回,所以上述反应是无法发生的。由于碳的电负性并不大,所以带负电荷的碳中间体是很难生成的,因此上图所示机理不可行。
而当离去基团在吸电子硝基的共轭位置(邻位或者间位)的情况下,如下图所示移动到硝基上的负离子,由于氧的电负性较大,电子的兼容性也强,最后通过苯环为媒介返回,推动氯的离去,完成整个反应。
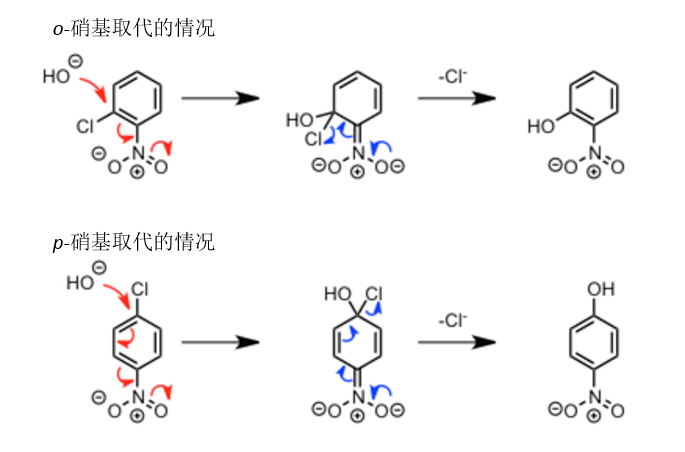
当反应机理中有负离子生成的时候,一般得先让负离子通过共轭电子移动到电负性强的原子上,然后再返回推动离去基的离去完成反应,而不是停留在一些比如碳上形成非常不稳定的碳负离子,当然也有例外。而这一点基本的非常重要,希望初学者能够明记。
哪个能成为离去基团?
接下来就是离去基团的判断,简单的说一般离去后形成的负离子状态最稳定的最容易离去,有的书中也常常以pKb的大小来判断离去性强弱。比如酮的烷基与醛的氢,如果作为离去基团离去后变成烷基负离子与氢负离子,都是极其不稳定的,所以一般不能作为离去基团。
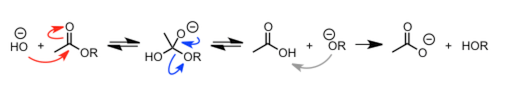
对于离去基团的选择,我们回到最初的酯水解的例子进行解说。仔细看可以发现,从羟基负离子进攻羰基,到醇羟基离去的过程,用了平衡箭头表示,这是为什么?
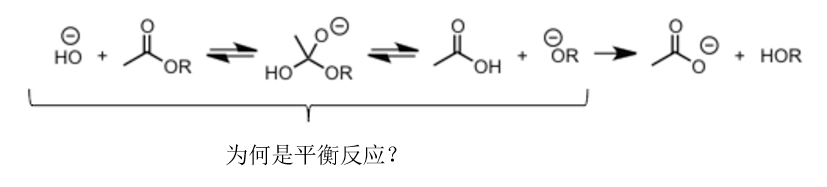
事实上,这是因为亲核剂进攻羰基后形成的左侧的羟基也是有可能离去的。也就是说,如果醇羟基离去的话,反应往右进行,如果羟基离去的话反应还是回到最初,往左进行。因此在这个阶段的反应是可逆的。(如下图所示)
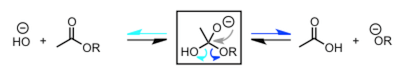
四面体中间体中的氢氧化物负离子或者醇羟基都有可能离去
但是,当醇羟基离去后生成物是羧酸,而接下来,羧酸的酸性氢被离去的醇羟基负离子捕获,该反应是不可逆的。因此反应整体是往右进行的。也就是说,酯的水解反应中碱是等量消耗,使得反应向右进行的。
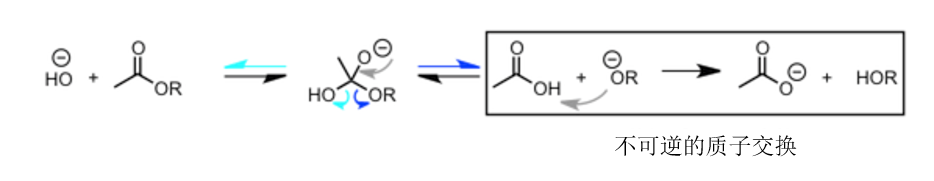
醇羟基离去的情况下,通过不可逆的质子交换使得反应向右进行。
总结一下就是说「亲核剂与离去基在具有相同程度的离去能的时候,一直到离去阶段都是一个可逆过程,所以必须以平衡箭头表示」。虽说画反应机理时,代表电子流动的箭头非常重要,但是每个阶段反应是可逆的还是不可逆的,尤其是rate-determination在哪个阶段,这个至关重要。以此来判断,哪一步的不可逆反应驱动了平衡反应,使得整个反应往产物方向进行的。如果能做到这点,那么我想对于有机反应的理解肯定是比一般的人要深刻。
综上,这一次单纯的主要以羰基的亲核取代反应,芳香族的亲核取代反应为例子讲解了一下这类反应的机理,共同点等。其他的类似反应小编也归纳了一下,以下面表格的形式给出。有不足之处,请各位读者大神们指出。
| 反应名 | 关键阶段 | 备注 | |
| 酯水解 | 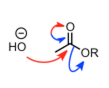 |
亲核的酰基化反应也是一样。 | |
 |
|||
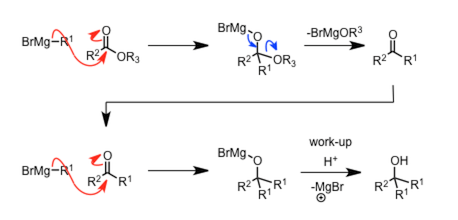
| 酯的Grignard 反应 | 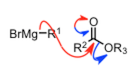 |
通过亲核进攻消除形成酮,但是形成的酮也能再次被Grignard试剂亲和进攻,形成醇。 | |
 |
|||
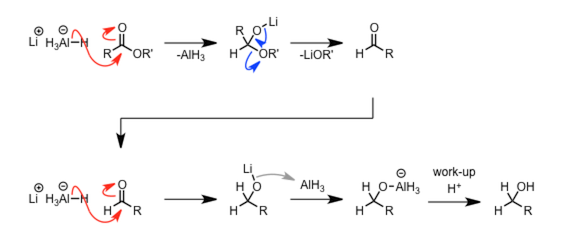
| 酯的 LAH 还原 | 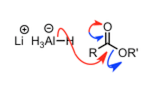 |
对酯的亲核进攻消除先形成醛,醛再次被还原形成醇。 | |
 |
|||
| Claisen 缩合 | 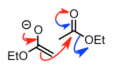 |
醇羟基的离去先形成 β-酮酯,但是还会被碱拔去酸性氢发生不可逆脱质子化形成烯醇。 | |
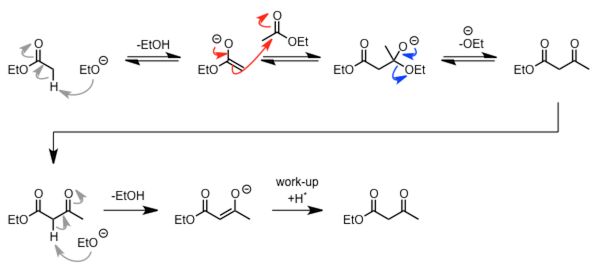 |
|||
| 芳香族亲核取代反应(SNAr) | 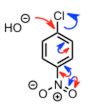 |
||
 |
|||
| Chichibabin 反应 | 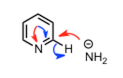 |
||
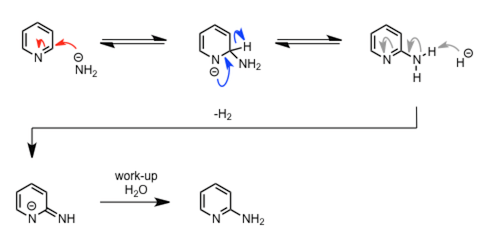 |
|||
| Smiles 重排 | 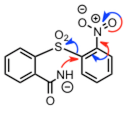 |
||
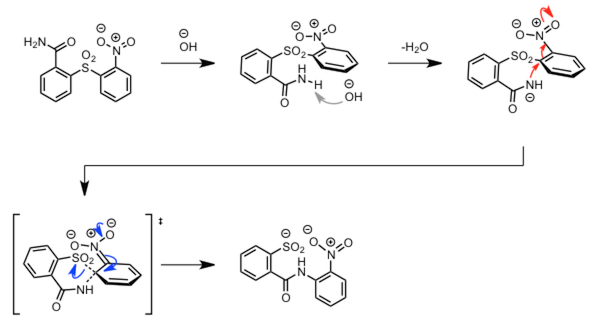 |
|||
| Julia-Kocienski 烯烃合成 | 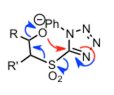 |
反应机理与 Smiles 类似,但是形成的是烯烃产物。 | |
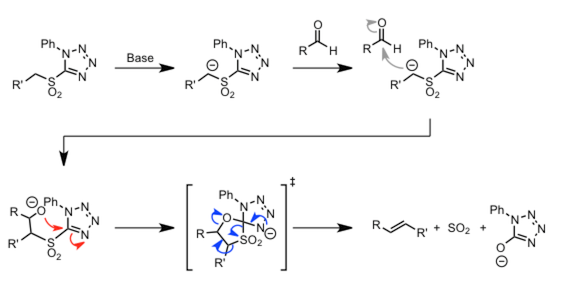 |
|||
| Cannizzaro 反应 | 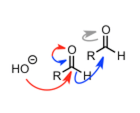 |
虽然说氢负离子通常是无法离去的,但是在高浓度的碱性条件下,通过四面体中间体的脱质子化,中间体负离子增强,从而导致氢的离去。 | |
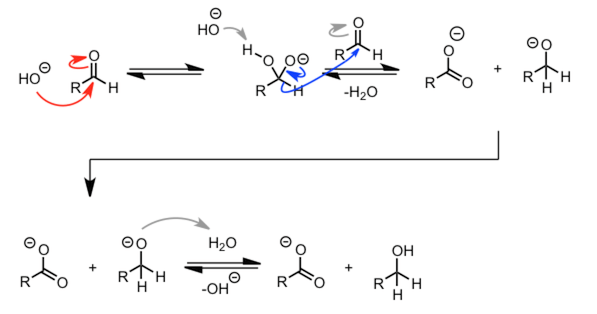 |
|||
| Tishchenko 反应 | 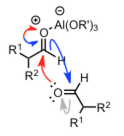 |
||
 |
|||
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!





















No comments yet.