本文作者:杉杉
导读
虽然C-B键的自由基裂解已是一种实现C-H功能化的有效策略,但实际上仍具有一定的挑战。近日,南开大学汪清民教授课题组在Green Chem.发表论文,报道了一种温和的电氧化方法,可通过烷基硼酸(酯)和三氟硼酸烷基酯的自由基加成反应,实现喹喔啉-2(1H)-酮的C-H烷基化反应,获得C-C偶联产物。
Electro-oxidative C-H Alkylation of Quinoxalin-2(1H)-ones with Organoboron Compounds
Kaikai Niu, Yanke Hao, Lingyun Song, Yuxiu Liu and Qingmin Wang*
Green Chem. ASAP DOI:10.1039/D0GC03892J
正文
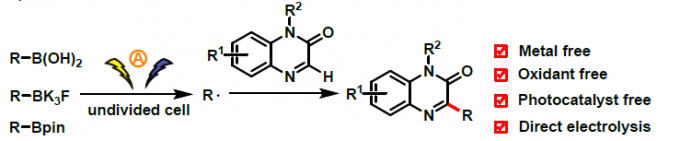
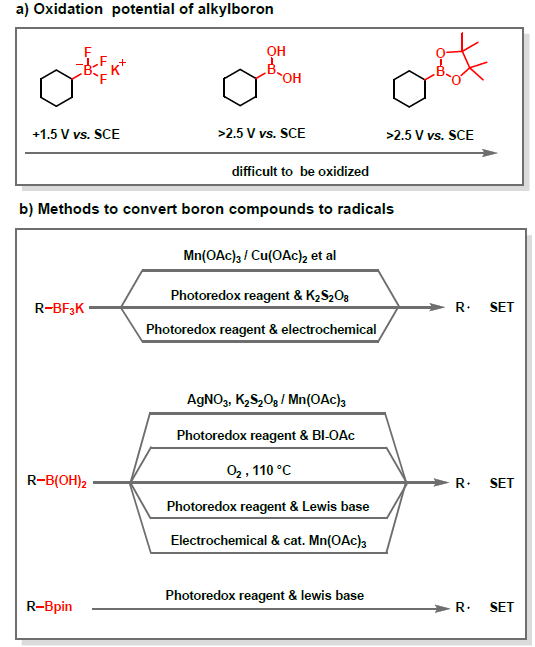
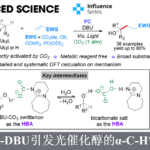
碳自由基,是构建C-C键反应中常用的中间体。在温和条件下通过有机硼化合物的去硼化过程,可生成烷基自由基。但由于C-B键具有高氧化电位(Scheme 1a),它们的裂解需要苛刻的条件。在经典方法中(Scheme 1b),三氟硼酸烷基酯和硼酸需化学计量的强氧化剂(如AgNO3/K2S2O8,Mn(OAc)3和Cu(OAc)2或O2)进行单电子氧化。三氟硼酸烷基酯也可在催化光氧化还原条件下进行单电子转移生成烷基自由基[1],同时,在路易斯碱催化下烷基硼酸和酯可通过光氧化还原活化而转化为烷基自由基[2]。电化学氧化作为一种绿色环保的策略,可替代传统的化学氧化剂,并使用电子作为清洁的可再生试剂。但硼酸衍生物的高氧化电位可能导致自由基二聚化或过氧化以生成碳正离子导致从阳极产生烷基自由基的方法仍未开发出来,。仅有少数文献报道关于氧化还原途径的例子,如光氧化还原催化剂[3]或Mn(OAc)3催化剂[4](Scheme 1b)。此外,关于将有机硼化合物直接用作碳自由基的电氧化C-H官能化反应也尚未实现。在此,南开大学汪清民教授课题组报道了一种温和的电化学氧化策略,使用烷基硼酸和酯以及三氟硼酸烷基酯作为烷基化剂,实现了喹喔啉-2(1H)-酮的C-H烷基化反应(Scheme 1c)。
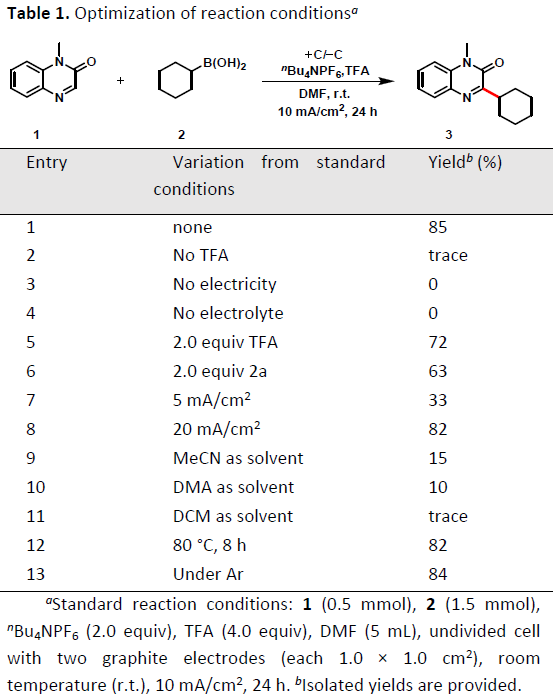
首先,作者以1-甲基喹喔啉-2(1H)-酮1和环己基硼酸2作为模型底物,进行了相关反应条件的筛选(Table 1)。反应的最佳条件为:以石墨板作为电极,DMF作为溶剂,nBu4NPF6(2.0当量)作为电解质,三氟乙酸(TFA,4.0当量)作为添加剂,电流密度为10 mA /cm2,即可获得85%收率的烷基化产物3。
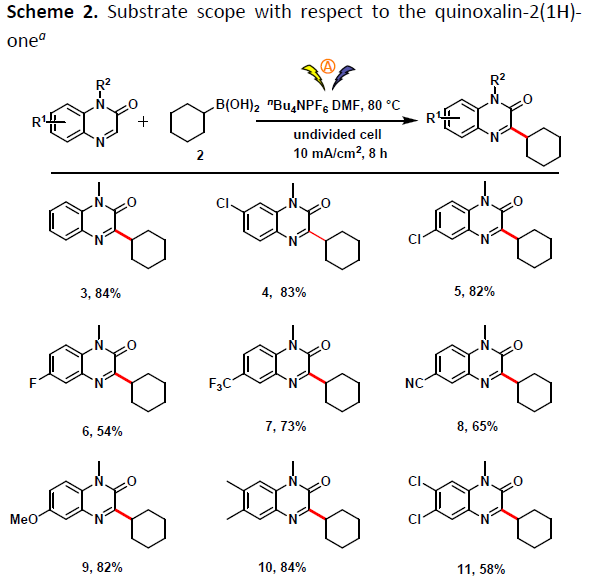
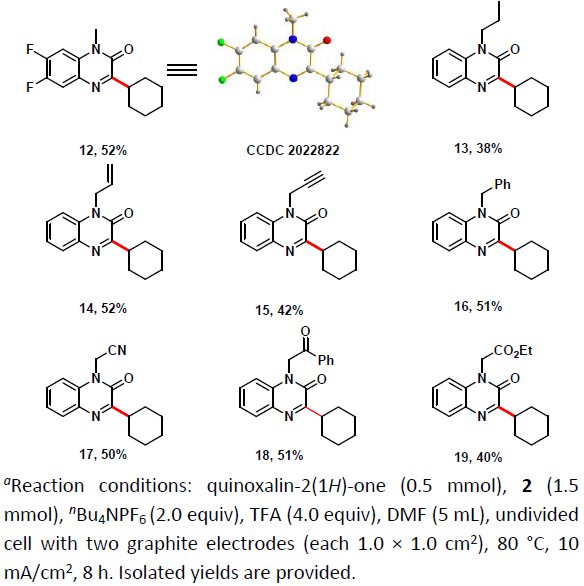
在获得上述最佳反应条件后,作者开始对喹喔啉酮底物1进行了扩展(Scheme 2)。反应结果表明,芳环上具有各种取代基(如甲基、氯、氟、三氟甲基、氰基、甲氧基等)的底物均与2平稳反应,以中等至良好的收率获得相应的产物4–12。同时,各种氮取代的底物(丙基、烯基、炔丙基、苄基等)也可与2顺利反应,获得相应的产物13–19。
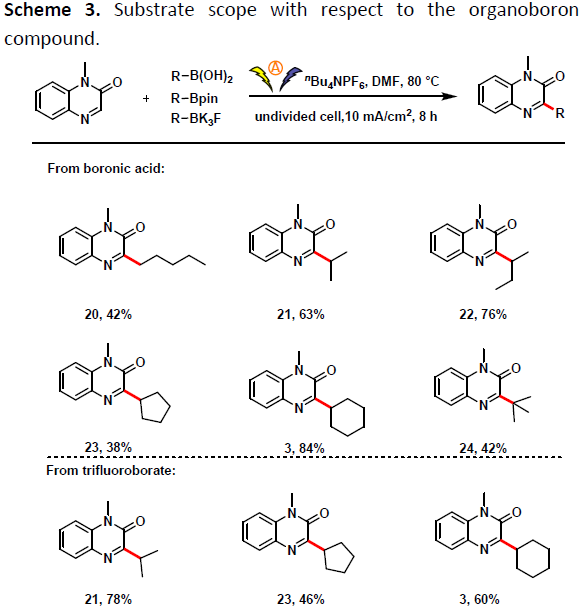
随后,作者对有机硼化合物的范围进行了扩展(Scheme 3)。反应结果表明,一系列无环和环状的伯、仲和叔烷基硼酸均为合适底物(3,20–24)。同时,环状仲和叔有机三氟硼酸酯也可用于反应中(3、21、23、24)。此外,环状和叔硼酸酯也与体系兼容(3、24)。
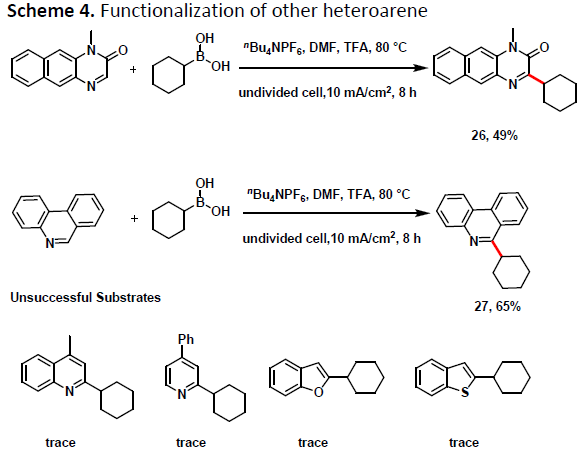
杂芳基骨架广泛存在于天然产物、小分子药物、有机材料和金属催化剂的配体中,此类结构的构建极具价值。在上述标准条件下,具有杂芳基骨架的苯并喹喔啉酮(26)和菲啶(27)均为合适的底物,从而进一步证明了该反应在药物后期衍生化中的价值(Scheme 4)。
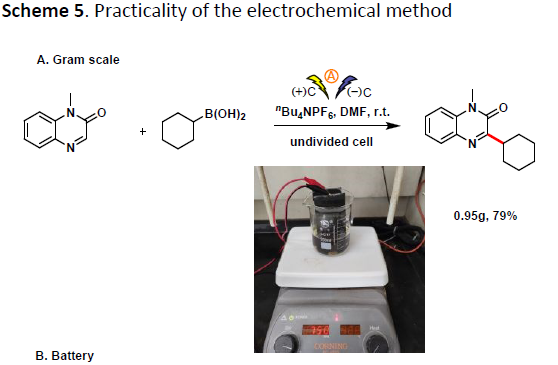
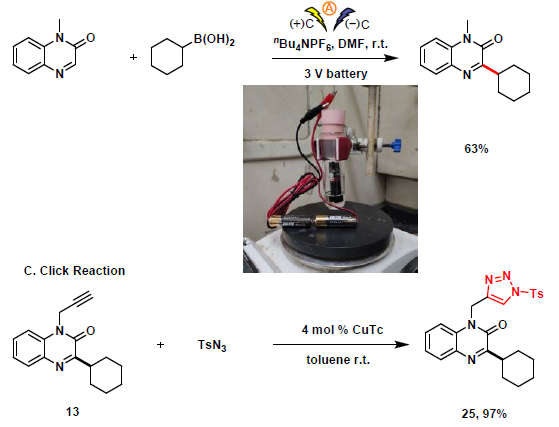
随后,为了进一步证明反应的实用性,作者进行了克级反应,在标准条件下,同样获得预期79%收率的产物3(Scheme 5)。值得注意的是,该反应可以使用电池作为电源,从而避免复杂的直流电源设备。此外,通过烷基化产物13的点击反应,可将炔烃转化为三唑骨架(25,产率为97%)。
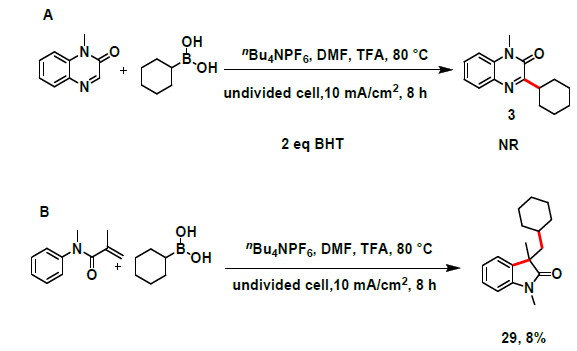
为了进一步了解反应的机理,作者进行了相关的对照实验(Scheme 6)。首先,在标准条件下,加入自由基抑制剂BHT后,反应被抑制,从而表明反应涉及自由基的参与。其次,使用N-苯基甲基丙烯酰胺与硼酸2在标准条件下反应时,获得产物29,收率为8%,从而表明反应形成了烷基自由基。
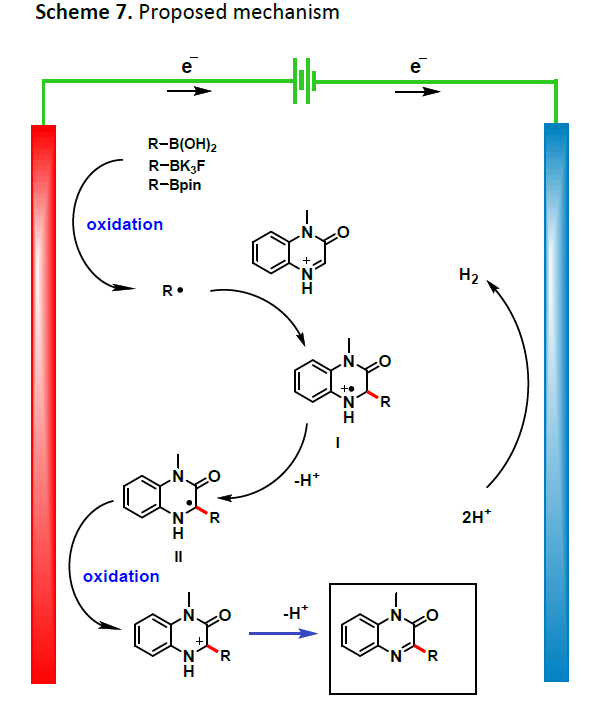
根据上述的实验,作者提出了一种可能的反应机理(Scheme 7)。首先,硼化合物在阳极经单电子氧化生成一个烷基自由基,再与质子化的杂芳烃反应生成自由基阳离子I。随后,自由基阳离子I失去质子,生成碳自由基中间体II。最后,II在阳极进行单电子氧化从而获得最终产物。
总结
南开大学汪清民教授课题组报道了一种喹喔啉-2(1H)-酮与有机硼化合物的电氧化C-H烷基化反应。值得注意的是,通过电化学氧化方法,可将有机硼酸、三氟硼酸酯,甚至硼酸酯直接转化为烷基自由基,无需使用金属催化剂、氧化剂或光氧化还原试剂等。
参考文献
[1] G. X. Li, C. A. Morales-Rivera, Y. Wang, F. Gao, G. He, P. Liu, G. Chen, Chem. Sci. 2016, 7, 6407-6412. [2] F. Lima, U. K. Sharma, L. Grunenberg, D. Saha, S. Johannsen, J. Sedelmeier, E. V. Van der Eycken, S. V. Ley, Angew. Chem., Int. Ed. 2017, 56, 15136-15140. [3] H. Yan, Z. W. Hou, H. C. Xu, Angew. Chem., Int. Ed. 2019, 58, 4592-4595. [4] Y. Yuan, Y. Zheng, B. Xu, J. Liao, F. Bu, S. Wang, J.-G. Hu, A. Lei, ACS Catal. 2020, 10, 6676-6681.
















No comments yet.