概要
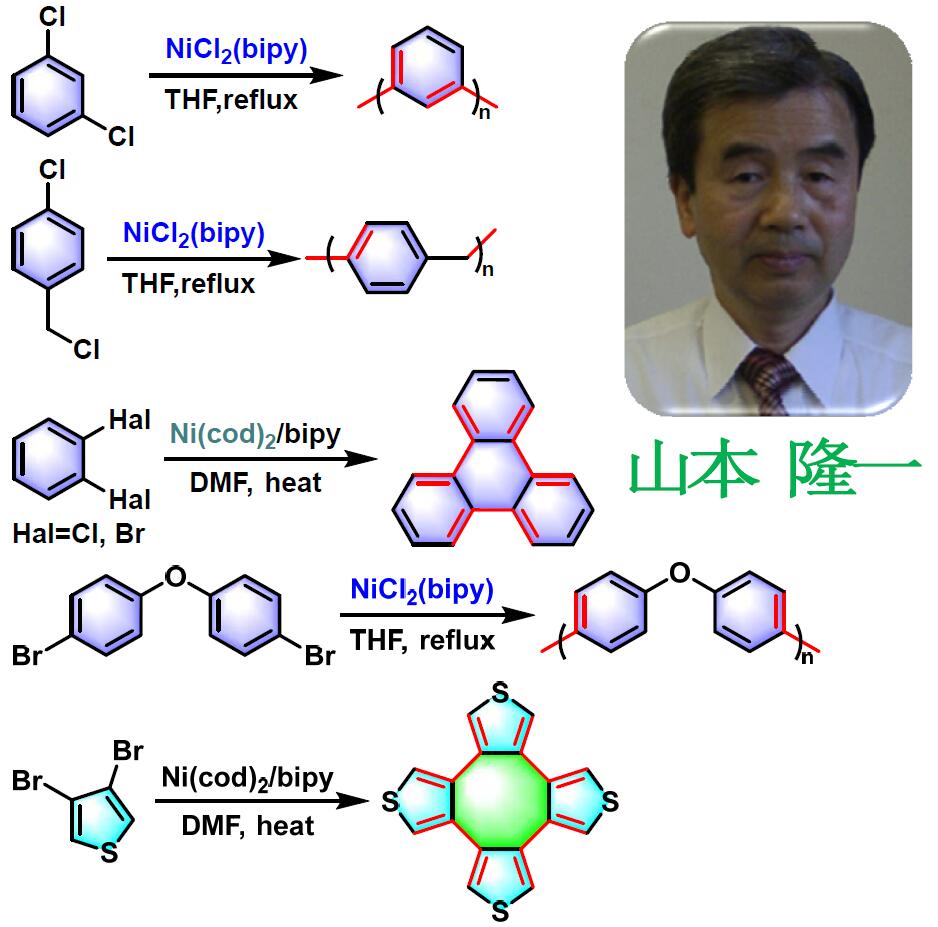
Yamamoto偶联 (Yamamoto coupling)又称为Yamamoto聚合 (Yamamoto polymerization),是过渡金属试剂 (如PdCl2(bipy), NiCl2(bipy), Ni (cod)2,NiBr2(PPh3)2, NiCl2, CoCl2, FeCl2等,其中NiCl2(bipy)与Ni (cod)2最为常用)促进的二卤代芳烃与多卤代芳烃通过去卤化反应而进行偶联缩聚[1]或脱卤C-C偶联 (dehalogenative carbon-carbon coupling reactions)[2]过程,获得聚芳烃类聚合物[1]及环低聚 (环三聚最为常见)产物[2]的反应。该反应在1978年由日本东京工业大学资源化学研究所(東京工業大学資源化学研究所,Research Laboratory of Resources Utilization, Tokyo Institute of Technology)的山本隆一 (山本 隆一,Yamamoto Takakazu)研究室首次报道[1]-[2]。
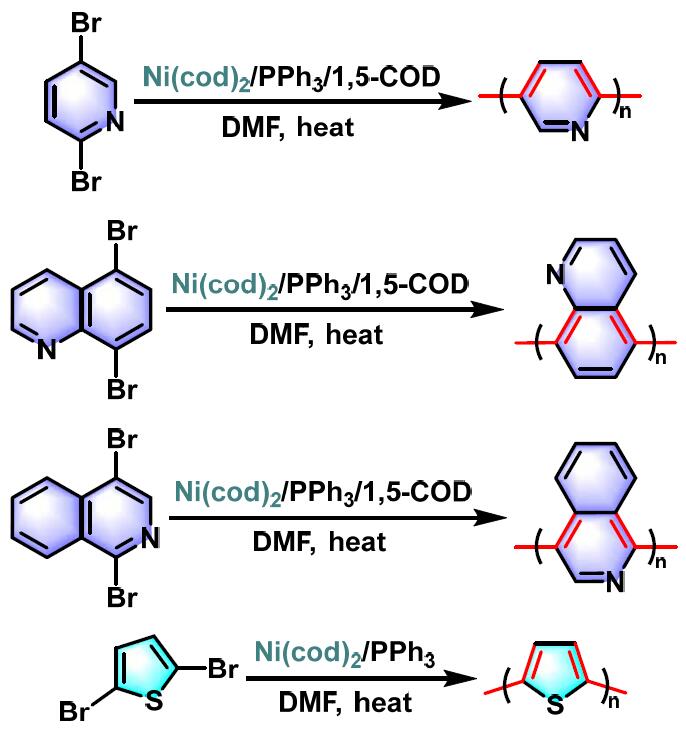
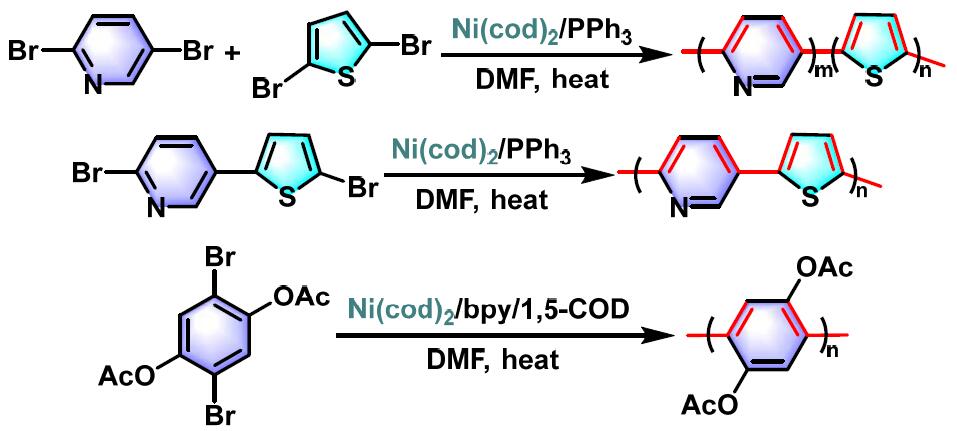
之后,Yamamoto将上述反应条件进行了深入研究,并成功应用于聚吡啶[3]-[4]、聚啉[5]与聚异喹啉[5]、聚噻吩[6]、吡啶-硒吩共聚物[7]、聚氢醌[8]、聚对苯醌[8]与聚对二乙酰氧基苯单元[8]、光学活性[9]及氧化还原活性聚合物[9]的合成。
目前,该反应已经广泛应用于具有较高聚合度与热稳定性的各类π-共轭聚合物 (π-conjugated polymer) [1]-[10]、共轭微孔聚合物[11] (Conjugated Microporous Polymer, CMP)及全芳香梯形聚合物[12]等的合成。
基本文献
- [1] T. Yamamoto, Y. Hayashi, A. Yamamoto, Bull. Chem. Soc. Jpn. 1978, 51, 2091. doi: 10.1246/bcsj.51.2091.
- [2] Z. Zhou, T. Yamamoto, J. Organomet. Chem. 1991, 414, 119. doi: 10.1016/0022-328X(91)83247-2.
- [3] T. Yamamoto,T. Ito, K. Kubota, Chem.Lett. 1988, 17, 153. doi: 10.1246/cl.1988.153.
- [4] T. Maruyama, K. Kubota, T. Yamamoto, Macromolecules 1993, 26, 4055. doi: 10.1021/ma00067a052.
- [5] T. Kanbara, N. Saito, T. Yamamoto, K. Kubota, Macromolecules 1991, 24, 5883.
- doi: 10.1021/ma00021a027.
- [6] T. Yamamoto, A. Morita, Y. Miyazaki, T. Maruyama, H. Wakayama, Z. Zhou, Y.
- Nakamura, T. Kanabara, Macromolecules 1992, 25, 1214. doi: 10.1021/ma00030a003
- [7] T. Yamamoto, N. Hayashida, React. Funct. Polym. 1998, 37, 1. doi: 10.1016/S1381-5148(97)00140-5.
- [8] T. Yamamoto, T. Kimura, K. Shiraishi, Macromolecules 1999, 32, 8886. doi: 10.1021/ma9907946.
- [9] U. Scherf, E. J. W. List, Adv. Mater. 2002, 14, 477. doi: 10.1002/1521-4095(20020404)14:7<477::AID-ADMA477>3.0.CO;2-9.
- [10] T. Yamamoto, J. Synth. Org. Chem. Jpn.1995, 53, 999. doi: 10.5059/yukigoseikyokaishi.53.999.
- [11] J. Schmidt, M. Werner, A. Thomas, Macromolecules 2009, 42, 4426. doi: 10.1021/ma9005473.
- [12] K. Chmil, U. Scherf, Makromol. Chem. Rapid Commun. 1993, 14, 217. doi: 10.1002/marc.1993.030140401.
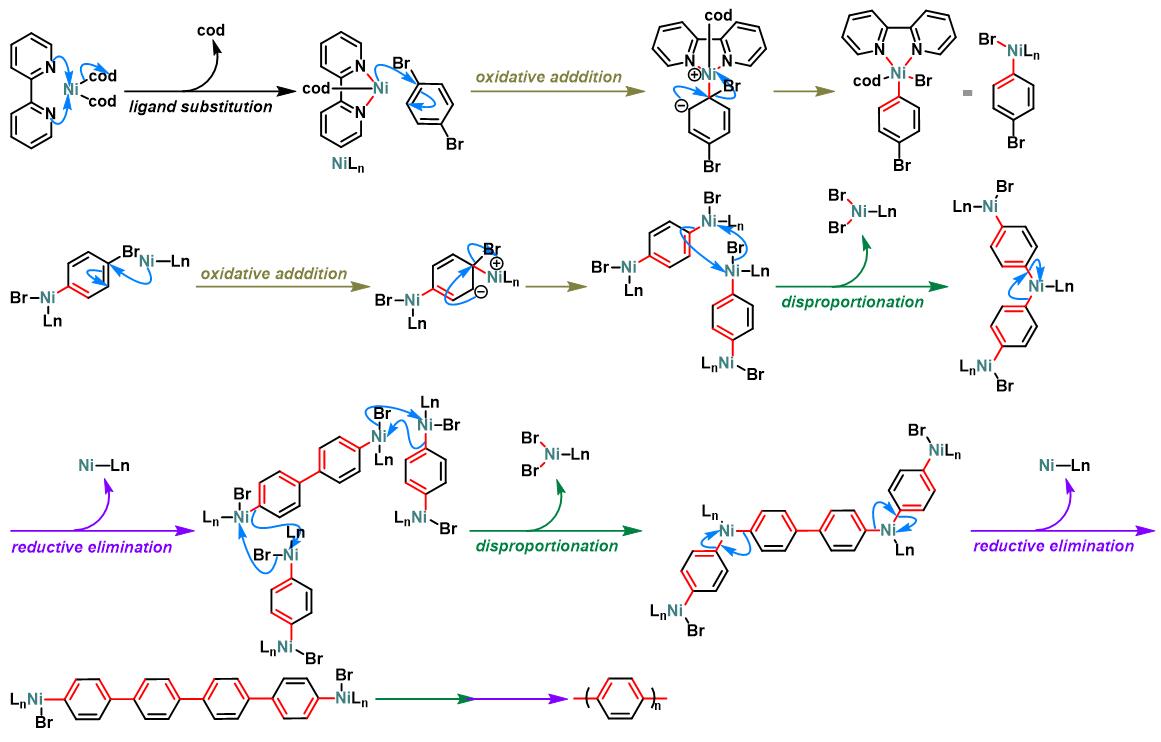
反应机理
低聚反应
聚合反应
参考文献
- [1] T. Yamamoto, S. Wakabayashi, K. Osakada, J. Organomet. Chem. 1992, 428, 223. doi: 10.1016/0022-328X(92)83232-7.
- [2] T. Yamamoto, T. Koizumi, Polymer, 2007, 48, 5449. doi: 10.1016/j.polymer.2007.07.051.
- [3] T. Kohara, T. Yamamoto, A. Yamamoto, J. Organomet. Chem. 1980, 192, 265. doi: 10.1016/S0022-328X(00)94431-0.
- [4] S. Komiya, Y. Abe, A. Yamamoto, T. Yamamoto, Organometallics 1983, 2, 1466. doi: 10.1021/om50004a042.
- [5] K. Tatsumi, A. Nakamura, S. Komiya, T. Yamamoto, A. Yamamoto, J. Am. Chem.Soc. 1984, 106, 8181. doi: 10.1021/ja00338a029
- [6] D. R. Fahey, J. E. Mahan, J. Am. Chem.Soc. 1977, 99, 2501. doi: 10.1021/ja00450a017.
- [7] D. R. Fahey. J. Am. Chem. Soc. 1970, 92, 402. doi: 10.1021/ja00705a612
- [8] F. Ozawa, T. Hidaka, T. Yamamoto, A. Yamamoto, J. Organomet. Chem. 1987, 330, 253. 10.1016/0022-328X(87)80292-9.
反应实例
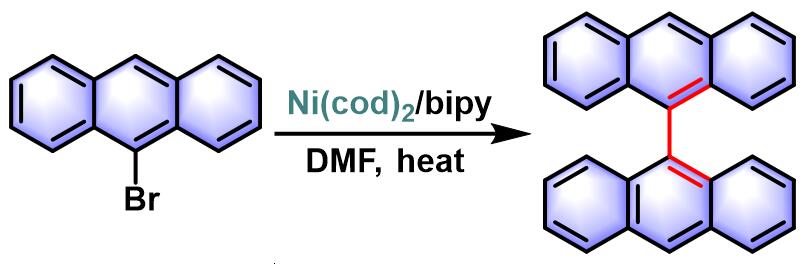
联芳的合成[1]
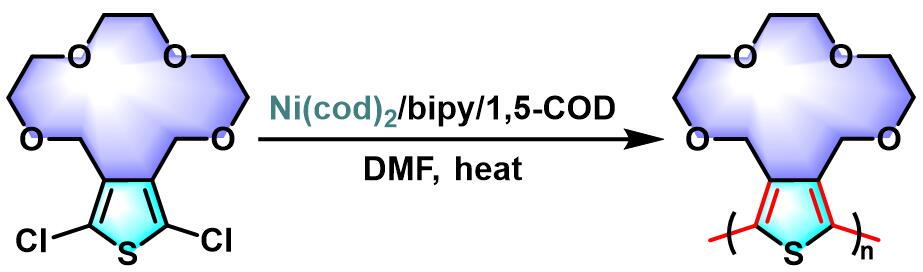
聚噻吩的合成[2]
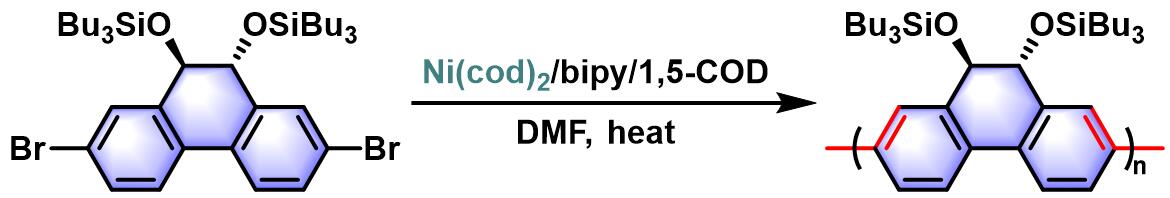
手性聚合物的合成[3]-[4]
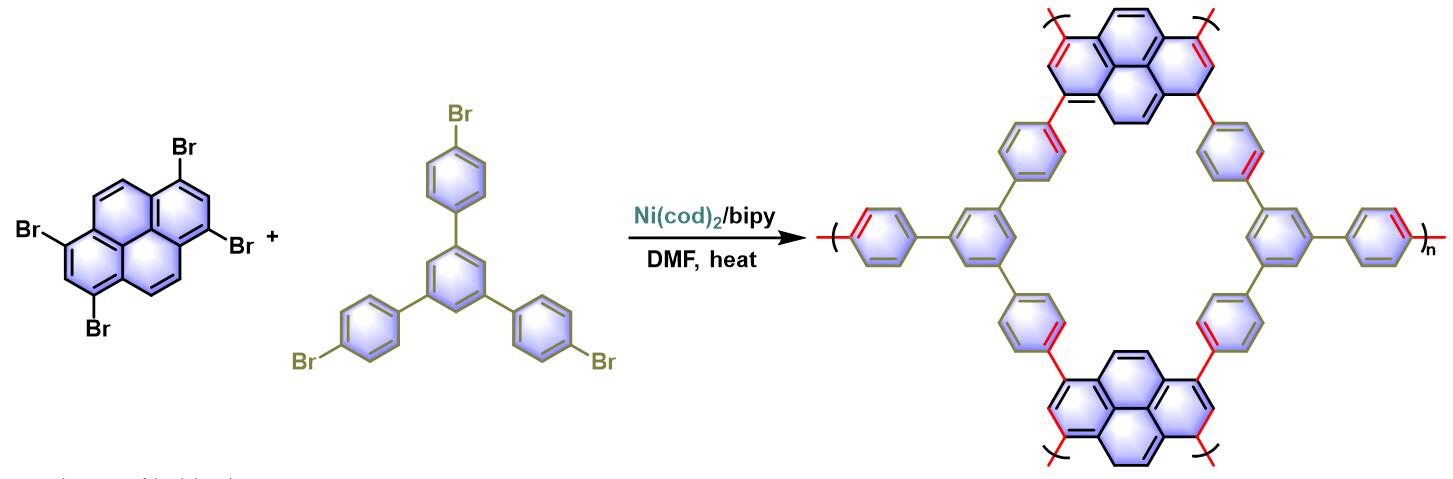
多孔共价有机聚合物 (porous covalent organic polymers, COPs)的合成[5]
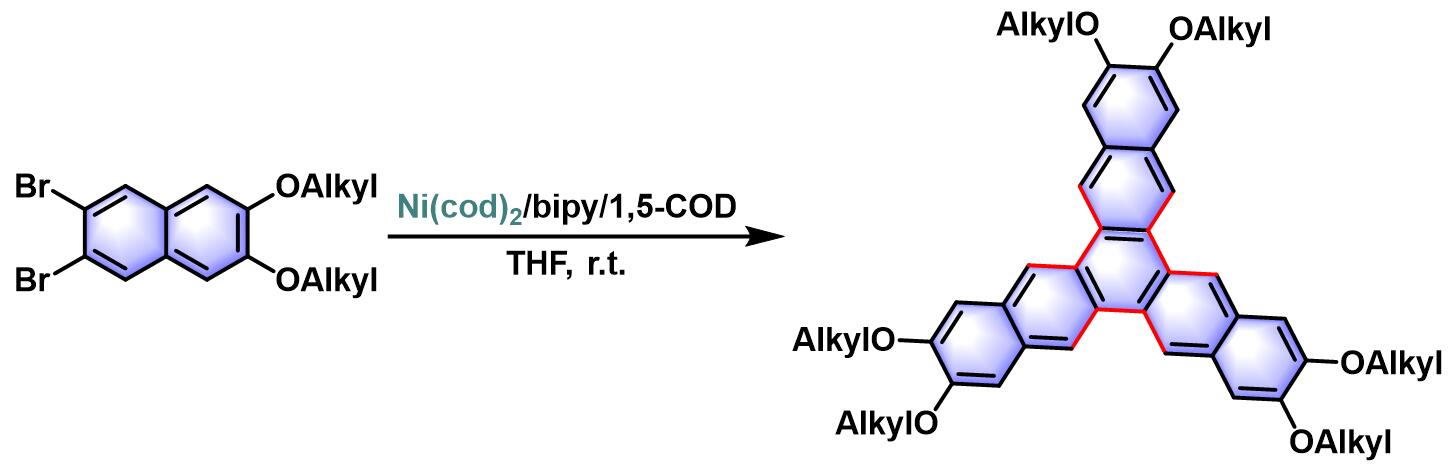
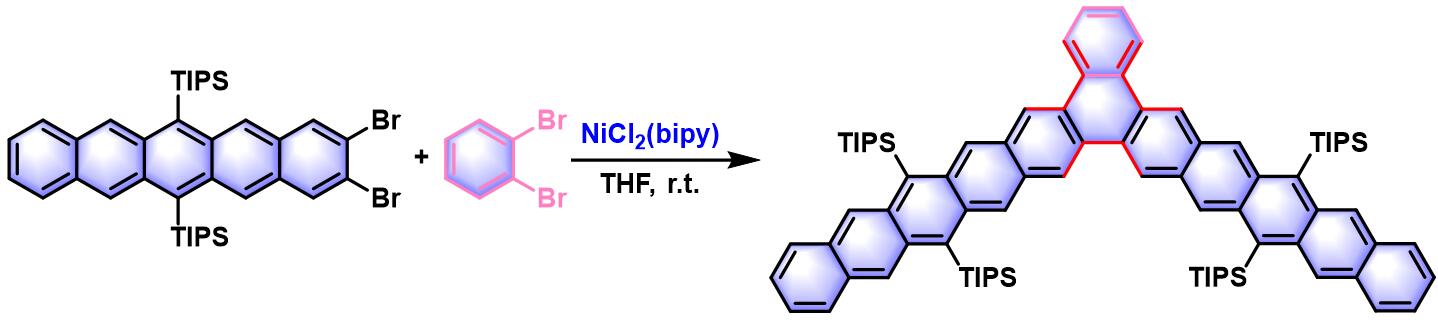
取代三萘的合成[6]
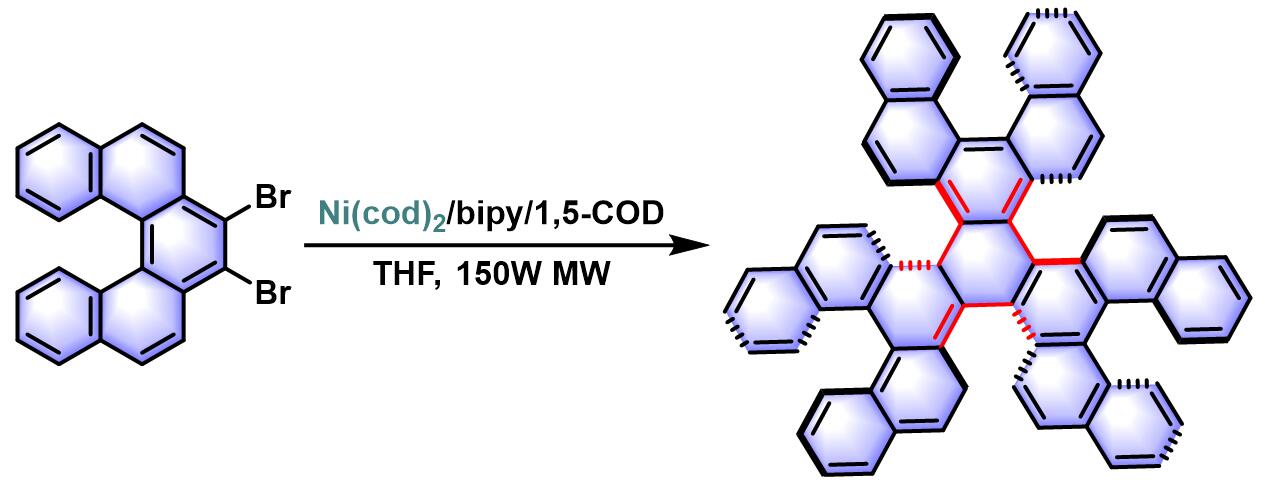
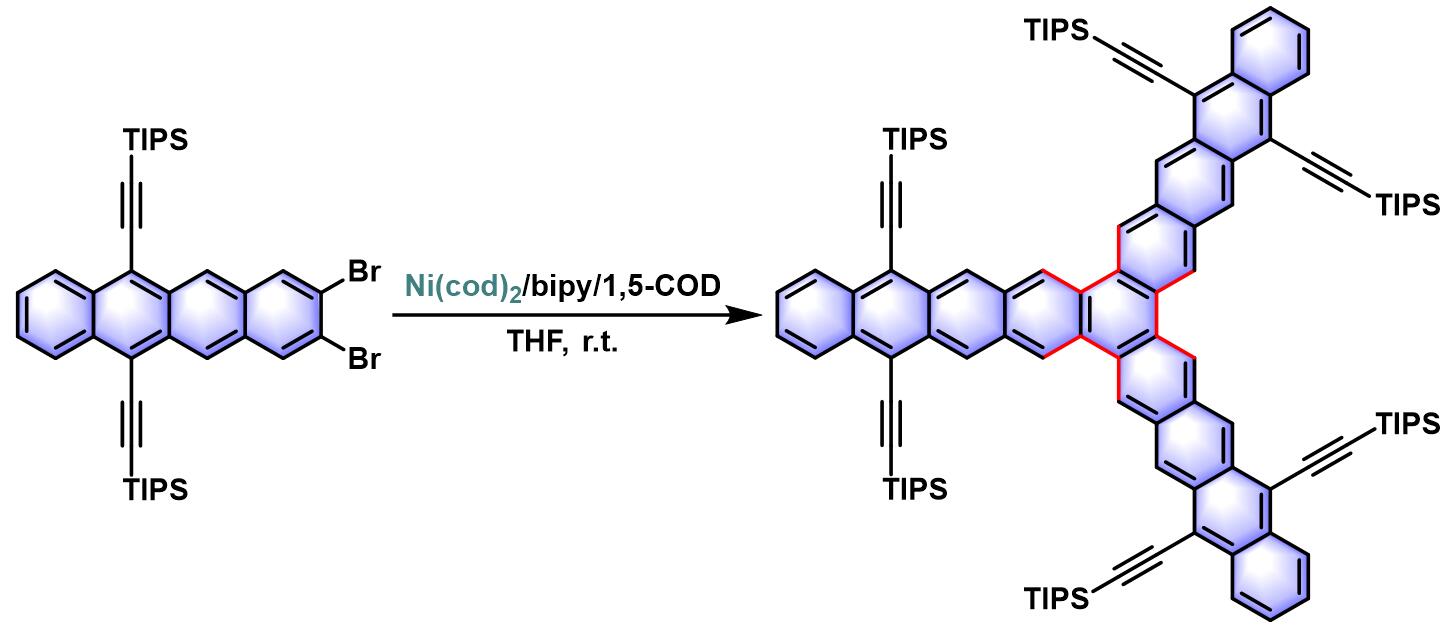
[5]螺烯的合成[7]炔基取代Starphenes的合成[8]
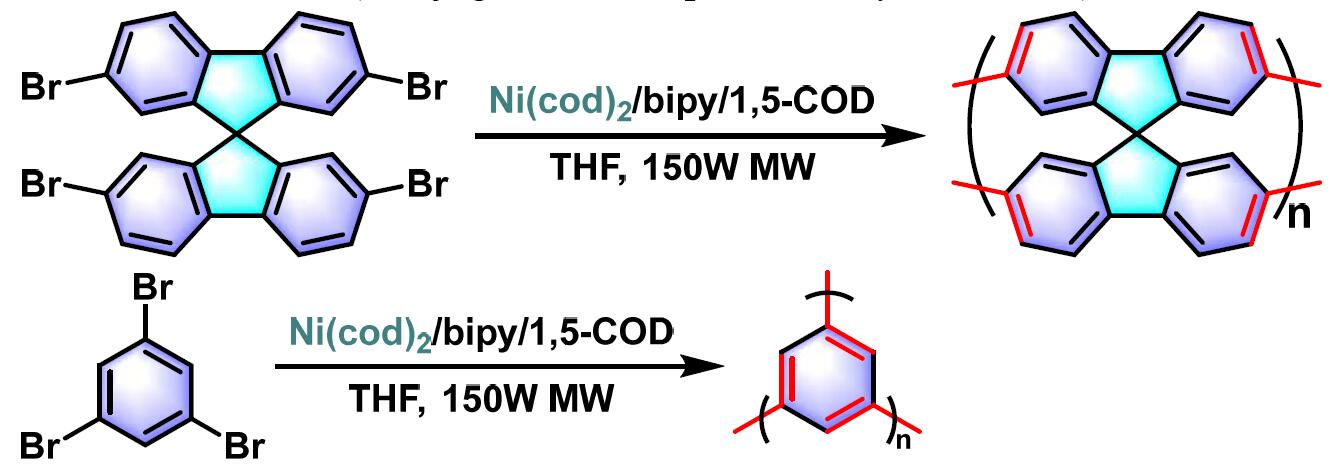
共轭微孔聚合物 (Conjugated Microporous Polymer, CMP)的合成[9]
Benzophenes的合成[10]
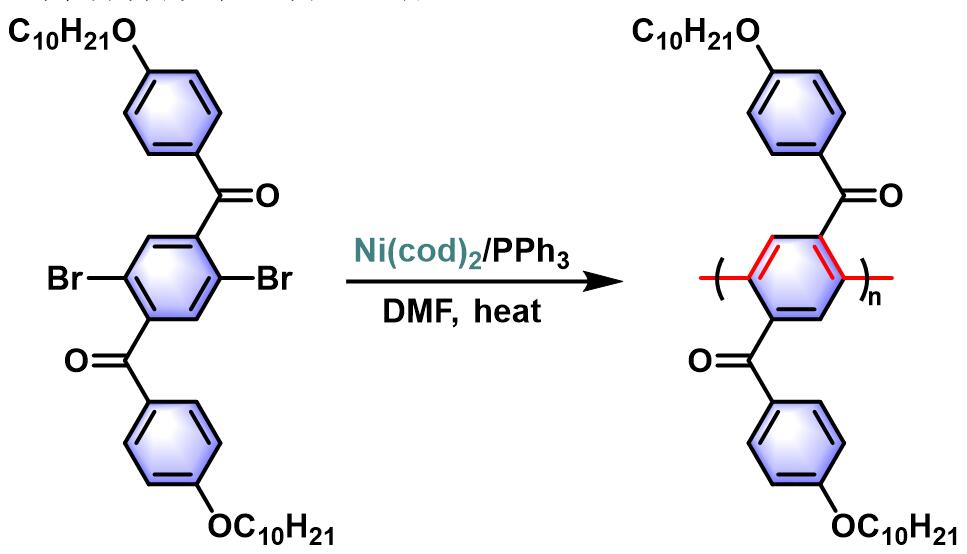
全芳香梯形聚合物的合成[11]
实验步骤
聚合反应
在手套箱内,向管式反应瓶 (tubular reaction vessel)中加入Ni(COD)2 (1.45 eq.)、2,2′-联吡啶(1.93 eq.)、芳基卤 (1 eq.)、cis-1,5-环辛二烯 (5.72 eq.)及无水THF (维持底物浓度为0.15 M)。将反应瓶在手套箱内密封后,在微波辐射下加热 (温度为120°C) 12 min。减压除去溶剂后,将残余物溶于煮沸的CHCl3中,并通过短硅胶柱过滤,除去难溶性盐。 粗产物通过三次连续研磨粉碎 (successive trituration)的方式进行纯化,固体通过离心机分离进行回收: 第一次在EtOH中回流45 min,第二次在乙腈中,室温下超声30 min,最后在甲苯/乙醇中回流45 min,获得最终目标产物。
低聚反应
室温下,向Ni(cod)2 (1.3 eq.)的DMF溶液 (浓度为0.43 M)中加入1,5-环辛二烯 (1.6 eq.)与2,2′-联吡啶 (1.3 eq.). 随后,滴加芳基卤 (1 eq.)的DMF溶液 (浓度为0.52 M)。将上述反应混合物在70oC下搅拌22h后,加入适量水及乙醚进行萃取。将乙醚相采用无水硫酸镁进行干燥,过滤。减压除去溶剂后,将残余物采用硅胶柱色谱分离纯化,再用乙醚进行重结晶,获得环三聚产物。
参考文献
- [1] Z. Zhou, T. Yamamoto, J. Organomet. Chem. 1991, 414, 119. doi: 10.1016/0022-328X(91)83247-2.
- [2] T. Yamamoto, M. Omote, Y. Miyazaki, A. Kashiwazaki, B. Lee, T. Kanbara, K. Osakada, T. Inoue, K. Kubota, Macromolecules 1997, 30, 7158. doi: 10.1021/ma9708104.
- [3] T. Yamamoto, T. Asao, H. Fukumoto, Polymer, 2004, 45, 8085. doi: 10.1016/j.polymer.2004.09.060.
- [4] T. Ijima, T. Yamamoto, Chem. Lett., 2005, 1672. doi: 10.1246/cl.2005.1672.
- [5] L. Guo, D. Cao, J. Mater. Chem. C, 2015, 3, 8490. doi: 10.1039/C5TC01649E.
- [6] E. C. Rüdiger, F. Rominger, L. Steuer, U. H. F. Bunz, J. Org. Chem. 2016, 81, 193. doi: 10.1021/acs.joc.5b02481.
- [7] V. Berezhnaia, M. Roy, N. Vanthuyne, M. Villa, J.-V. Naubron, J. Rodriguez, Y. Coquerel, M. Gingras, J. Am. Chem. Soc. 2017, 139, 18508. doi: 10.1021/jacs.7b07622.
- [8] E. C. Rüdiger, M. Porz, M. Schaffroth, F. Rominger, U. H. F. Bunz, Chem. Eur. J. 2014, 20, 12725. doi: 10.1002/chem.201403697.
- [9] J. Schmidt, M. Werner, A. Thomas, Macromolecules 2009, 42, 4426. doi: 10.1021/ma9005473.
- [10] E. C. Rüdiger, S. Koser, F. Rominger, J. Freudenberg, U. H. F. Bunz, Chem.Eur. J. 2018, 24, 9919 , doi: 10.1002/chem.201801459.
- [11] K. Chmil, U. Scherf, Makromol. Chem. Rapid Commun. 1993, 14, 217. doi: 10.1002/marc.1993.030140401.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!


















No comments yet.