本文作者:竹悠
导言
作者使用膦-喹啉铑催化剂,实现了高效的炔烯的氢胺化环合反应。反应的过程可能经历了胺基卡宾配体催化形成新的碳碳键。
正文
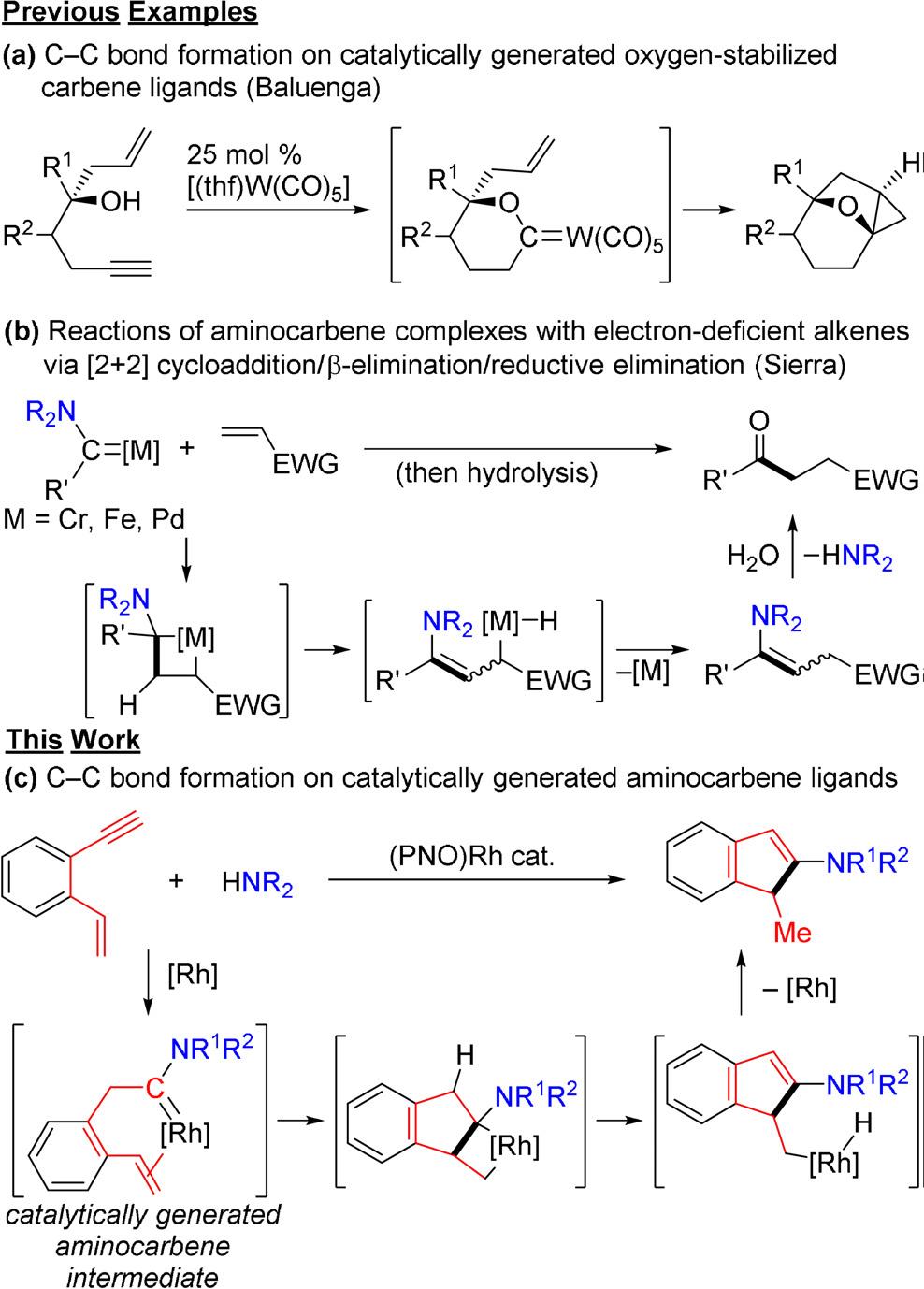
杂原子稳定的过渡态金属卡宾络合物,是有机合成中的重要合成砌块。在大多数应用卡宾络合物的反应中,这些络合物都是提前制备,并使用化学计量的与底物反应,而催化量的反应极少报道过。2005年,Barluenga课题组报道了烷氧基卡宾络合物催化环异构化反应/环丙烷化反应,生成三环化合物。这也是仅有的催化碳碳键,如图1a所示
最近,日本Keio University的Fumitoshi Kakiuchi报道了膦-喹啉铑络合物[简写为(PNO)Rh, phosphine-quinolinolato rhodium]作为催化剂,实现了端基炔烃的反马氏规则的氢胺化反应,其中胺基卡宾是反应中的重要中间体。因此,作者推测原位生成的胺基卡宾络合物可以催化碳碳键的形成。
此论文发表在顶级期刊Angewandte Chemie International Edition上,并被选为封面文章。
Carbon–Carbon Bond Formation via Catalytically Generated Aminocarbene Complexes: Rhodium-Catalyzed Hydroaminative Cyclization of Enynes with Secondary Amines
Shotaro Takano, Ryosuke Shiomi, Yoshihiko Morimoto, Takuya Kochi and Fumitoshi Kakiuchi
Angew. Chem. Int. Ed., 2020, 59(29), 11754-11757. DOI: 10.1002/anie.202002710
胺基卡宾络合物可以催化多种反应,如与缺电子的烯烃反应后水解生成金属杂环丁烷,然后经β-H消除和还原消除生成产物酮,如图1b所示,但是催化原位生成胺基卡宾还未实现。
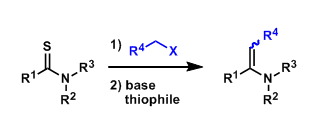
本文报道了炔烃和二级胺在(PNO)Rh催化下,发生氢胺化环合反应,生成环状的烯胺。如2-乙烯基苯乙炔衍生物和二级胺反应,以良好的收率生成2-胺基卡宾,再精力[2+2]环加成和β-H消除过程得到产物。这是首例报氨基卡宾催化生成新的碳碳键的报道,如图1c所示。
图1 杂原子稳定的卡宾络合物发生的反应
反应优化
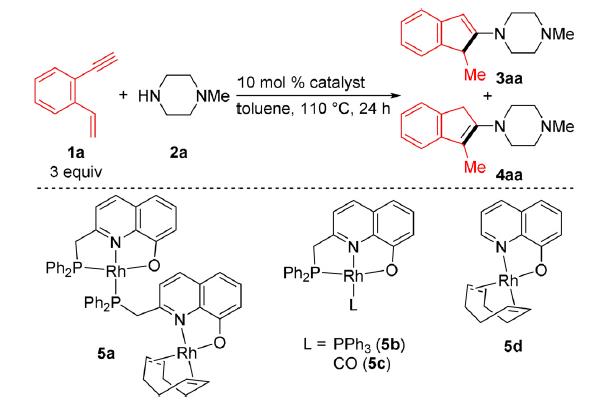
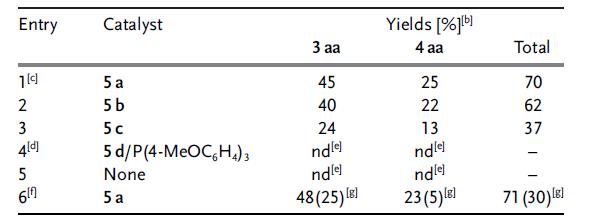
底物2-乙烯基苯乙炔1a和1-甲基哌嗪2a在5%双核催化剂(PNO)Rh 5a作用下,110 ℃甲苯为溶剂,得到1-甲基-2-(N-哌嗪)茚3aa (45%)和3-甲基-2-(N-哌嗪)茚 4aa (25%),如表1中entry 1。没有铑催化剂时,也不会生成环合产物(entry 5)。继续优化反应,催化剂5b的效果和5a类似,但5c的效果较差。结合8-喹啉铑络合物5d和膦P(4-MeOC6H4)3,可以催化端基炔烃的反马氏氢胺化反应(entry 4)。没有铑催化剂时,不会生成环合产物(entry 5)。如果使用5 mol%的催化剂5a,反应在2小时内结束。虽然产物在空气中不稳定,通过氮气保护下柱层析,两个产物的分离收率为30%。
表 1 筛选8-异喹啉铑催化剂催化底物1a和2a的反应
底物拓展
作者继续考察了底物1a和其它二级胺的氢胺化环合反应,如表2所示。六元环的哌啶、吗啉收率较高 (entries 1-3);七元环的环己亚胺收率略低(entriey 4).;1,2,3,4-四氢异喹啉的收率较高(entry 5);其它非环状的胺(2g-2l)的收率为50-65%(entries 6-11);N-单取代的苯胺类没有环合产物(entries 12-13)。
表2 底物1a和其他多种胺的氢胺化环合反应
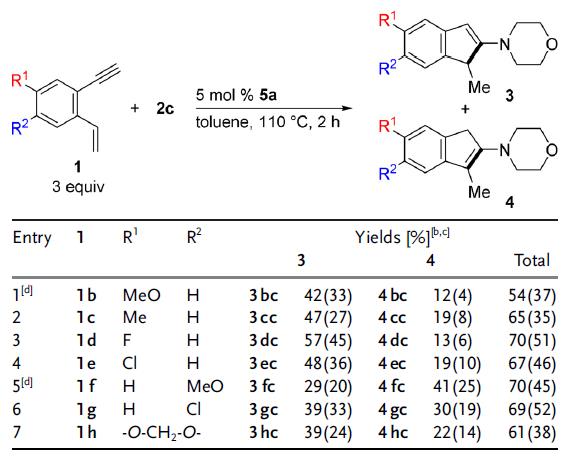
在炔烃底物1和吗啉2c的反应如表3所示,乙烯基的对位有取代基时的底物(1b-1e),反应可以进行(entries 1-4),甲氧基取代1b时反应时间长24h(entry 1),其对位它衍生物(1f-1g)也有类似的倾向;环醚衍生物1h的总收率为61%(entry 7)。丙烯基取代乙烯基底物收率很低,烷基取代乙烯基没有产物。
表3 多种底物1和二级胺2c的氢胺化环合反应
机理研究
以氘代甲苯为溶剂,通过核磁1H NMR监控反应:1a和2b。3当量的1a和2b反应时,20 min得到3ab(9%)和4ab(2%),反应2 h后4ab的比例逐渐上升至2:1,说明两个产物之间存在可逆的异构化。磷谱核磁52.3 ppm说明存在(PNO)Rh胺基卡宾络合物。
作者推测反应机理为:
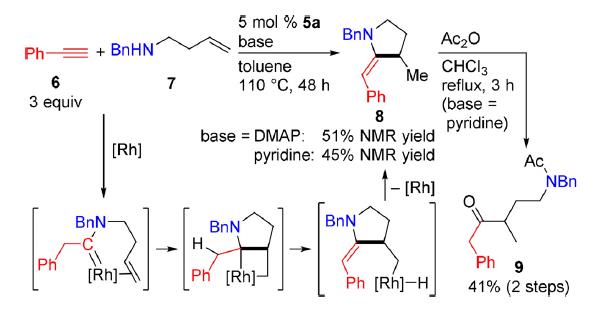
首先,乙烯基苯乙炔1和铑催化剂(PNO)Rh反应生成联烯中间体,然后和二级胺反应生成胺基卡宾络合物,两个烯烃部分与铑配位后,发生环加成反应生成含铑的环丁烷结构。接着β-H消除生成含Rh-H的结构,还原消除后得到环烯胺产。并且,根据β-H消除时氢的来源不同,生成了3和4,如图2所示。
图2. 铑催化剂(PNO)Rh催化氢胺化环化反应的反应机理
将炔烃和烯烃两个官能团从一个化合物上分开,也能应用这个合成方法。如端基炔烃的苯乙炔6和N-苄基-3-丁烯-1-胺7,在碱的作用下生成基于吡咯烷结构的环状烯胺8,酸酐处理为酰胺9,如Scheme 1所示。
Scheme 1 端基炔烃与二级胺的反应
总结
作者将铑催化剂应用于烯烃和二级胺的氢胺化环合反应,首次实现了原位生成胺基卡宾催化碳碳键生成。反应机理可能通过了胺基卡宾络合物的[2+2]环加成-β-H消除-还原消除过程。这将会促进杂原子稳定的过渡态金属卡宾络合物催化剂在有机合成中的应用。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!























No comments yet.