本文投稿作者:孙苏赟
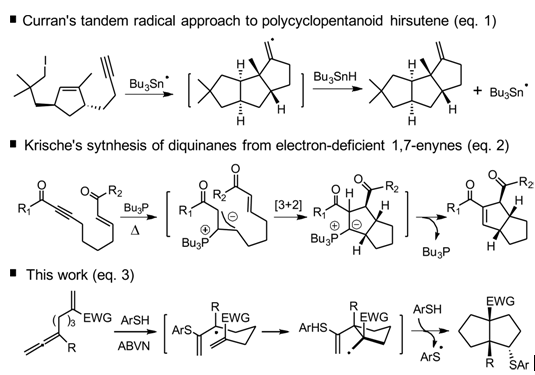
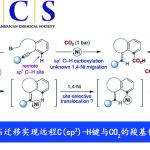
在天然物中,具有多个连续手性中心的多环天然产物非常多(Fig.1),这些结构常常是合成工作中的难点。在此前,Curran课题组曾报道过一种锡烷引发的自由基串联环化反应生成三个并环化合物(ref.1),其过程是引发剂nBu3SnH将炔转化成烯烃自由基,再经过两次成环得到具有四个连续手性中心的5,5,5-三环结构骨架(Fig.2-eq.1)。此外Krische课题组在2005年也开发过一种分子内[3+2]环加成反应(ref.2)成形成5,5-二并环骨架(Fig.2-eq.2)。
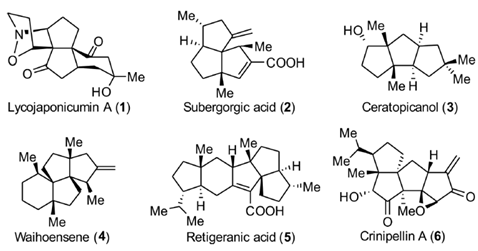
Figure1
Figure多环萜类化合物的合成
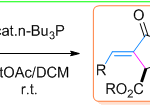
专注于萜类天然产物全合成的杨震教授不久前在OrganicLetter上报道了一篇(Org.Lett.,DOI:10.1021/acs.orglett.7b01733),报道了一种无金属参与的联烯为反应底物生成具有连续四个手性中心的5,5-二并环的不对称反应。前人开发的反应是用Br,PhS或是RSO2自由基引发反应的,这里考虑使用芳基硫酚引发反应,于是提出了设计的反应机理:
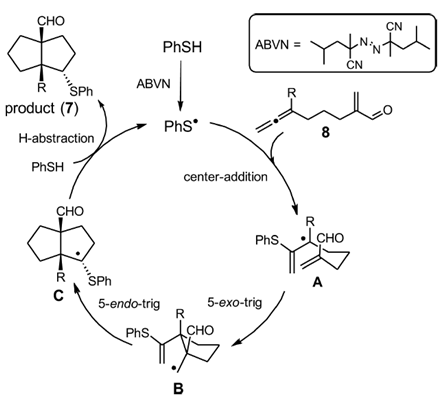
Figure3提出的可能的反应机理
反应过程中,ABVN脱去N2生成烷基自由基,自由基进攻硫酚生成硫自由基,硫自由基会倾向于联烯中多取代的碳原子生成中间体A,A中自由基进攻啊α,β-不饱键发生5-exo-trig环化得到另一自由基中间体B,B再成环得到亲核的自由基中间体C,C得到一个质子环得到了产物7和生成ArS自由基。
为了优化反应条件,接下来进行了反应条件的筛选。影响反应主要有反应引发剂的种类和剂量、芳基硫酚的种类和剂量、反应溶剂和底物的取代基几种影响因素。
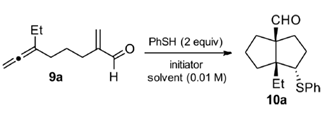
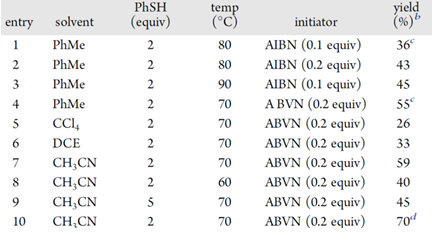
Table1反应条件的筛选
首先是引发反剂的筛选(Tbl.1),测试中的溶剂有甲苯,CCl4,DCE,CH3CN,同时改变引发剂的种类和剂量AIBN/ABVN(0.1/0.2equiv.)和硫酚PhSH的剂量(2/5equiv.),多次试验之后得到最优化反应条件:CH3CN为溶剂,0.2equiv.ABVN和2equiv.PhSH做自由基引发剂,此条件下产率可高达70%。
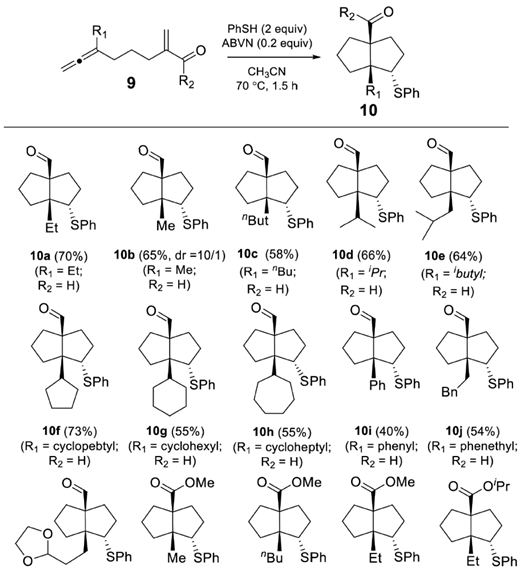
Scheme1底物取代基对联烯的[3+2]反应的影响
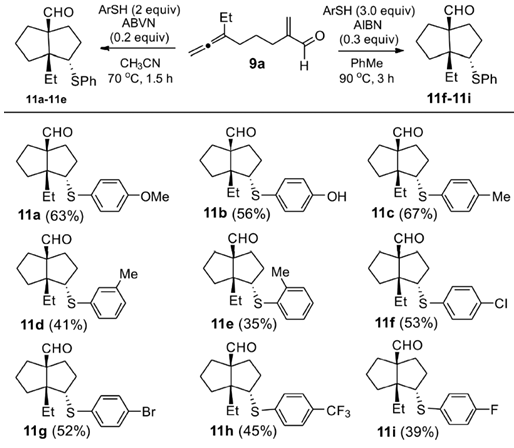
Scheme2芳基硫酚的电子效应对反应的影响
接下来是底物取代基和硫酚上取代基对反应的影响。
试验后发现,底物上R1对反应产率的影响不大,除个别底物(10i,R1=Ph)外,反应的产率均在50-70%之间,这一点在合成上是很具有潜在的利用价值的(Schm.1)。
而R2的影响,在此前有研究报道(ref.3),EDG会导致PhS-H键解离能增加而不利于反应,故EWG是有利于反应的,如Schm.2所示。并且在替换不同种类的硫酚后发现,对于相同的取代基,o-/m-二取代硫酚的产率不如p-二取代硫酚,并且取代基为EDG有利于反应产率的提高。
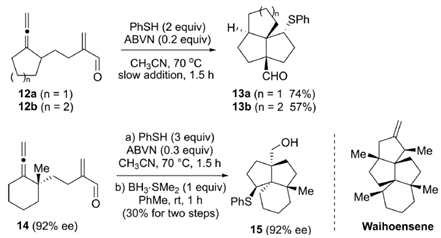
Scheme3三奎烷的合成
最后,这个反应被用于以上的反应(Schm.3),这表明如果反应底物环状是环状化合物,那么产物是可以得到多环化合物的,Schm.3中的12a/b和14就分别高产率的转化成了13a/b和15,其中15的ee值高达92%。这个反应在全合成中的应用现在正在杨震教授的课题组中展开(ref.4),我们期待精彩的全合成!
参考文献
- (a) J. Am. Chem. Soc. 1985, 107, 1448. DOI: 10.1021/ja00291a077 (b) Tetrahedron Lett. 1985, 26, 4991. DOI: 10.1016/S0040-4039(01)80834-0
- (a) Org. Lett. 2007, 9, 3069. DOI: 10.1021/ol071181d (b) J. Am. Chem. Soc. 2015, 137, 4587. DOI: 10.1021/jacs.5b01985
- (a)Acc. Chem. Res. 2004, 37, 334. DOI: 10.1021/ar010010k (b)J. Org. Chem. 1996, 61, 8312. DOI: 10.1021/jo961301n (c) J. Am. Chem. Soc. 1994, 116, 6605. DOI: 10.1021/ja00094a015
- Angew. Chem., Int. Ed. 2017, 56, 8254. DOI: 10.1002/anie.201704492
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!



















No comments yet.