接前期
首次合成碳纳米带–背后的故事(二)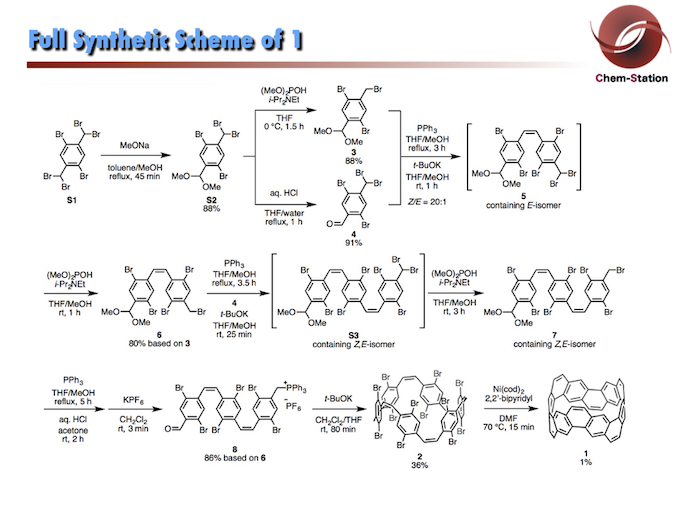 上一期我们介绍到了碳纳米带前体的具体合成,经过多步反应得到环状化合物2(碳纳米带的前体)。在这里要说一下,对于前体2的大量制备,在合成路线打通后,都是由Erato招收实验技术员们来合成的,这些重复性的工作都是从社会上招聘一些化学修士毕业生来完成的,这也是Erato课题组的特色,注重人才利用效率,更像公司里的模式,加上日本学生人数有限,如果是在国内的话,应该有很多实验室的小弟来帮忙合成吧!
上一期我们介绍到了碳纳米带前体的具体合成,经过多步反应得到环状化合物2(碳纳米带的前体)。在这里要说一下,对于前体2的大量制备,在合成路线打通后,都是由Erato招收实验技术员们来合成的,这些重复性的工作都是从社会上招聘一些化学修士毕业生来完成的,这也是Erato课题组的特色,注重人才利用效率,更像公司里的模式,加上日本学生人数有限,如果是在国内的话,应该有很多实验室的小弟来帮忙合成吧!
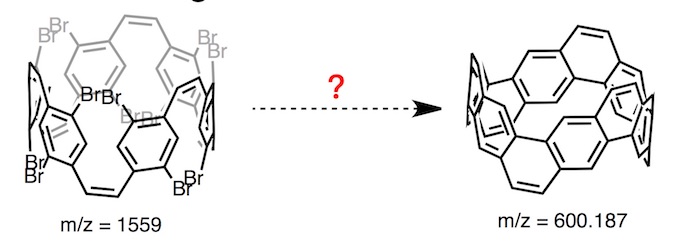
为了能得到碳纳米带1,Guillaume博士用前体2也尝试了一系列还原偶联条件,如:Na Naphthalenide, Rieke Mg, Stille-Kelly, Ullmann Coupling等反应,其他如高压汞灯照射和自由基条件也没办法获得很好地结果。最终锁定了Ni催化的Yamamoto偶联反应,筛选了膦配体,联吡啶配体等,也发现催化量的催化剂反应效力不够,通过MALDI对分子量检测,发现不能使全部的C-Br键转化成C-C键,最终通过提高反应温度,并加入12当量的Ni(cod)2/2,2′-联吡啶才得到1%的产物1。这样的少量化合物的分离定性,我真是不得不佩服Guillaume博士的精细手法了。
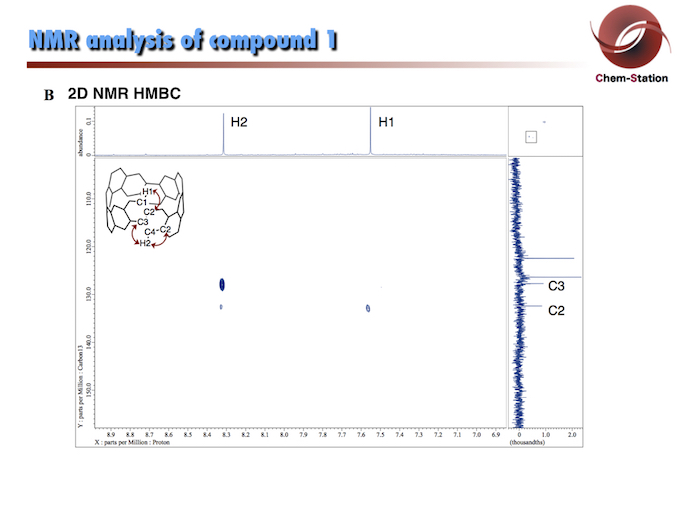
在归属化合物1的氢和碳时,只有两组H的峰分别在7.52和8.27(各12个H)这样高度对称的化合物,归属碳原子则借助了碳氢相关二维谱 (H2 和H1的归属参考了理论计算值,见论文SI)然后依次通过相邻C-H相关(HMQC)和远程C-H相关(HMBC)归属了C1,C4,C2, C3。

 当然化合物1的分子结构由NMR初步确定后,最直观的结构证据就是单晶了。在去年的九月,实验室就拿到了碳纳米带的单晶结构,接下来的工作,就是进对结构的进一步分析和其他物化性质表征的工作,到此为止,与碳纳米带合成有关的工作就告一段落了。
当然化合物1的分子结构由NMR初步确定后,最直观的结构证据就是单晶了。在去年的九月,实验室就拿到了碳纳米带的单晶结构,接下来的工作,就是进对结构的进一步分析和其他物化性质表征的工作,到此为止,与碳纳米带合成有关的工作就告一段落了。
从单晶数据结果,研究组将碳纳米带与[6]-CPP进行了对比,尤其是各个碳碳键长的变化,证实了a环,也具有了一定的芳香性(下图共振式 minor),碳纳米带的b环相比a环,更具有芳香性(下图共振式 major)。

而从单晶结构的纵面视图看到,碳纳米带1明显比[6]-CPP的结构更具有刚性,[6]-CPP的苯环会发生一定的偏转,导致苯环一侧向内,而碳纳米带则更加固定的内外直径比更接近于1,更像一个规则的圆环。这已经初步证实了碳纳米带相比CPP,结构性质向碳纳米管更接近了。
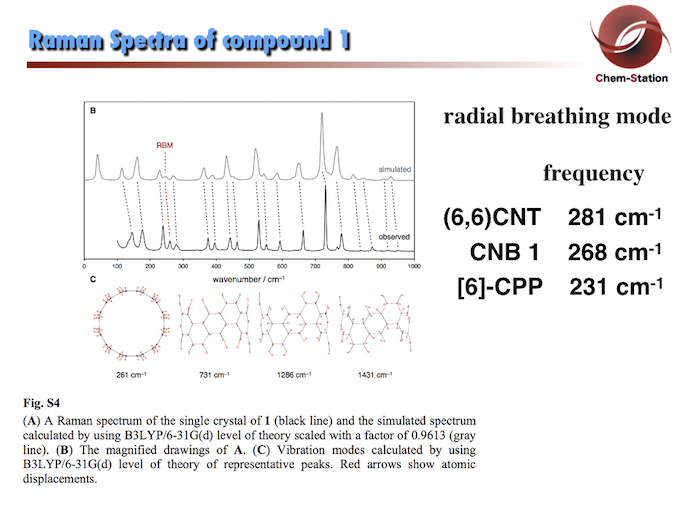
接下里通过Raman光谱数据,碳纳米带1的呼吸模式的振动频率(268 cm-1),较[6]-CPP(231 cm-1)更为接近(6,6)碳纳米管(281 cm-1)。
其他和碳纳米带有关的物理化学性质,感兴趣的可以看看论文原文中的相关讨论,尤其是它亮眼的红色荧光及独特的光电性质,使它在今后光电材料中的应用也具有相当的潜力。相信碳纳米带的首次合成,会开辟这个领域一个新的时代,也希望碳纳米管的可控合成能够不再遥不可及。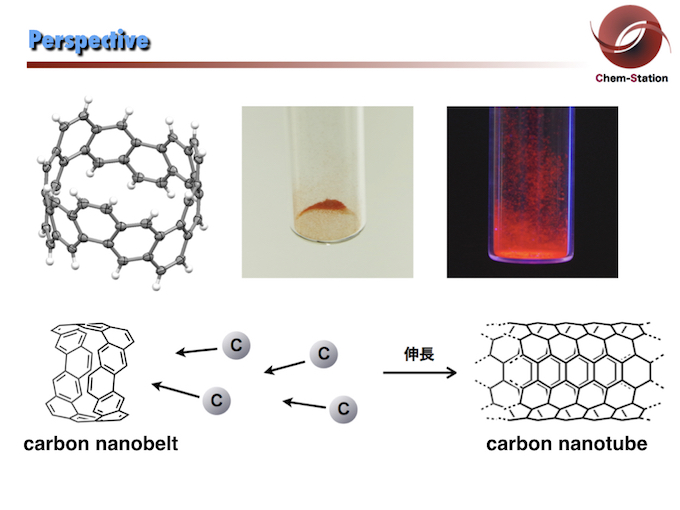
在去年的九月,实验室拿到了这个化合物的单晶,证实这个千辛万苦得来的化合物1就是碳纳米带结构的那一天,整个实验室都沸腾了,研究室的伊藤讲师也很用心的用视频记下了这个感动的瞬间。(视频来自youtube,国内读者请翻墙观看)
记得当时我把这个独家视频发到化学空间qq讨论群时,一些网友都感慨伊丹实验室浓厚并富有热情的科研氛围,这些也确实是我曾经深深感受到的那种氛围。有网友说“这辈子要是能做成一件精彩的工作可以和导师击掌庆贺,也就无憾了”
我明白伊丹老师之所以把大家聚在一起见证这个重要时刻,除了一起感受化学的美丽带来的感动,也让大家看到艰难挑战成功后的胜利喜悦,同时让大家被同辈优异成绩的激励,并转化为对科研奋斗的动力。。。

相关链接
- “Dream molecule”carbon nanobelt formed by Japanese team–The Asahi Shinbun
- Carbon puts new nanostructure under its belt (Chemistry World)
- At Last: Beautiful, consistent carbon belts ~ (ITbM research highlight)
- 筒状の炭素分子、初合成=名古屋大
- 名大、「カーボンナノベルト」初合成 単一構造のCNTに道
- できた! 夢のカーボンナノベルト 60年前に存在予言 (朝日新聞)
- カーボンナノベルト「夢の分子」初合成 名古屋大チーム
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.