作者:石油醚
谨以此文庆祝华中师范大学建校120周年!
导读:
近日,华中师大舒超课题组在著名学术期刊Angew. Chem. Int. Ed.发表论文,报道亚磺酸内酯化学最新进展。该反应利用自由基加成/二氧化硫重插入/极性环化策略为亚磺酸内酯的选择性制备提供了一个条件温和,操作简便的策略。底物适用范围广,官能团兼容性强,还可以实现复杂分子的后期制备级官能团化,同时也间接为磺内酯和巯基烷醇的构建提供了新的合成途径,
“Synthesis of Multifluoromethylated γ-Sultines by a Photoinduced Radical Addition–Polar Cyclization.
Helian Li, Yongxin Zhang, Xiaoxiao Yang, Zhenxi Deng, Zhimin Zhu, Pan Zhou, Xinke Ouyang, Yuting Yuan, Xi Chen, Lingyue Yang, Meng Liu, Chao Shu*
Angew. Chem. Int. Ed. 2023, doi:10.1002/anie.202300159.”
正文:
亚磺酸内酯(sultine)是一类非常有趣且重要的含硫杂环化合物,具有显要的开发价值,在医药、助剂与添加剂等领域都有广泛的应用。例如,γ-亚磺酸内酯衍生物可作为类固醇受体、利尿剂、香料等;同时,亚磺内酯化合物也是有机合成中一类非常重要的中间体和电解液添加剂,可作为多种重要材料如显像剂、电解液添加剂、香料的合成前体。但是目前亚磺酸内酯化学并未得到显著发展,主要原因之一是亚磺酸内酯不易合成(The chemical transformations of sultines long remained little studied due to their inaccessibility)。
目前已发展的亚磺酸内酯制备方法非常少且局限很大,例如,反应条件苛刻,需要使用有毒试剂,产率偏低,官能团兼容性差等等,这些问题显著阻碍了亚磺酸内酯的发展和应用(图1a,b)!
舒超教授近年来一直致力于重要稀缺资源型分子的设计与合成,此前通过非金属参与的自由基反应,实现了惰性烷烃碳氢硼化(Nature, 2020, 586, 714),脱羧环丙烷反应(Angew. Chem. Int. Ed. 2018, 57, 15430)以及脱硼环丁烷化反应(Angew. Chem. Int. Ed. 2019, 58, 3870)等,为系列重要资源型分子提供了全新的合成策略。
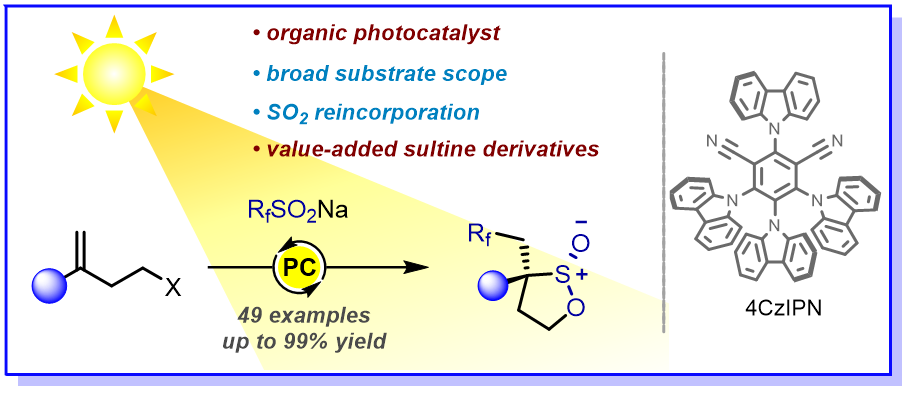
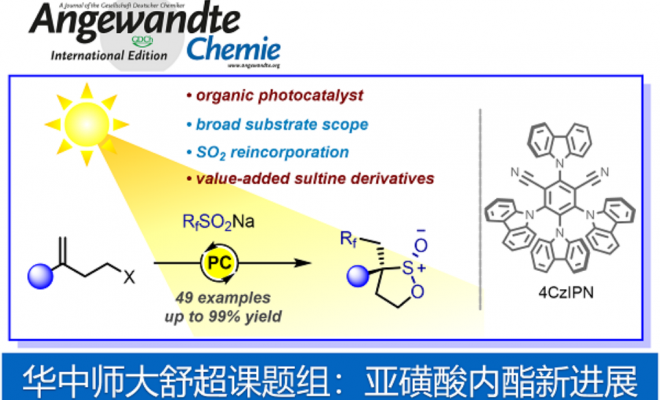
在此前工作基础上,该课题组在国内率先开展亚磺酸内酯的合成与应用研究并取得重要进展。该课题组发展了一种操作简单,无金属参与的策略,在温和条件下实现了可见光引发的自由基加成/二氧化硫重插入/极性交叉环化反应,成功应用于多氟代亚磺酸内酯的选择性合成,并对反应的独特机理进行了初步探讨(图1c)。

图1. 图片来源:(Angew. Chem. Int. Ed.)
该团队巧妙的以商业可得的廉价三氟亚磺酸钠为双官能团化试剂,同时提供氟源和二氧化硫源!作者首先进行了大量条件优化,最终以带有离去基团的烯烃为底物,简单易得的4CzIPN为有机光催化剂,乙腈为溶剂,在可见光照射下实现了目标反应!特别是当光催化剂降低到0.1 mol% 时,产率仍然可以达到85%,同时还可以在空气氛围中进行,显示了重要的应用潜力。
在最优条件下,作者探索了此类反应的底物普适性和官能团兼容性。从大量实例中,表面了该方法具有非常好的底物范围,对于多种不同种类、不同电性、不同取代的官能团都可以较好的兼容,以中等到优秀的产率得到目标产物。为了进一步表明该策略的普遍性和应用价值,作者还将此反应成功应用于更加复杂的烯烃底物中,如药物中间体Ibuprofen,Fenbufen,Loxoprofen,Etodolac,Sulbactam和氨基酸BOC-D-Alanine等的衍生物(图2)。
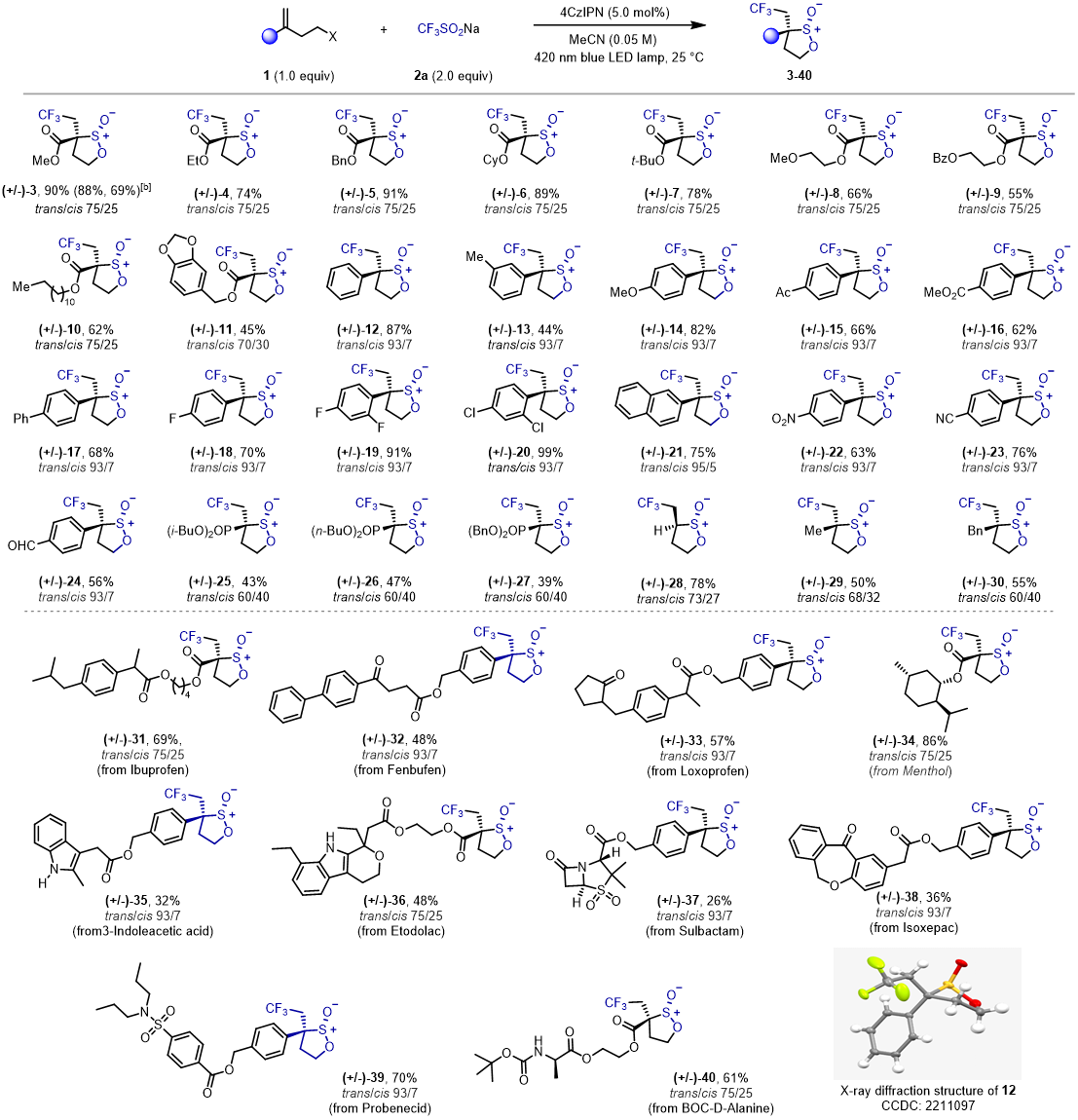
图2. 图片来源:(Angew. Chem. Int. Ed.)
同时,该反应还可以应用于其他多氟代亚磺酸内酯的制备。例如二氟亚磺酸钠也可以作为二氟试剂源参与此反应,以良好的产率得到二氟代亚磺酸内酯。其它多氟代亚磺酸内酯均可以顺利制备(图3)。
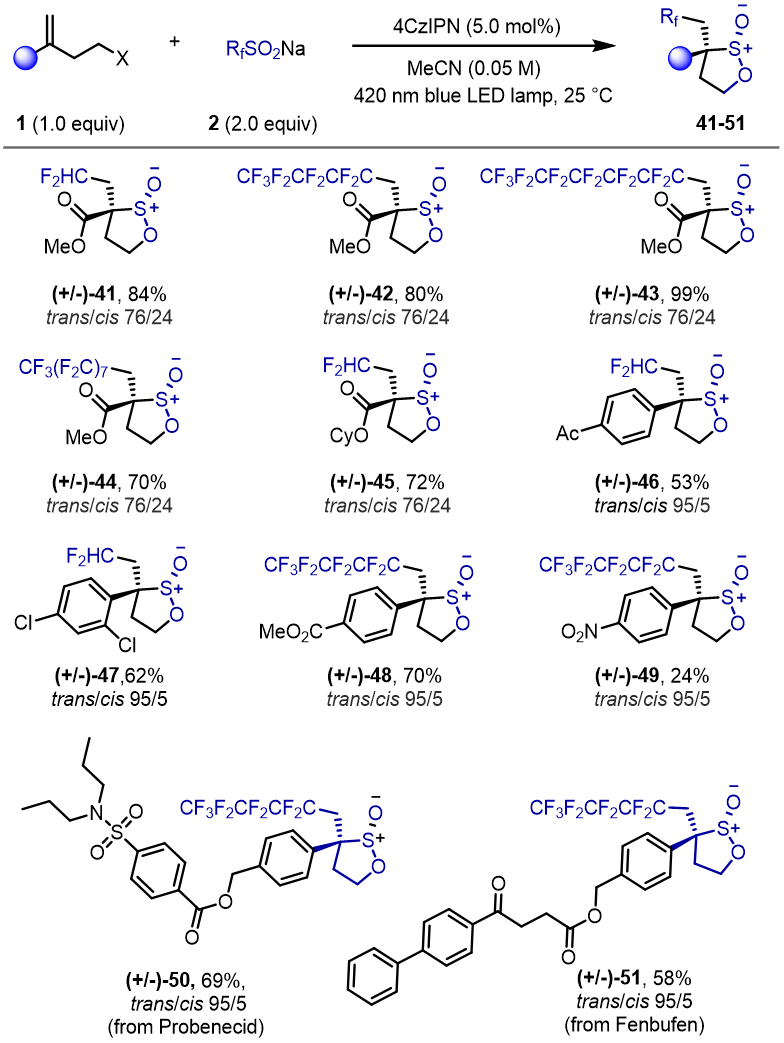
图3. 图片来源:(Angew. Chem. Int. Ed.)
进一步作者对所得化合物进行了产物转化(图 4)。首先,反应可通过克级规模进行。其次,亚磺酸内酯可通过氧化得到磺内酯,也可通过还原得到巯基烷醇,值得一提的是此类3,3-二取代的磺内酯和巯基烷醇具有重要应用且合成较为困难。最后,此类sultine还可从商业可得的高烯丙醇出发通过一锅法制备。
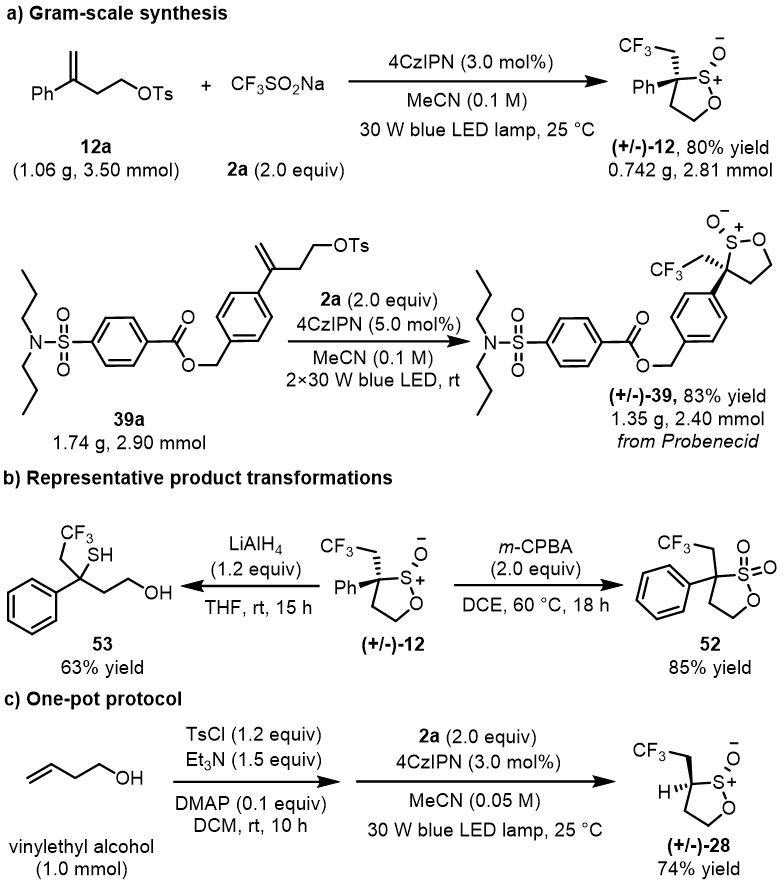
图4. 图片来源:(Angew. Chem. Int. Ed.)
最后研究人员在根据实验结果的基础上,通过大量控制实验数据,对反应的特殊选择性和可能的机理进行了初步探索(图5)。初步机理表明该反应经过了一个自由基加成/二氧化硫重插入/5-exo-tet极性环化的途径,没有观察到环丙烷和氢官能团化产物。
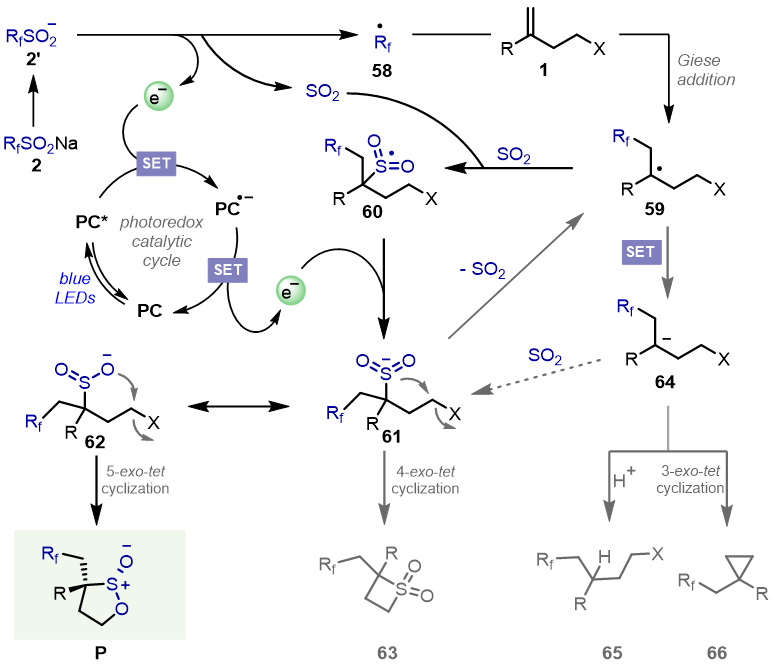
图5. 图片来源:(Angew. Chem. Int. Ed.)
总结:
总之,该课题组发展的首例光引发的自由基加成/二氧化硫重插入/极性环化策略为亚磺酸内酯的选择性制备提供了一个条件温和,操作简便的途径。该反应的底物适用范围广,官能团兼容性强,操作简便,易于放大,还可以实现复杂分子的后期制备级官能团化,同时也为磺酸内酯和巯基烷醇的制备提供了新的合成途径,将对含硫药物和电池电解液添加剂的发展提供新的可能。后续该课题组将对此类光化学环化反应合成亚磺酸内酯开展持续深入的研究。
舒超授课题组2021级硕士生李荷莲为论文第一作者,课题组其他研究生和本科生参加工作。
特别感谢厦门大学叶龙武教授,华中师大肖文精教授的鼎力支持
相关链接:课题组主页:https://www.x-mol.com/groups/chaoshu
参考文献:
- 【1】 a) D. C. Dittmer, M. D. Hoey, The Chemistry of Sulphinic Acids, Esters and their Derivatives (Ed.: S. Patai), Wiley, New York, 1990, Chap. 9, p. 239; b) O. B. Bondarenko, L. G. Saginova, N. V. Zyk, Russ. Chem. Rev. 1996, 65, 147; c) S. Kotha, P. Khedkar, Chem. Rev. 2012, 112, 1650.
- 【2】a) J. Coulomb, V. Certal, L. Fensterbank, E. Lacôte, M. Malacria, Angew. Chem. Int. Ed. 2006, 45, 633; Angew. Chem. 2006, 118, 649; b) J. Coulomb, V. Certal, M.-H. Larraufie, C. Ollivier, J.-P. Corbet, G. Mignani, L. Fensterbank, E. Lacôte, M. Malacria, Chem. Eur. J. 2009, 15, 10225.
- 【3】 G. M. T. Smith, P. M. Burton, C. D. Bray, Angew. Chem. Int. Ed. 2015, 54, 15236; Angew. Chem. 2015, 127, 15451.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载




















No comments yet.