Gelsedine-Type生物碱的系列全合成的手法被开发。通过巧妙简短的工艺,构建骨架,从同一中间体合成四种相同的生物碱。
Gelsedine-Type生物碱
从马钱科Gelsemium属分离提取出来的生物碱、具有高度的缩环结构的衍生物,根据其骨架的差异,大致分为gelsemine、humantenine、gelsedine型这三类。从有机合成化学来看,其中gelsemine是最受瞩目的,目前为止,已经有9个所属化合物实现了全合成(图1A)[1a-j]。此外、gelsedine型(含有氧杂二环[3.2.2]壬烷骨架和螺-N-甲氧基二氢吲哚酮)也有60种以上的衍生物被分离提取出来,然而他们的醛合成还有很大的挑战与改良的余地(图1B)。2011年福山透课题组首次实现了gelsemoxonine(4)的全合成[2]。然后Carreira报道了4、Ferreira 报道了gelsenicine(2)、Zhao等人报道了gelsedilam(3)的全合成路线[3-5]。最近,在2016年,福山透等人从共通中间体合成了gelsedine(1),2,以及3[6]。虽然说每条全合成路线都非常不错,但是缺点是都需要多步骤,而且1–4的网罗性的合成手法还没有实现。
在这里要介绍的是上海有机化学研究所的马大为教授课题组通过迈克尔加成实现骨架的合成,然后再通过串联氧化/羟醛环化构建螺环、通过随后的频哪醇重排短步骤合成gelsedine型天然产物的中间体(9)。然后以9出发,实现了4种Gelsedine型生物碱的网罗性全合成(图1C)。
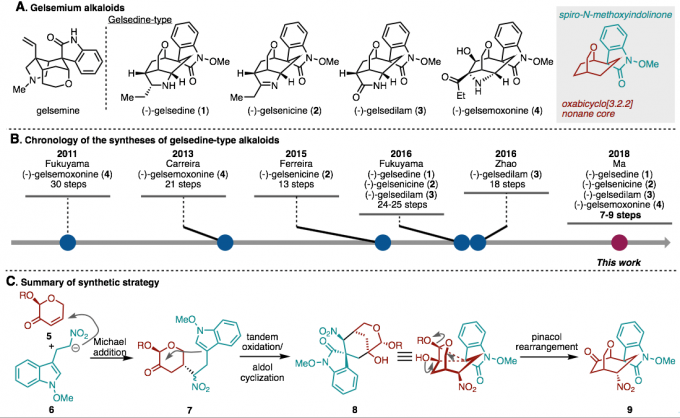
图1. (A)Gelsemium生物碱 (B) Gelsedine型生物碱的合成年表 (C) 马大为教授合成路线
“Divergent Entry to Gelsedine-Type Alkaloids: Total Syntheses of (−)-Gelsedilam, (−)-Gelsenicine, (−)-Gelsedine, and (−)-Gelsemoxonine”
Wang, P.; Gao, Y.; Ma, D. J. Am. Chem. Soc., 2018, 140, 11608–11612.
论文作者介绍

研究者:Dawei Ma
经历:
-1984 B.S., Shandong University, Jinan, China
1984-1989Ph.D., Shanghai Institute of Organic Chemistry, CAS (Prof. Xiyan Lu)
1990–1994Postdoctoral fellow, University of Pittsburgh and Mayo Clinic, U.S.A.
1995–Professor, State Key Laboratory of Bioorganic Chemistry, Shanghai Institute of Organic Chemistry, Chinese Academy of Sciences, P. R. China
2000–Director, State Key Laboratory of Bioorganic Chemistry, Shanghai Institute of Organic Chemistry, Chinese Academy of Sciences
研究内容:天然产物权合成、新合成方法学开发
论文概要
首先、烯酮5(从L-阿拉伯糖为原料4步合成)与吲哚6(从芦竹碱开始3步合成)先进行迈克尔加成意图得到产物7(图2A)。在反应条件筛选中发现,使用有机碱的话反应无法进行,最终反应在无机碱(碳酸铯)下,得到了高产率的立体选择性产物7(1:1、硝基碳的立体异构体混合物)。然后、7在NCS条件下发生氯化/消除(串联氧化)、继而羟醛环化成功构筑了螺环骨架。并且得到的螺环8a的立体结构基本是单一结构(major)、8b由于与硝基部位存在的立体位阻所以没有生成(图2B)。8a在TEA与硅胶处理后异构化得到了热力学稳定的化合物8。之后、在氯化铝参与下进行频哪醇重排从8合成了共通中间体9(产率86%)。然后9再与氯甲酸甲酯进行乙酰化/丙酰氰化引入酮羰基,从而进一步合成出4种Gelsedine型生物碱。
如上所述、本合成方法没有使用保护基,因此是目前最短的合成法(从5与6为原料出发只需要7-9步),并且一次性用于合成4种Gelsedine型生物碱導。此外合成的中间体9、可以用于合成类似的生物碱衍生物,有助于生物活性的构效关系的研究。

图2. (A)共通中间体9の合成 (B) 螺环的立体选择性的构建(minor成分) (C) X射线单晶衍射结构分析 (8与9)
参考文献
- (a) Sheikh, Z.; Steel, R.; Tasker, A. S.; Johnson, A. P. J. Chem. Soc., Chem. Commun. 1994, 763.DOI: 10.1039/C39940000763(b) Dutton, J. K.; Steel, R. W.; Tasker, A. S.; Popsavin, V.; Johnson, A. P. J. Chem. Soc., Chem. Commun.1994, 765. DOI: 10.1039/C39940000765(c) Newcombe, N. J.; Ya, F.; Vijn, R. J.; Hiemstra, H.; Speckamp, W. N. J. Chem. Soc., Chem. Commun.1994, 767. DOI: 10.1039/C39940000767(d) Fukuyama, T.; Liu, G. J. Am. Chem. Soc.1996, 118,7426. DOI: 10.1021/ja961701s(e) Atarashi, S.; Choi, J.-K.; Ha, D.-C.; Hart, D. J.; Kuzmich, D.; Lee, C.- S.; Ramesh, S.; Wu, S. C. J. Am. Chem. Soc. 1997, 119, 6226. DOI:10.1021/ja970089h(f) Madin, A.; O’Donnell, C. J.; Oh, T.; Old, D. W.; Overman, L. E.; Sharp, M. J. Angew. Chem., Int. Ed. 1999, 38,2934. DOI: 10.1002/(SICI)1521-3773(19991004)38:19<2934::AID-ANIE2934>3.0.CO;2-L (g) Yokoshima, S.; Tokuyama, H.; Fukuyama, T. Angew. Chem., Int. Ed. 2000, 39, 4073. 10.1002/1521-3773(20001117)39:22<4070::AID-ANIE4070>3.0.CO;2-C(h) Ng, F. W.; Lin, H.; Danishefsky, S. J. J. Am. Chem. Soc. 2002, 124, 9812. DOI:10.1021/ja0204675(i) Zhou, X.; Xiao, T.; Iwama, Y.; Qin, Y. Angew. Chem., Int. Ed. 2012,51,4909. DOI: 10.1002/anie.201201736(j) Chen, X.; Duan, S.; Tao, C.; Zhai, H.; Qiu, F. G. Nat. Commun. 2015, 6, 7204. DOI: 10.1038/ncomms8204
- Shimokawa, J.; Harada, T.; Yokoshima, S.; Fukuyama, T. J. Am. Chem. Soc. 2011,133,17634. DOI:10.1021/ja208617c
- Diethelm, S.; Carreira, E. J. Am. Chem. Soc.2013, 135, 8500. DOI:10.1021/ja403823n
- Newcomb, E. T.; Knutson, P. C.; Pedersen, B. A.; Ferreira, E. J. Am. Chem. Soc.2016, 138, 108. DOI:10.1021/jacs.5b12263
- Huang, Y.; Liu, Y.; Zheng, C.; Jin, Q.; Pan, L.; Pan, R.; Liu, J.; Zhao, G. Chem. Eur. J. 2016,22, 18339-18342. DOI:10.1002/chem.201604620
- Harada, T.; Shimokawa, J.; Fukuyama, T. Org. Lett. 2016, 18,4622−4625. DOI:10.1021/acs.orglett.6b02263
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!


















No comments yet.