概要
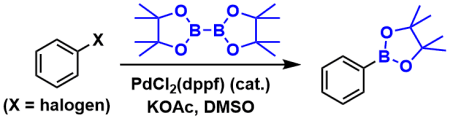
由芳基或烯基卤化物/三氟甲磺酸酯作为底物与钯催化剂合成有机硼酸化合物的方法。市售的频哪醇二硼化合物(PinB-BPin)常常作为硼源。另一方面使用H-BPin、(HO)2B-B(OH)2作为硼源的条件也有所报道。
近年来,随着铱催化剂的开发应用,不通过卤素,直接经由C-H活化进行硼酸化的反应被开发(Hartwig·Miyaura硼化)。 请参阅关联反应。
关联反应
- Liebeskind-Srogl Cross Coupling
- Cross Dehydrogenative Coupling (CDC)
- Catalytic C-H Oxidation
- Hofmann-Löffler-Freytag Reaction
- Catalytic C-H activation
- C-H Insertion of Metal Carbenoid
- Brown Hydroboration
- Suzuki-Miyaura Cross Coupling
- Hartwig-Miyaura C-H Borylation
基本文献
- Ishiyama, T.; Murata, M.; Miyaura, N. J. Org. Chem. 1995, 60, 7508. DOI: 10.1021/jo00128a024
- Murata, M.; Watanabe, S.; Masuda, Y. J. Org. Chem. 1997, 62, 6458. DOI: 10.1021/jo970963p
- Murata, M.; Oyama, T.; Watanabe, S.; Masuda, Y. J. Org. Chem. 2000, 65, 164. DOI: 10.1021/jo991337q
- Takagi, J.; Takahashi, K.; Ishiyama, T.; Miyaura, N. J. Am. Chem. Soc. 2002, 124, 8001. DOI: 10.1021/ja0202255
<review>
- Ishiyama, T.; Miyaura, N. Chem. Rec. 2004, 3, 271. DOI: 10.1002/tcr.10068
- Shimizu, M.; Hiyama, T. Eur. J. Org. Chem. 2013, 36, 8096. DOI: 10.1002/ejoc.201300632
- Chow, W. K.; Yuen, O. Y.; Choy, P. Y.; So, C. M.; Lau, C. P.; Wong, W. T.; Kwong, F. Y. RSC Adv. 2013, 3, 12518. DOI: 10.1039/C3RA22905J
- Shinokubo, H. Proc. Jpn. Acad. Ser. B. 2014, 90, 1. doi:10.2183/pjab.90.1
反应机理
基本反应机理与钯交叉偶联相似。具体请参照Suzuki-Miyaura Cross Coupling。
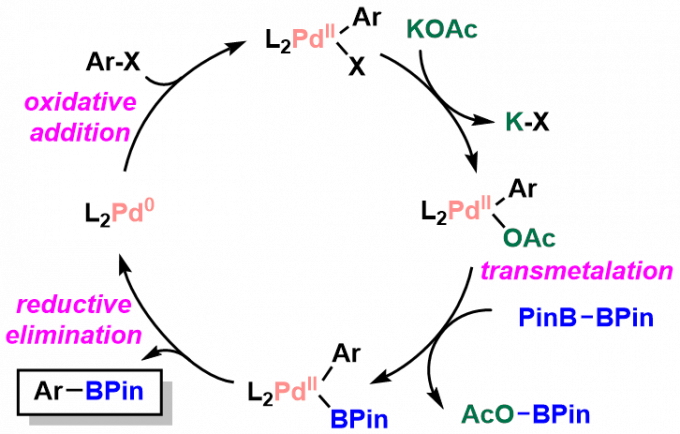
反应实例
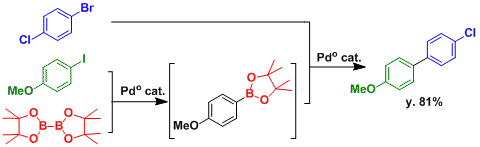
通过选择具有适当反应性的底物,可以经过Miyaura硼酸化→Suzuki-Miyaura交叉偶联的连续反应获得联芳烃。
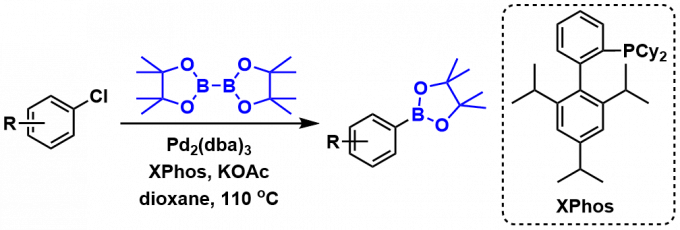
适用于低反应性氯代芳烃的反应条件[1]
实验步骤
芳基溴化物的硼化[2]
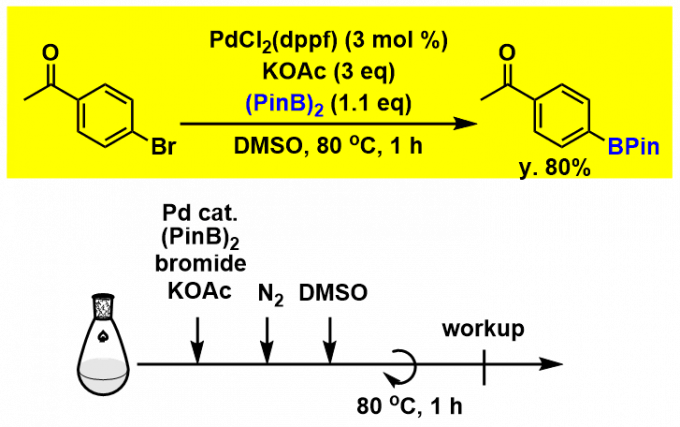
实验技巧
※碱的话KOAc是最优的。在使用像K2CO3,K3PO4这样相对强的碱的话,会伴随形成铃木偶联形式的二聚体副产物。对三氟甲磺酸烯基酯作为底物的时候,使用KOPh做为碱进行反应。
※对于溶剂,反应速度如下 DMSO >> DMF > 1,4-dioxane。
参考文献
- (a) Billingsley, K. L.; Barder, T. E.; Buchwald, S. L. Angew. Chem. Int. Ed. 2007, 46, 5359. doi:10.1002/anie.200701551 (b) Billingsley, K. L.; Buchwald, S. L. J. Org. Chem. 2008, 73, 5589. DOI: 10.1021/jo800727s
- Ishiyama, T.; Murata, M.; Miyaura, N. J. Org. Chem. 1995, 60, 7508. DOI: 10.1021/jo00128a024
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!




















No comments yet.