- 概要
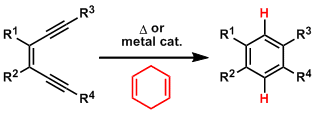
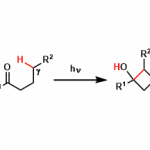
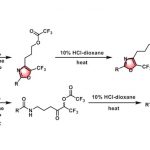
cis-1,5-戊二炔-3-烯加热到200℃以上,1,4-苯环双自由基生成。这个双自由基反应活性非常高,这时有氢离子受体的话就会迅速夺取氢,成为苯环。
环化的速度取决于二炔烯的原子间距,趋近于3.34Å时更容易环化。
- 基本文献
・Darby, N.; Kim, C.U.; Salaun, J.A.; Shelton, K.W.; Takada, S.; Masamune, S. J. Chem. Soc. 1971, 23, 1516.
・Jones, R. R.; Bergman, R. G. J. Am. Chem. Soc. 1972, 94, 660. DOI: 10.1021/ja00757a071
・Bergman, R. G. Acc. Chem. Res. 1973, 6, 25. DOI: 10.1021/ar50061a004
・Nicolaou, K. C. et al. Proc. Natl. Acad. Sci. USA 1993, 90, 5881.
・Nicolaou, K. C. et al. Chem. Ber. 1994, 41, 33.
・Grissom, J. C. et al. Tetrahedron 1994, 50, 4635. doi:10.1016/S0040-4020(01)85004-3
・Bowles, D. M.; Palmer, G. J.; Landis, C. A.; Scott, J. L.; Anthony, J. E. Tetrahedron 2001, 57, 3753. doi:10.1016/S0040-4020(01)00247-2
・Basak, A.; Mandal, S.; Bag, S. S. Chem. Rev. 2003, 103, 4077. DOI: 10.1021/cr020069k
・Rawat, D. S.; Zaleski, J. M. Synlett 2004, 393. DOI: 10.1055/s-2004-815422
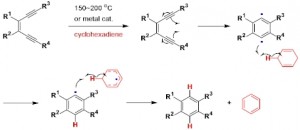
- 反应机理
(参考:J. Org. Chem. 1994, 59, 5833
- 反应实例
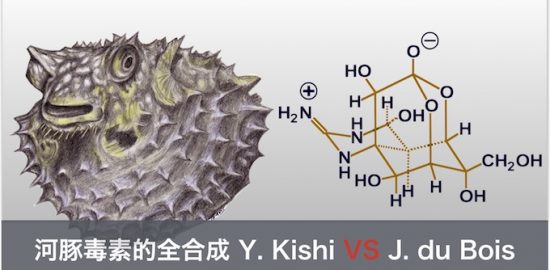
neocarzinostatin、Dynemicin、Calicheamicin等烯二炔类化合物含有DNA识别作用的烯二炔官能团。将烯二炔部位用Bergman环化反应产生双自由基从而切断DNA分子,是一种对抗肿瘤的方法。
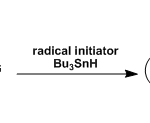
通常的烯二炔天然物质就这么样是不能发生Bergman环化的,因此生物体内的反应需要引发剂接近末端的烯二炔部分从而实现环化反应。
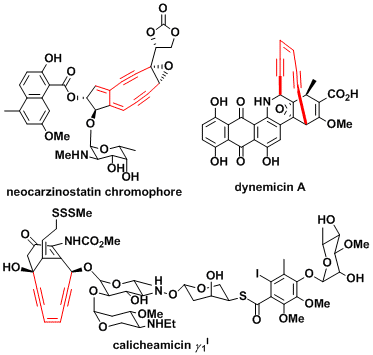
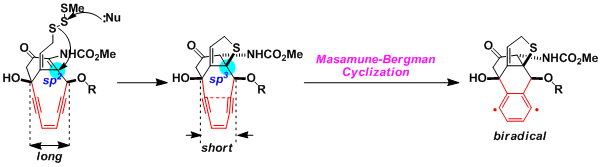
下面通过一些例子说明Calicheamicin的双自由基生成的机理。这种情况下二硫作为亲和取代引发剂导致了分子内环化,从而碳原子sp3杂化,接近炔基的末端实现了Bergman环化。
- 实验步骤
- 实验技巧
- 参考文献