作者:杉杉
导读:
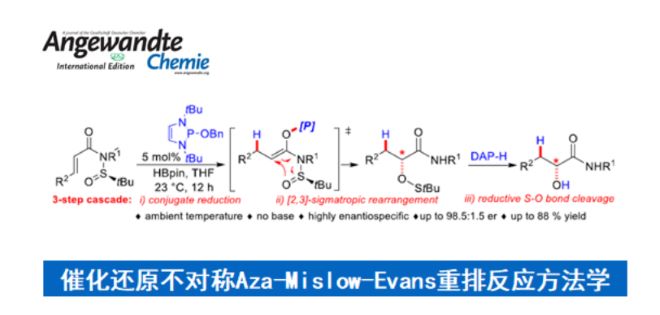
近日,Lausanne联邦理工学院的N. Cramer课题组在Angew. Chem. Int. Ed.中发表论文,报道一种全新的采用DAP-H (1,3,2-diazaphospholene hydride)催化剂促进的通N-亚磺酰基丙烯酰胺 (N-sulfinyl acrylamides)衍生物参与的还原不对称aza-Mislow-Evans重排反应方法学,进而成功完成一系列对映富集的α-羟基酰胺分子的构建。
Reductive Asymmetric Aza-Mislow-Evans Rearrangement by 1,3,2-Diazaphospholene Catalysis
G.Zhang, N.Cramer, Angew. Chem. Int. Ed. 2023, ASAP. doi: 10.1002/anie.202301076.
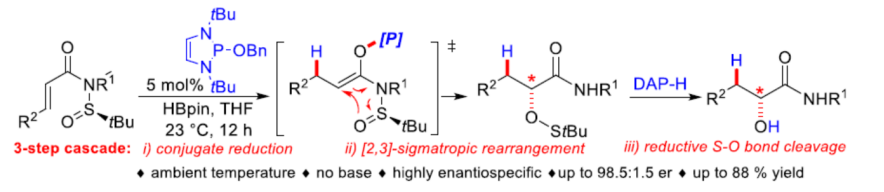
正文:
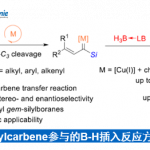
近年来,通过DAP-H (P-hydrido-1,3,2-diazaphospholene hydride)催化剂促进的1,4-还原与α-官能团化反应方法学 (Scheme 1a) [1]-[2]已经备受诸多研究团队的广泛关注。然而,对于采用DAP-H催化剂参与的不对称还原α-官能团化反应方法学,目前却仍面临诸多的挑战。这里,受到Mislow-Evans (Scheme 1b)[3] 以及aza-Misslow-Evans重排[4]-[5]反应方法学相关研究报道的启发,Lausanne联邦理工学院的N. Cramer课题组成功设计出一种全新的采用DAP-H (1,3,2-diazaphospholene hydride)催化剂促进的通过N-亚磺酰基丙烯酰胺 (N-sulfinyl acrylamides)衍生物参与的还原不对称aza-Mislow-Evans重排反应方法学 (Scheme 1c)。
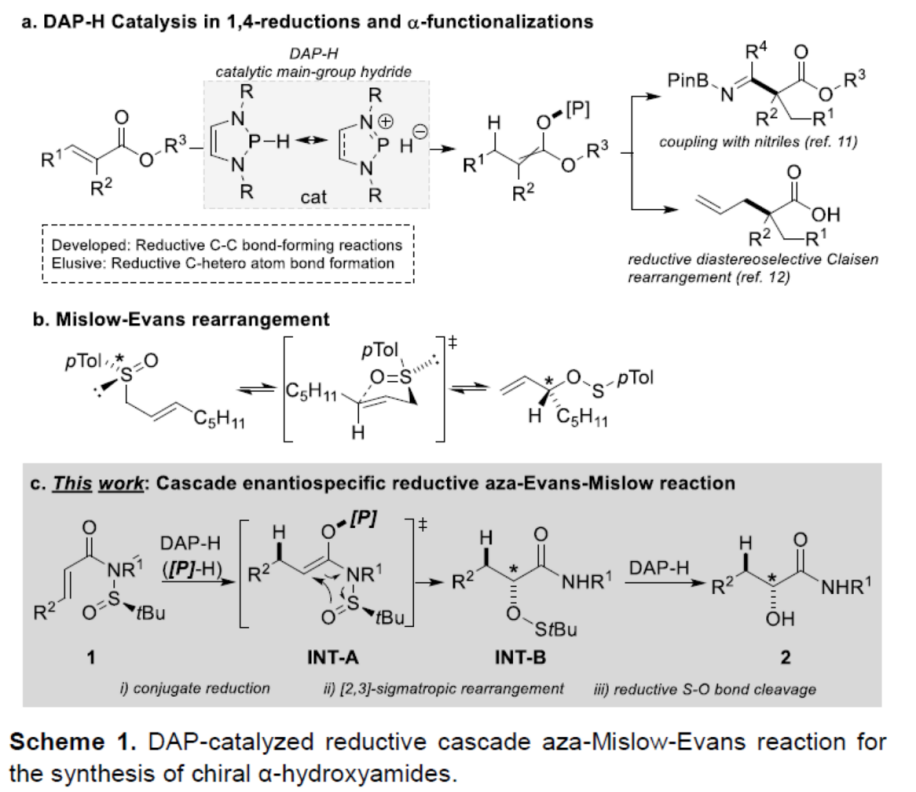
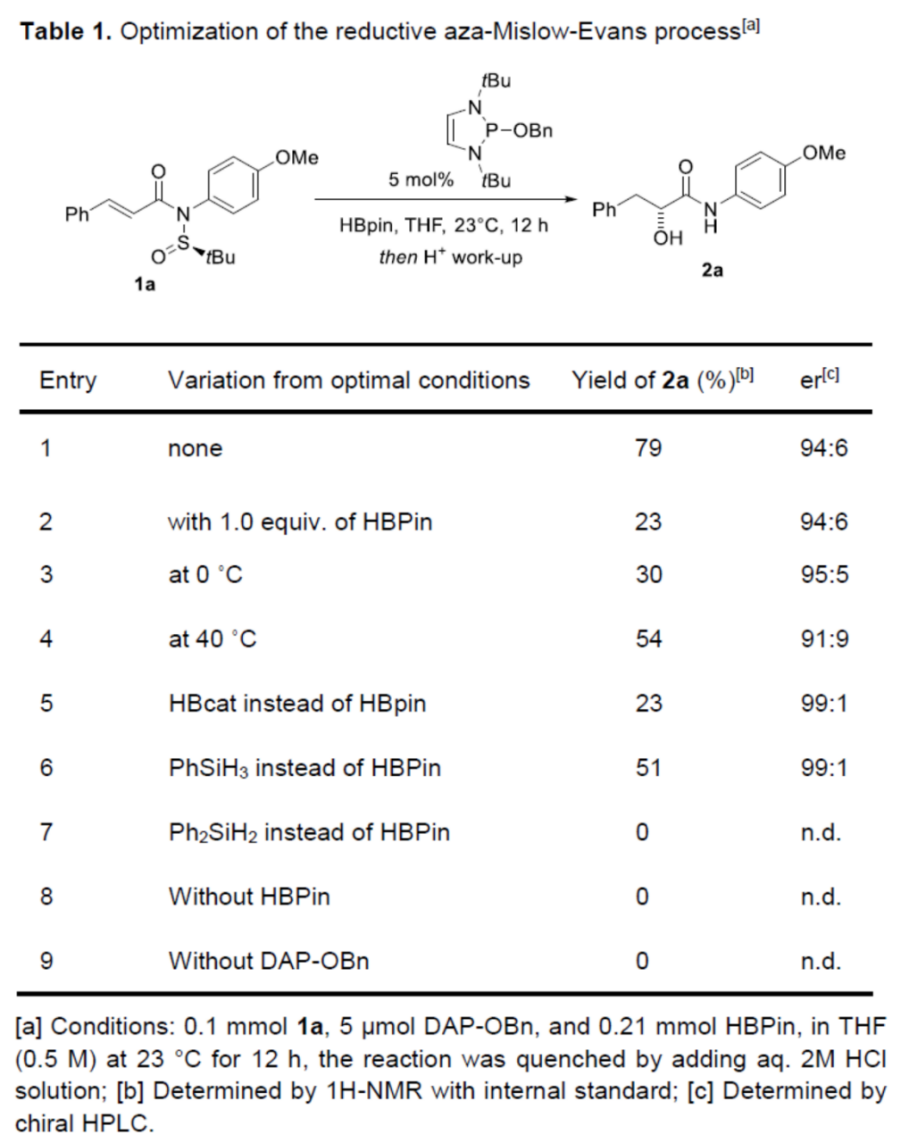
首先,作者采用(R)-N-(tert-butylsulfinyl)-N-(4-methoxyphenyl) cinnamamide (1a)作为模型底物,进行相关反应条件的优化筛选 (Table 1)。进而确定最佳的反应条件为:采用DAP-OBn作为催化剂前体,HBPin作为还原剂,THF作为反应溶剂中,反应温度为23 oC,并进一步通过酸处理后,最终获得79%收率的重排产物2a (94:6 er)。
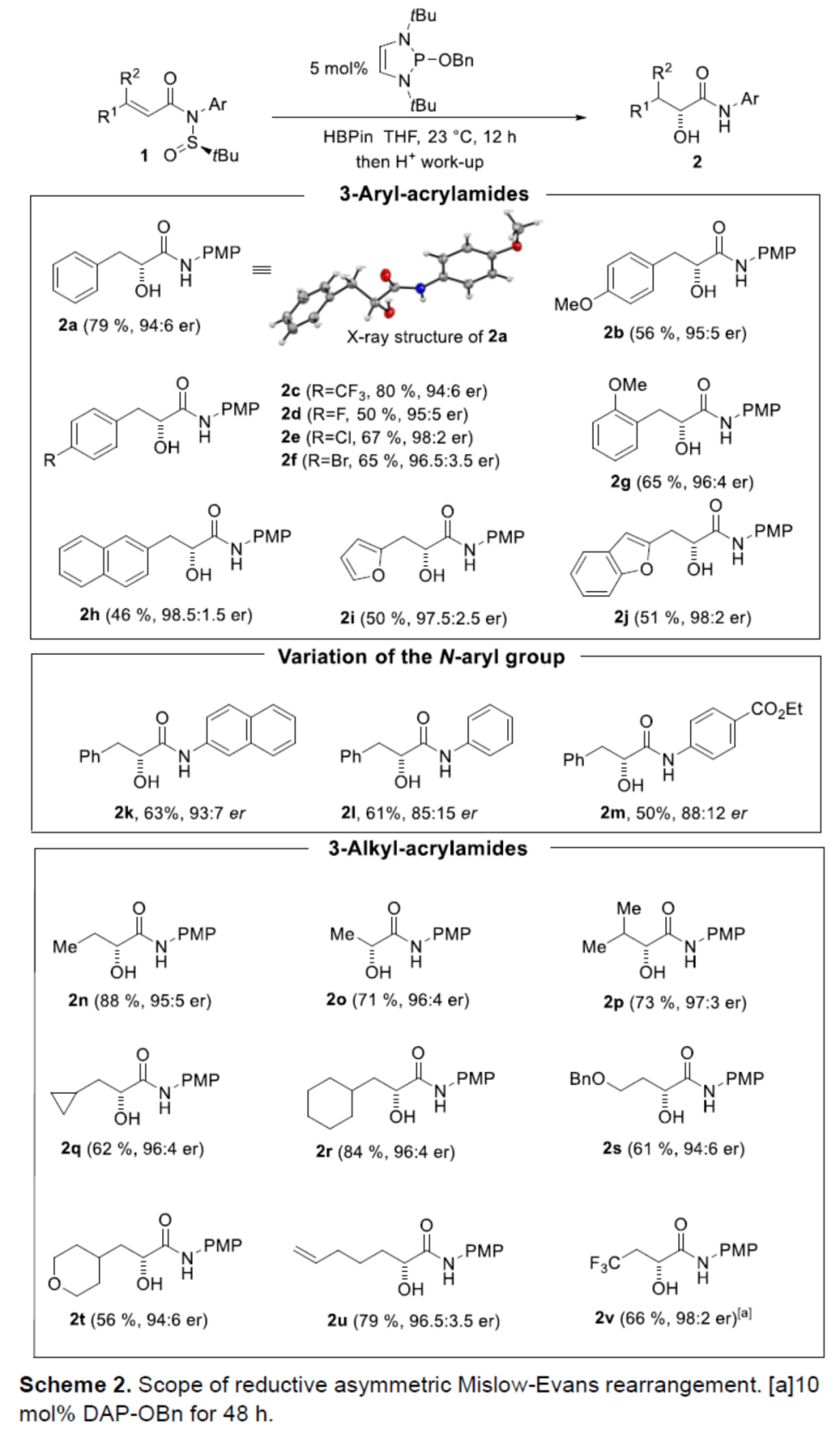
在上述的最佳反应条件下,作者分别对一系列N-亚磺酰基丙烯酰胺底物的应用范围进行深入研究 (Scheme 2)。

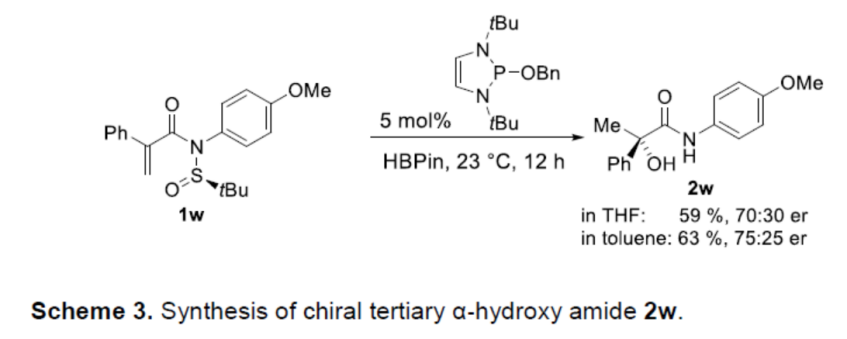
同时,该小组发现,采用上述的还原不对称aza-Mislow-Evans重排反应策略,同样能够完成手性三级α-羟基酰胺分子的构建 (Scheme 3)。
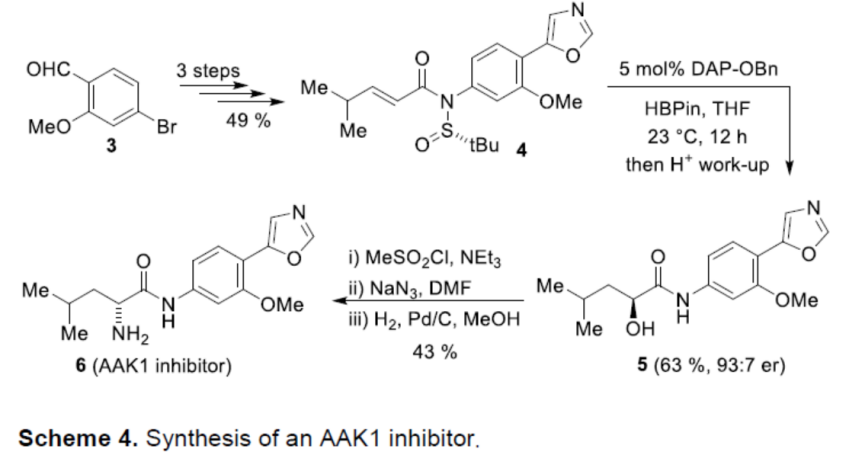
之后,该小组通过如下的一系列研究进一步表明,这一全新的对映选择性aza-Mislow-Evans重排反应策略具有潜在的合成应用价值 (Scheme 4)。
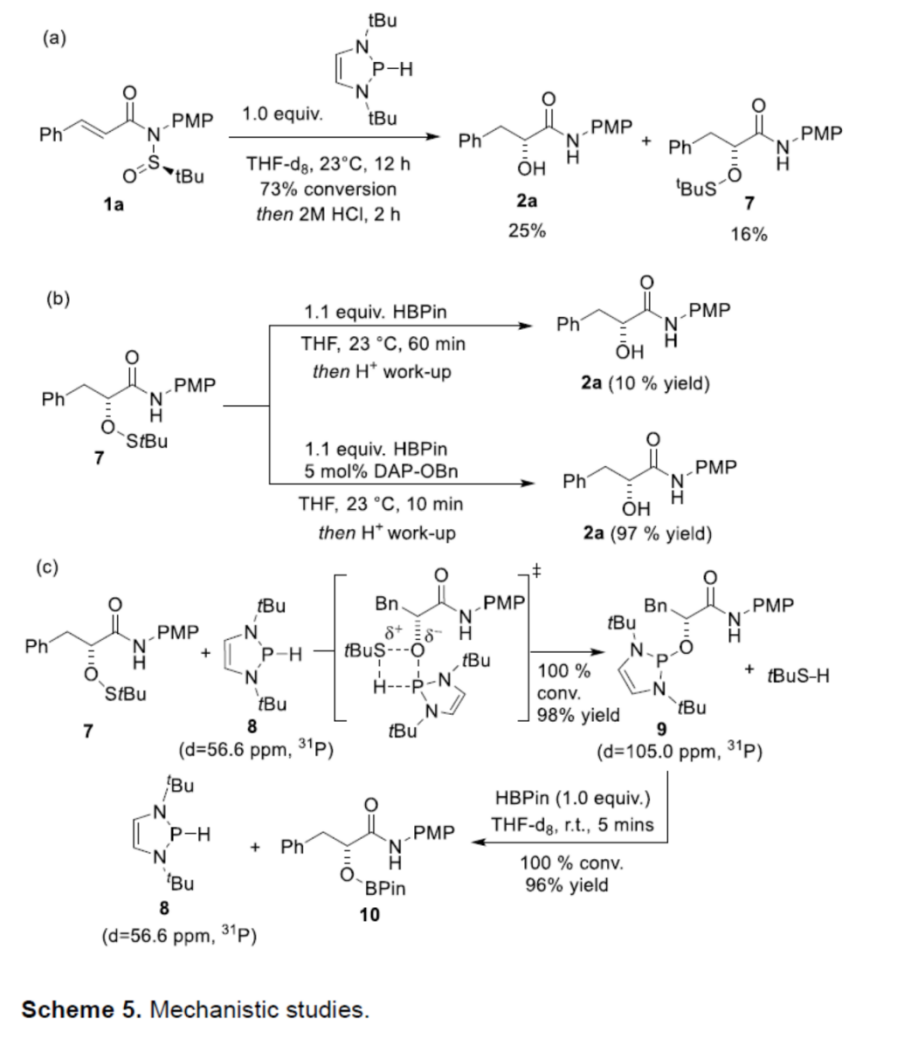
接下来,作者通过如下一系列相关的控制实验,对于上述还原不对称aza-Mislow-Evans重排过程的反应机理进行进一步研究 (Scheme 5)。

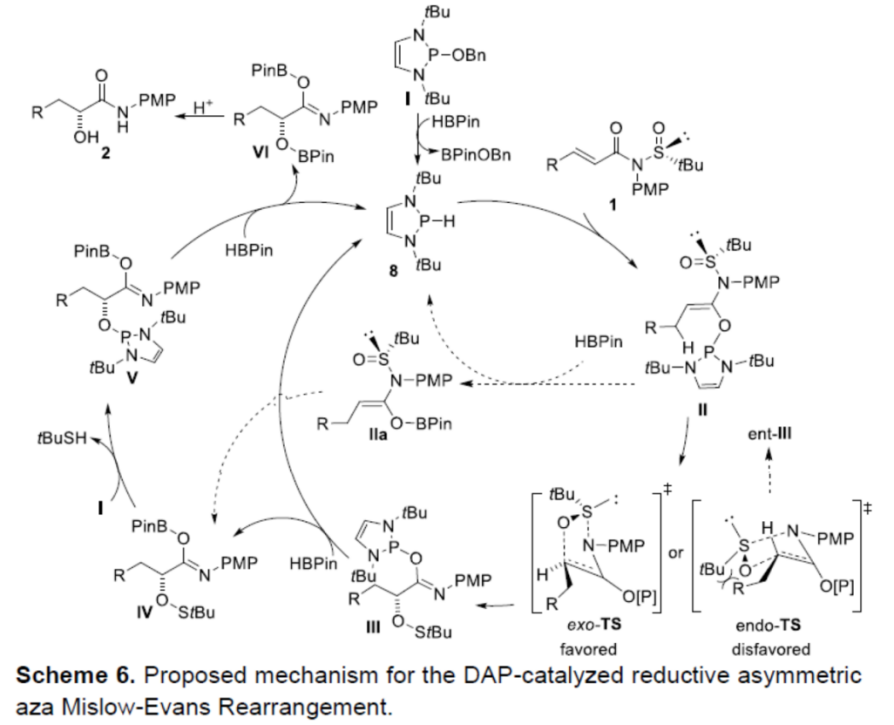
基于上述的实验研究以及前期相关的文献报道[6]-[7],作者提出如下合理的反应机理 (Scheme 6)。
总结:Lausanne联邦理工学院的N. Cramer团队成功设计出一种全新的采用DAP-H催化剂促进的通N-亚磺酰基丙烯酰胺衍生物参与的还原对映选择性aza-Mislow-Evans重排反应方法学,进而成功完成一系列对映富集的α-羟基酰胺分子的构建。这一全新的还原对映选择性aza-Mislow-Evans重排反应策略具有广泛的底物应用范围、温和的反应条件、优良的官能团兼容性以及优良的对映专一性等优势。
参考文献:
- [1] C. Chong, B. Rao, R. Kinjo, ACS Catal. 2017, 7, 5814. doi: 10.1021/acscatal.7b01338.
- [2] J. H. Reed, P. A. Donets, S. Miaskiewicz, N. Cramer, Angew. Chem. Int. Ed. 2019, 58, 8893. doi: 10.1002/anie.201904411.
- [3] P. Bickart, F. W. Carson, J. Jacobus, E. G. Miller, K. Mislow, J. Am. Chem. Soc. 1968, 90, 4869. doi: 10.1021/ja01020a021.
- [4] C. C. Chong, R. Kinjo, Angew. Chem. Int. Ed. 2015, 54, 12116. doi: 10.1002/anie.201505244.
- [5] B. S. N. Huchenski, K. N. Robertson, A. W. H. Speed, Eur. J. Org. Chem. 2020, 2020, 5140. doi: 10.1002/ejoc.202000880.
- [6] F. Tang, Y. Yao, Y. Xu, C. Lu, Angew. Chem. Int. Ed. 2018, 57, 15583. doi: 10.1002/anie.201809551.
- [7] P. Ma, F. Tang, Y. Yao, C. Lu, Org. Lett. 2019, 21, 4671. doi: 10.1021/acs.orglett.9b01555.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载




















No comments yet.