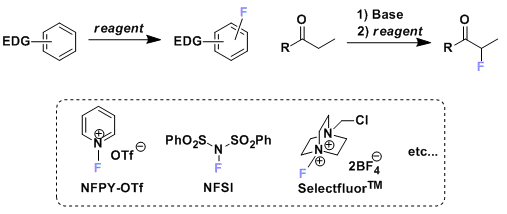
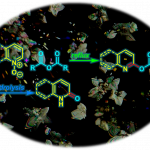
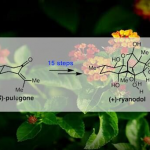
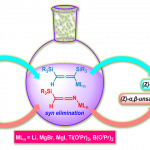
苯衍生物、羰基化合物→卤代物
概要
氟原子在立体大小上看与氢原子很类似,但是在电负性上确实全然相反的呈阴性。由于这个特性,当氢被氟置换后,在构造上变化不大,但是整个新分子的电子构成确有显著改变。另外C-F键相对于C-H键结合更牢固,化合物的稳定性也更强。例如当消旋化比较容易的分子的H被F取代后,就能够增加手性的稳定性。
由于这些性质,氟化反应经常被用于在医药品的探索合成以及材料化学中,是十分重要的一个反应。而到目前为止虽然一些列的氟化反应被开发出来,但是高效的工业合成法还是有所欠缺,所以其潜在价值还是很大的。
同时,近年来,由于不对称催化剂的发展,対映选择性的氟化反应也渐渐变热。有兴趣的同志们可以关注下这方面的研究。
基本文献
- Umemoto, T.; Kawada, K.; Tomita, K. Tetrahedron Lett. 1989, 27, 4465. doi:10.1016/S0040-4039(00)84980-1
- Singh, S.; DesMarteau, D. D.; Zuberi, S. S.; Witz, M.; Huang, H. N. J. Am. Chem. Soc. 1987, 109, 7194. DOI: 10.1021/ja00257a051
- Banks, R. E. et al. J. Fluorine Chem. 1990, 46, 297.
- Nyffeler, P. T.; Duron, S. G.; Burkart, M. D.; Vincent, S. P.; Wong, C.-H. Angew. Chem. Int. Ed. 2005,44 192. doi:10.1002/anie.200400648
- Kirk, K. L. Org. Process Res. Dev. 2008, 12, 305. doi:10.1021/op700134j
反应机理
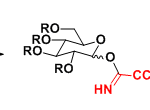
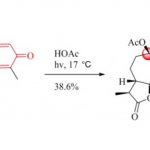
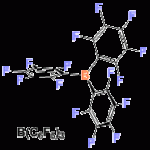
反应实例
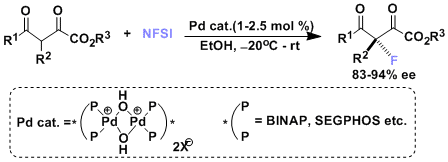
催化不对称氟化反应[1]
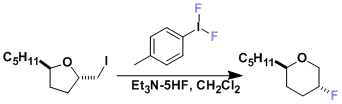
碘甲苯氟化试剂[2]:近年来新开发的亲电子氟化试剂。与其他氟化试剂相比,低毒性,稳定容易取用。
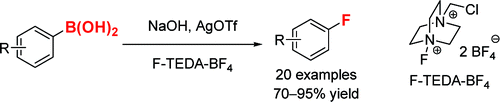
芳醇化合物与亲电子氟化试剂的反应活性比较低,一般来说很难进行氟化取代反应。Ritter等人开发了芳基硼酸与锡试剂的氟化方法。[4][5]
实验步骤
实验技巧