本文作者 石油醚
概要
Fabien Gagosz, 渥太华大学化学与生物分子科学系教授,有机化学家。课题组主页:https://www.thegagoszgroup.com/
经历
- 1994-1997年 斯特拉斯堡大学获得学士学位
- 1997年 法国路易斯-巴斯德大学DEA(Dr. C. Mioskowski)
- 1998-2002年 巴黎综合理工大学获得博士(Prof. S. Z. Zard)
- 2003-2004年 伦敦大学博士后(Prof. W. B. Motherwell)
- 2004-2007年 巴黎综合理工大学CNRS研究员(CR2)
- 2007-2012年 巴黎综合理工大学CNRS研究员(CR1)
- 2012-2016年 巴黎综合理工大学CNRS研究员(DR2)
- 2016-至今 渥太华大学正教授
获奖经历
- 2013 Junior Distinguished Member of the French Chemical Society
- 2012 ACROS award for young investigator from the French Chemical Society
- 2010 Thieme Chemistry Journal Award
- 2008 CNRS Bronze Medal Award
- 2003 Dina Surdin Ph.D. Thesis Award from the French Chemical Society
- 2002 “Roche Symposium for Leading Chemists of the Next Decade” Award
研究方向
Fabien Gagosz教授的研究兴趣集中在设计新的催化方法学,并将其用于开发各种感兴趣的分子结构合成。课题组研究计划专注于新催化反应的设计和新合成方法的开发,特别关注和偏爱后过渡金属催化和金的均相催化。
1. 金催化
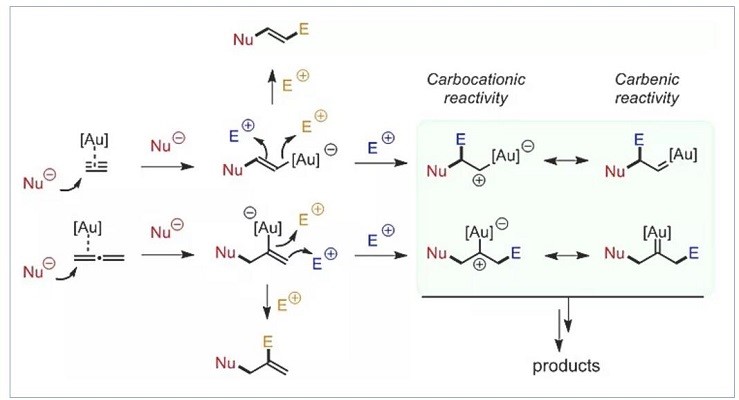
金的均相催化是一种可有效地使碳-π体系官能团化并为分子复杂性和多样性生成的一种特定且功能强大的合成方法。亲电的金络合物在其他官能团存在的情况下选择性与炔烃或联烯结合,并通过多种亲核物质激活它们实现官能团化的能力,为发现新的转化提供了独殊的机会。除了作为Lewis酸之外,金还可能作为电子供体,从而使中间阳离子物种稳定。金配合物还具有无毒、耐氧和与水环境相容的特性,因此可以在环境友好的工业过程和实际操作中具有潜在应用。Gagosz课题组正在利用亲电金络合物的独特反应性来发现可能适用于有机合成各个领域的新颖有机化学反应(scheme 1)。
Scheme 1 金催化
1.1 新型金催化剂
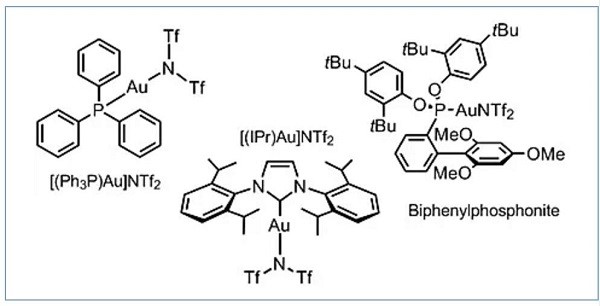
为了提高反应的效率和选择性,开发新反应性并调节合成转化中金中间体的作用,新的金催化剂的合成至关重要。Gagosz小组在这一领域很活跃,已经开发了多个金(I)配合物家族(scheme 2),并且已被该领域的研究小组广泛使用1-3。
Scheme 2 新型金催化剂
1.2 环化–多重键形成转化
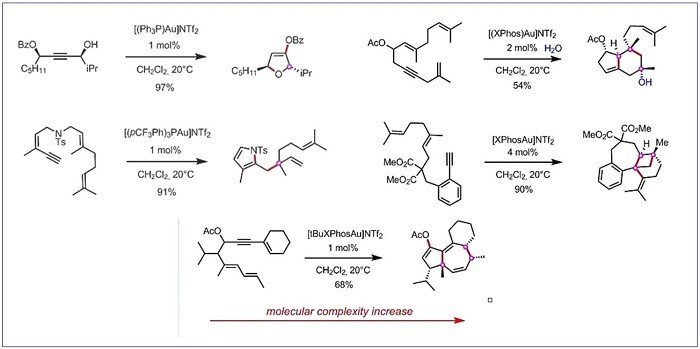
通过利用金物种亲电的独特反应性,Gagosz教授团队设计并开发了能够在一次反应中以立体选择性的方式形成多个C-C或C-杂原子键的催化过程4-8(Scheme 3)。
Scheme 3环化-多重键形成转化
1.3 氮宾转移到碳π–系统
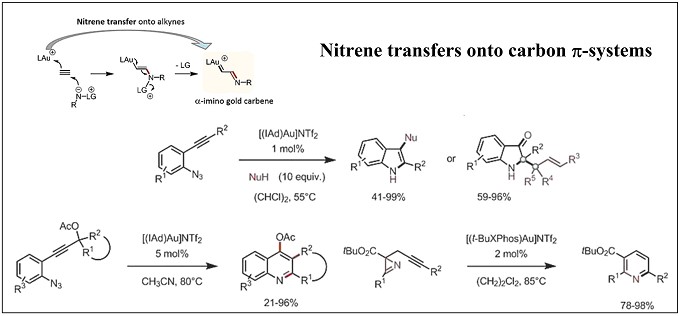
金催化反应中,具有离子化基团的氮亲核配合物可以在碳π-体系上转移氮宾化合物。Gagosz课题组利用这种类型的反应来开发能够以炔烃和联烯基团作为底物的氨基官能团化合成各种氮杂环的方法9-14(Scheme 4)。
Scheme 4 氮宾转移到碳π-系统
2. 氢转移过程
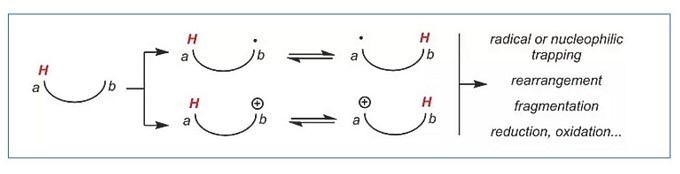
氢转移,无论是在亲电活化下以氢化物(H-)形式还是在氢自由基(H∙)中形式,都是使有机分子官能化并增加其结构复杂性的有用方法。尽管多年来已经报道了涉及这些过程的许多转化,但是这种反应仍然没有在合成方法的背景下得到充分的利用。使用金催化或自由基化学设计和开发了碳-π系统(烯烃,炔烃,联烯)加氢官能化和C-H键官能团化的转化(scheme 5)。
Scheme 5氢转移过程
2.1 氢转移过程
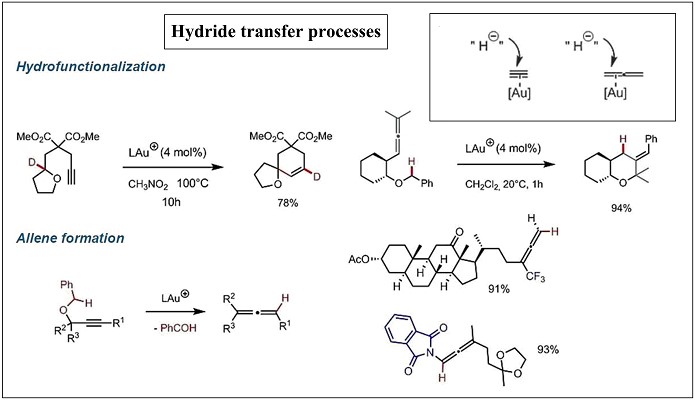
金的催化作用可以产生高度亲电的中间产物,是进行氢化物转移的一个特别有用的工具。Gagosz教授小组利用这一特性在金活化的炔烃与丙二烯或亲电金中间体上进行分子内氢转移的转化15-20(Scheme 6)。
Scheme 6 氢转移过程转化
2.2 自由基氢转移
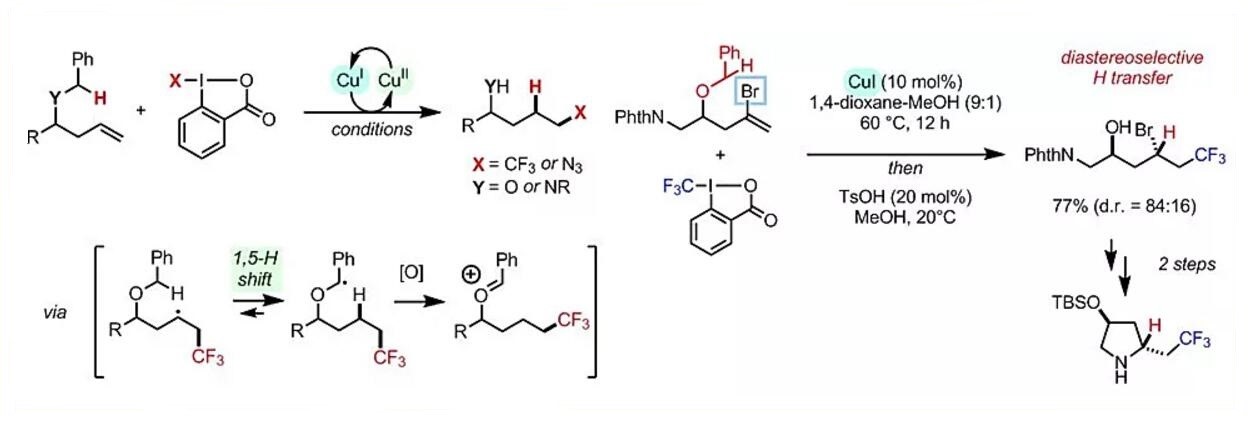
Gagosz教授利用氧化还原条件下的自由基化学,来发展涉及中间氢转移步骤的转化和对实现烯烃区域和非对映选择性氢官能团化的反应21-23(Scheme 7)。
Scheme 7自由基氢转移
参考文献
- [1] Revol, G., McCallum, T., Morin, M., Gagosz, F. & Barriault, L.Photoredox Transformations with Dimeric Gold Complexes. Angew. Chem. Int. Ed. (2013) 52, 13342-13345, doi:10.1002/anie.201306727.
- [2] Henrion, G., Chavas, T. E. J., Le Goff, X. & Gagosz, F.Biarylphosphonite Gold(I) Complexes as Superior Catalysts for Oxidative Cyclization of Propynyl Arenes into Indan-2-ones. Angew. Chem. Int. Ed. (2013) 52, 6277-6282, doi:10.1002/anie.201301015.
- [3] Escalle, A., Mora, G., Gagosz, F., Mézailles, N., Le Goff, X. F., Jean, Y. & Le Floch, P.Cationic Dimetallic Gold Hydride Complex Stabilized by a Xantphos-Phosphole ligand: Synthesis, X-ray Crystal Structure, and Density Functional Theory Study. Inorganic Chemistry (2009) 48, 8415-8422, doi:10.1021/ic901014r.
- [4] Zhao, Q., León Rayo, D. F., Campeau, D., Daenen, M. & Gagosz, F.Gold-Catalyzed Formal Dehydro-Diels–Alder Reactions of Ene-Ynamide Derivatives Bearing Terminal Alkyne Chains: Scope and Mechanistic Studies. Angew. Chem. Int. Ed. (2018) 57, 13603-13607, doi:10.1002/anie.201807136.
- [5] Cao, Z. & Gagosz, F.Gold-Catalyzed Tandem Cycloisomerization/Cope Rearrangement: An Efficient Access to the Hydroazulenic Motif. Angew. Chem. Int. Ed. (2013) 52, 9014-9018, doi:10.1002/anie.201304497.
- [6] Bolte, B. & Gagosz, F.Gold and Brønsted Acid Catalyzed Hydride Shift onto Allenes: Divergence in Product Selectivity. J. Am. Chem. Soc. (2011) 133, 7696-7699, doi:10.1021/ja202336p.
- [7] Buzas, A. K., Istrate, F. M. & Gagosz, F.Gold(I)-Catalyzed 5-endo Hydroxy- and Alkoxycyclization of 1,5-Enynes: Efficient Access to Functionalized Cyclopentenes. Angew. Chem. Int. Ed. (2007) 46, 1141-1144, doi:10.1002/anie.200604140.
- [8] Mézailles, N., Ricard, L. & Gagosz, F.Phosphine Gold(I) Bis-(trifluoromethanesulfonyl)imidate Complexes as New Highly Efficient and Air-Stable Catalysts for the Cycloisomerization of Enynes. Org. Lett. (2005) 7, 4133-4136, doi:10.1021/ol0515917.
- [9] Lonca, G. H., Tejo, C., Chan, H. L., Chiba, S. & Gagosz, F.Gold(i)-catalyzed 6-endo-dig azide–yne cyclization: efficient access to 2H-1,3-oxazines. Chem. Commun. (2017) 53, 736-739, doi:10.1039/C6CC08397H.
- [10] Gronnier, C., Bel, P. F. d., Henrion, G., Kramer, S. & Gagosz, F.Divergent Product Selectivity in Gold- versus Silver-Catalyzed Reaction of 2-Propynyloxy-6-fluoropyridines with Arylamines. Org. Lett. (2014) 16, 2092-2095, doi:10.1021/ol500939v.
- [11] Prechter, A., Henrion, G., Faudot dit Bel, P. & Gagosz, F.Gold-Catalyzed Synthesis of Functionalized Pyridines by Using 2H-Azirines as Synthetic Equivalents of Alkenyl Nitrenes. Angew. Chem. Int. Ed. (2014) 53, 4959-4963, doi:10.1002/anie.201402470.
- [12] Gronnier, C., Boissonnat, G. & Gagosz, F.Au-Catalyzed Formation of Functionalized Quinolines from 2-Alkynyl Arylazide Derivatives. Org. Lett. (2013) 15, 4234-4237, doi:10.1021/ol4019634.
- [13] Wetzel, A. & Gagosz, F.Gold-Catalyzed Transformation of 2-Alkynyl Arylazides: Efficient Access to the Valuable Pseudoindoxyl and Indolyl Frameworks. Angew. Chem. Int. Ed. (2011) 50, 7354-7358, doi:10.1002/anie.201102707.
- [14] Kramer, S., Odabachian, Y., Overgaard, J., Rottländer, M., Gagosz, F. & Skrydstrup, T.Taking Advantage of the Ambivalent Reactivity of Ynamides in Gold Catalysis: A Rare Case of Alkyne Dimerization. Angew. Chem. Int. Ed. (2011) 50, 5090-5094, doi:10.1002/anie.201100327.
- [15] Gandamana, D. A., Wang, B., Tejo, C., Bolte, B., Gagosz, F. & Chiba, S.Alkyl Ethers as Traceless Hydride Donors in Brønsted Acid Catalyzed Intramolecular Hydrogen Atom Transfer. Angew. Chem. Int. Ed. (2018) 57, 6181-6185, doi:10.1002/anie.201801953.
- [16] Wang, B., Gandamana, D. A., Gagosz, F. & Chiba, S.Diastereoselective Intramolecular Hydride Transfer under Brønsted Acid Catalysis. Org. Lett. (2019) 21, 2298-2301, doi:10.1021/acs.orglett.9b00590.
- [17] Boreux, A., Lonca, G. H., Riant, O. & Gagosz, F.Synthesis of Trifluoromethyl-allenes by Gold-Catalyzed Rearrangement of Propargyl Benzyl Ethers. Org. Lett. (2016) 18, 5162-5165, doi:10.1021/acs.orglett.6b02636.
- [18] Bolte, B., Odabachian, Y. & Gagosz, F.Gold(I)-Catalyzed Rearrangement of Propargyl Benzyl Ethers: A Practical Method for the Generation and in Situ Transformation of Substituted Allenes. J. Am. Chem. Soc. (2010) 132, 7294-7296, doi:10.1021/ja1020469.
- [19] Jurberg, I. D., Odabachian, Y. & Gagosz, F.Hydroalkylation of Alkynyl Ethers via a Gold(I)-Catalyzed 1,5-Hydride Shift/Cyclization Sequence. J. Am. Chem. Soc. (2010) 132, 3543-3552, doi:10.1021/ja9100134.
- [20] Buzas, A. & Gagosz, F.Gold(I) Catalyzed Isomerization of 5-en-2-yn-1-yl Acetates: An Efficient Access to Acetoxy Bicyclo[3.1.0]hexenes and 2-Cycloalken-1-ones. J. Am. Chem. Soc. (2006) 128, 12614-12615, doi:10.1021/ja064223m.
- [21] Boreux, A., Indukuri, K., Gagosz, F. & Riant, O.Acyl Fluorides as Efficient Electrophiles for the Copper-Catalyzed Boroacylation of Allenes. ACS. Catal. (2017) 7, 8200-8204, doi:10.1021/acscatal.7b02938.
- [22] Lonca, G. H., Ong, D. Y., Tran, T. M. H., Tejo, C., Chiba, S. & Gagosz, F.Anti-Markovnikov Hydrofunctionalization of Alkenes: Use of a Benzyl Group as a Traceless Redox-Active Hydrogen Donor. Angew. Chem. Int. Ed. (2017) 56, 11440-11444, doi:10.1002/anie.201705368.
- [23] Gronnier, C., Kramer, S., Odabachian, Y. & Gagosz, F.Cu(I)-Catalyzed Oxidative Cyclization of Alkynyl Oxiranes and Oxetanes. J. Am. Chem. Soc. (2012) 134, 828-831, doi:10.1021/ja209866a.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!



























No comments yet.