导读:
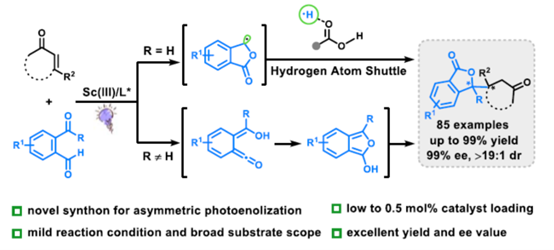
近日,四川大学的冯小明等课题组在J. Am. Chem. Soc.中发表论文,首次报道一种全新的邻苯二甲醛(OPA)与邻苯甲酰基苯甲醛(OBBA)的直接不对称光环化异构化反应,该反应随后与α,β-不饱和羰基化合物发生1,4-共轭加成,以优异产率及非对映/对映选择性合成多种手性内酯。值得注意的是,微量羧酸通过氢原子穿梭机理显著加速反应,实现低催化剂负载量(0.5 mol%)。机理研究(光谱分析、氘代标记、EPR及对照实验)证实该催化循环路径与传统光烯醇化路径不同。
Photoinitiated Enantioselective Cycloisomerization/Addition Cascades of 2‑Acyl Benzaldehydes with α,β-Unsaturated Carbonyl Compounds
J. Wu, L. Yang, X. Lu, F. Li, Y. Mo, W. Cao, X. Liu, X. Feng, J. Am. Chem. Soc. 2026 ASAP. doi: 10.1021/jacs.6c00267.
正文:
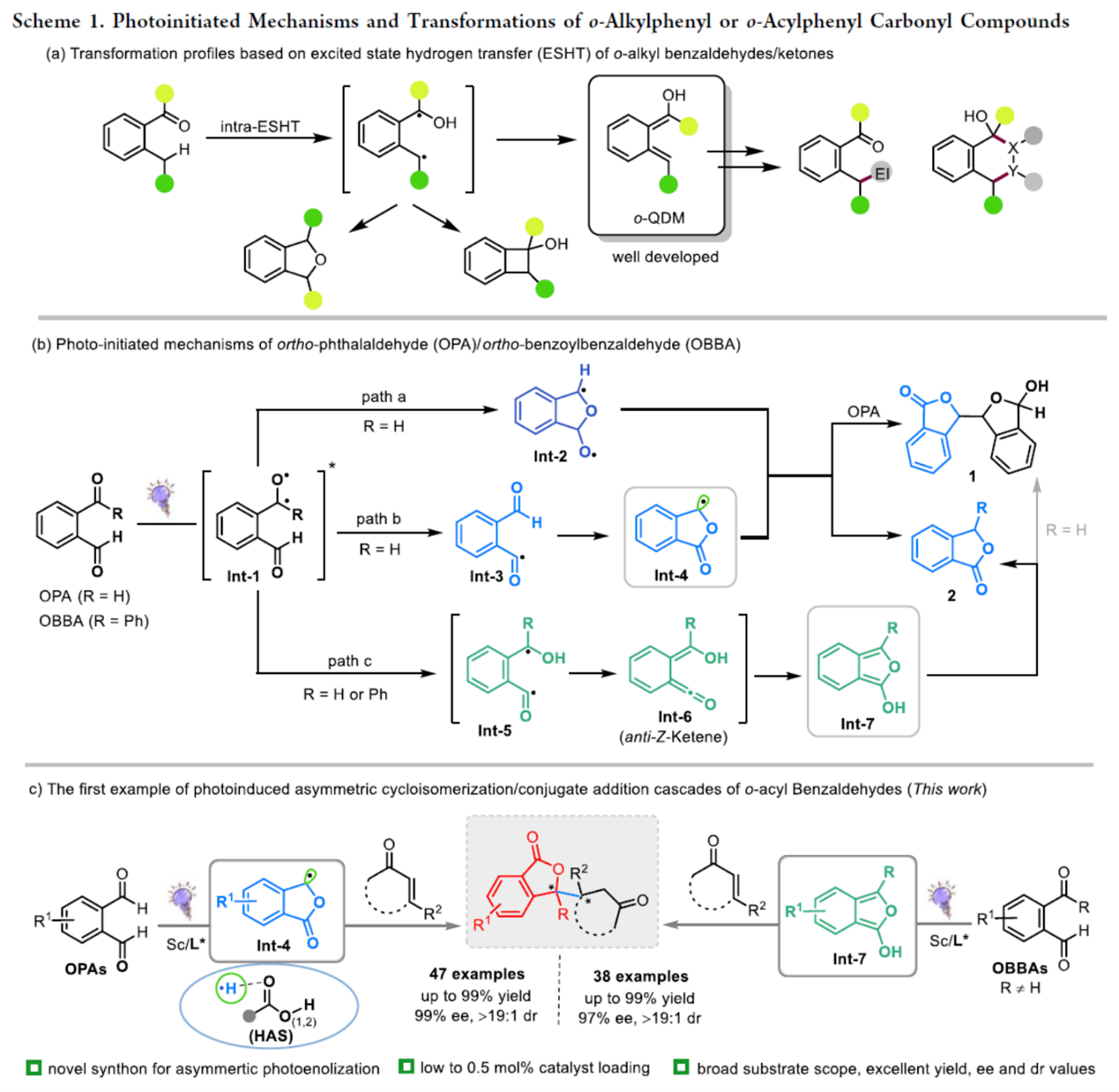
光化学反应为有机合成提供了稳健且强大的平台,极大地丰富了化合物家族的转化类型。羰基化合物(尤其是醛酮类化合物)不仅是传统有机合成的基础性重要原料,在有机光化学领域同样发挥着关键作用。其中,邻烷基苯甲醛及邻烷基二苯甲酮通过激发态分子内氢转移过程(intra-ESHT)发生光烯醇化反应,形成羟基邻醌二甲烷(o-QDM)中间体,是此类反应的典型范例。此外,光化学反应平台在促进转化反应(包括亲核加成、环加成)及生物活性天然产物合成方面受到特别关注[1](Scheme 1a)。值得注意的是,邻氨基二苯甲酮同样可发生光烯醇化反应。
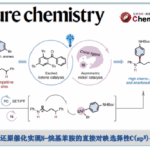
邻苯二甲醛(OPA)与邻苯甲酰基苯甲醛(OBBA)是最简单的芳香二羰基化合物。尽管OPA因其与亲核试剂的反应性已备受关注逾一个世纪,但其跃迁至n−π*激发态后的详细反应机理仍是当前争议焦点[2−4](Scheme 1b)。目前已提出三种不同反应路径,分别涉及通过不同过程生成的关键中间体:分子内氧自由基加成形成Int-2(Scheme 1b, path a)[2];Norrish I型C−H键断裂产生内酯自由基Int-4(Scheme 1b, path b)[3];以及不可逆光烯醇化生成环状烯醇中间体Int-7(Scheme 1b, path c)[4]。这些反应路径最终生成二聚体(1)或环化异构化产物苯酞(2)。相比之下,通过激光闪光光解、计算化学及瞬态吸收光谱学研究,已明确邻苯甲酰基苯甲醛(OBBA)的光化学行为:其激发路径(path c)经由中间体Int-7,专一性生成3-取代苯酞(2)。尽管取得了上述的研究,但基于OPA/OBBA的转化探索,尤其在手性内酯衍生物的不对称合成领域,仍未得到充分发展。近日,四川大学的冯小明等课题组首次报道一种全新的利用手性钪(III) Lewis酸催化剂,实现了OPA与OBBA的对映选择性光驱动环化异构化/加成串联反应,成功构建含密集手性中心的手性内酯骨架,并具有高收率与优异的非对映/对映选择性(Scheme 1c)。
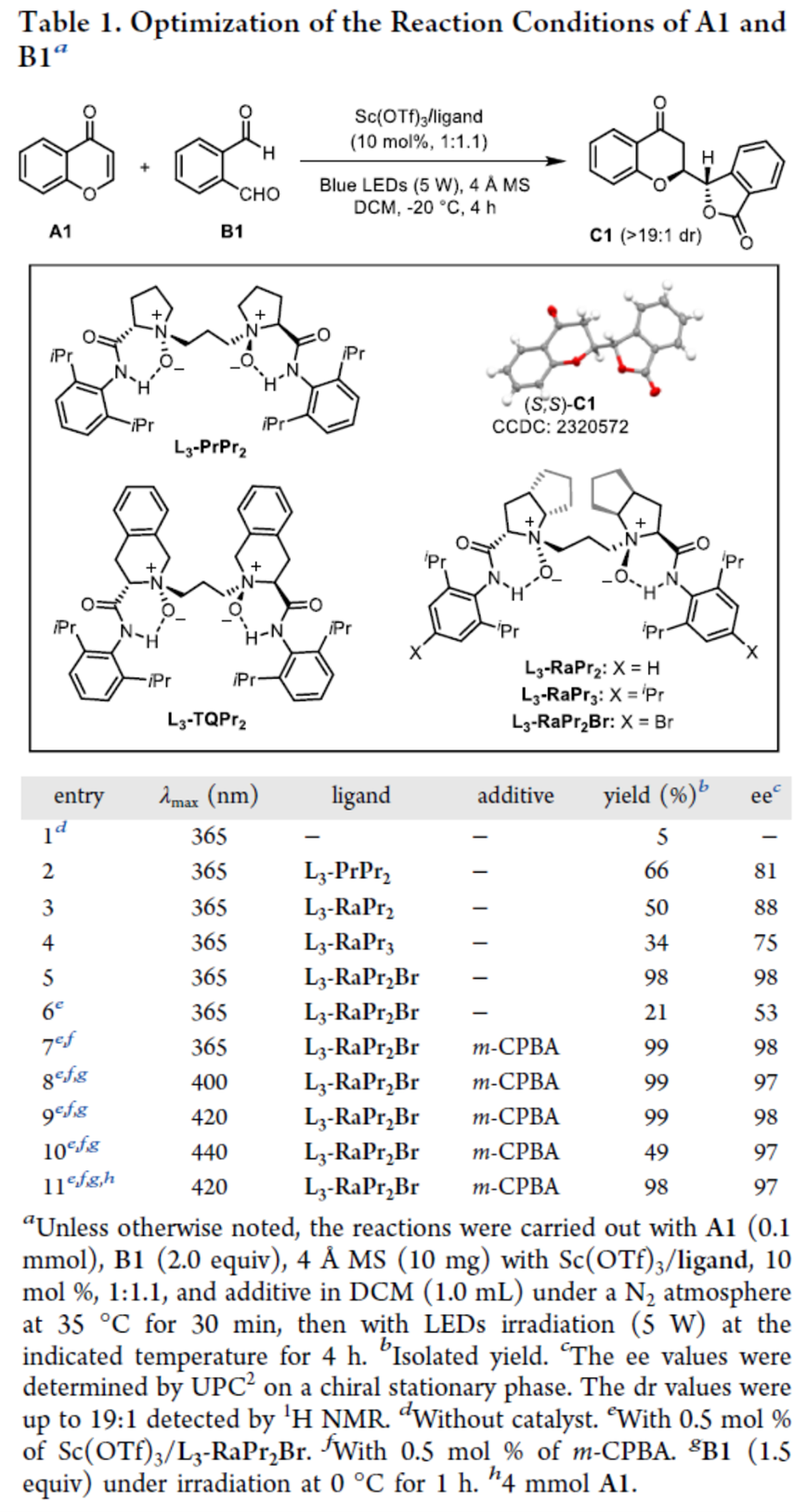
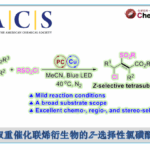
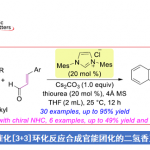
首先,作者采用4H-色烯-4-酮(A1)与邻苯二醛(B1)作为模型底物,进行相关反应条件的优化筛选(Table 1)。进而确定最佳的反应条件为:采用Sc(OTf)3作为催化剂,L3-RaPr2Br作为手性配体,m-CPBA作为添加剂,蓝色LED(λ = 420 nm, 5 W)作为光源,在DCM反应溶剂中,最终获得99%收率的产物C1(98% ee)。
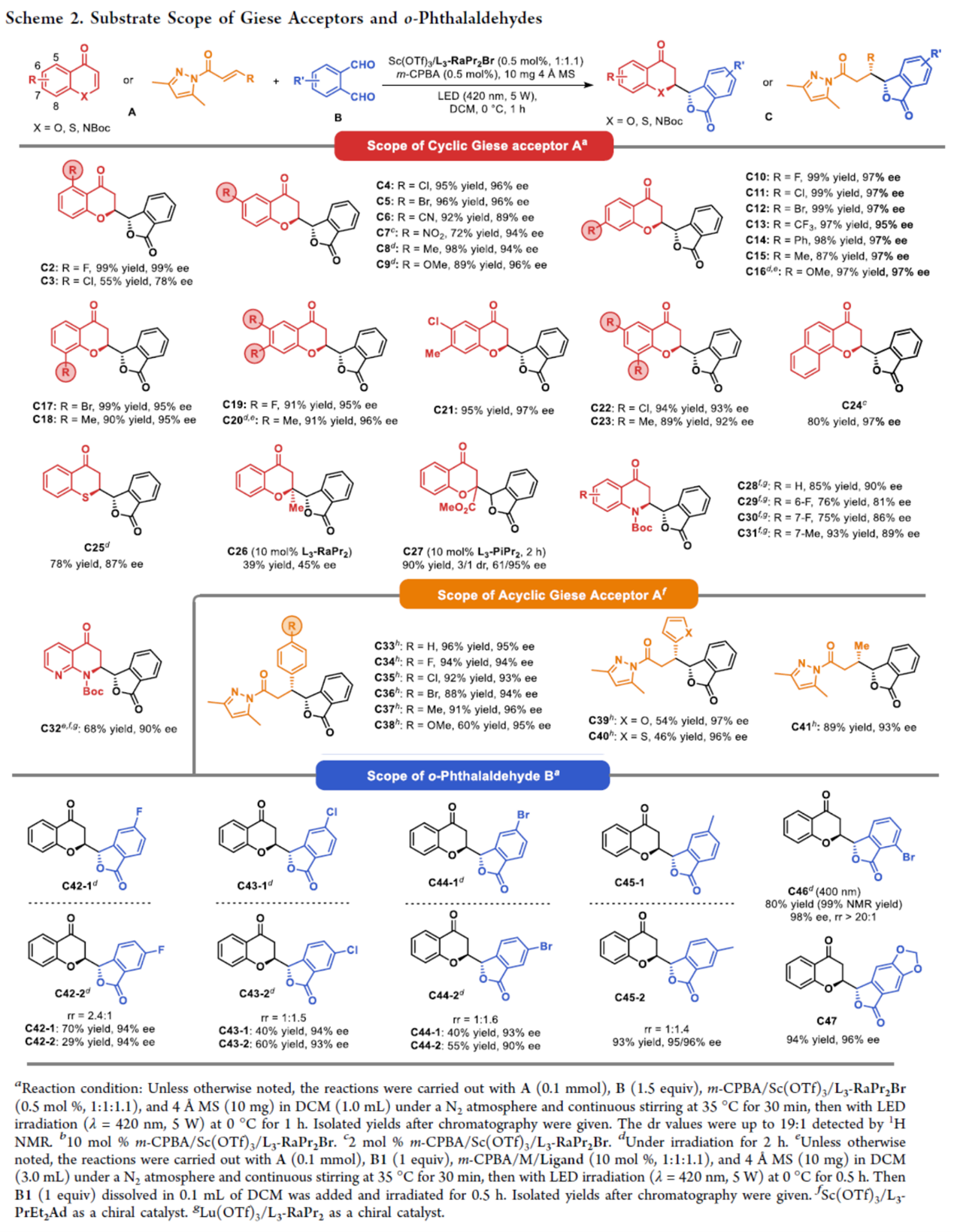
在上述的最佳反应条件下,作者分别对一系列Giese受体与邻苯二甲醛的底物范围进行了深入研究(Scheme 2)。首先,在5-至8-位上含有吸电子或供电子取代基的色酮类衍生物与二取代色酮衍生物,均可顺利进行反应,获得相应的产物C2–C23,收率为55-99%,ee为78-99%。4H-苯并[h]色烯-4-酮和4H-硫代色烯-4-酮反应,也是合适的底物,如C24与C25。2-甲基取代色酮,可能由于位阻效应,导致反应结果较差,如C26。同时,在配体L3-PiPr3的作用下,2-甲酯色酮成功转化为目标产物C27,且产率高、对映体选择性良好、非对映体选择性适中。通过对反应条件的优化后发现,在Sc(OTf)3/L3-PrEt2Ad或Lu(OTf)3/L3-RaPr2催化体系下,N-Boc喹诺酮类化合物,也能够进行反应,获得相应的产物C28–C32,收率为68-85%,ee为81-90%。其次,在Lu(OTf)3/L3−RaPr2催化体系下,非环状α,β-不饱和酰基吡唑衍生物,也与体系兼容,获得相应的产物C33–C41,收率为46-96%,ee为93-97%。此外,不同取代的邻苯二甲醛,也能够顺利进行反应,获得相应的产物C42–C47。其中,仅有3-溴邻苯二醛具有很高的区域选择性,如C46。
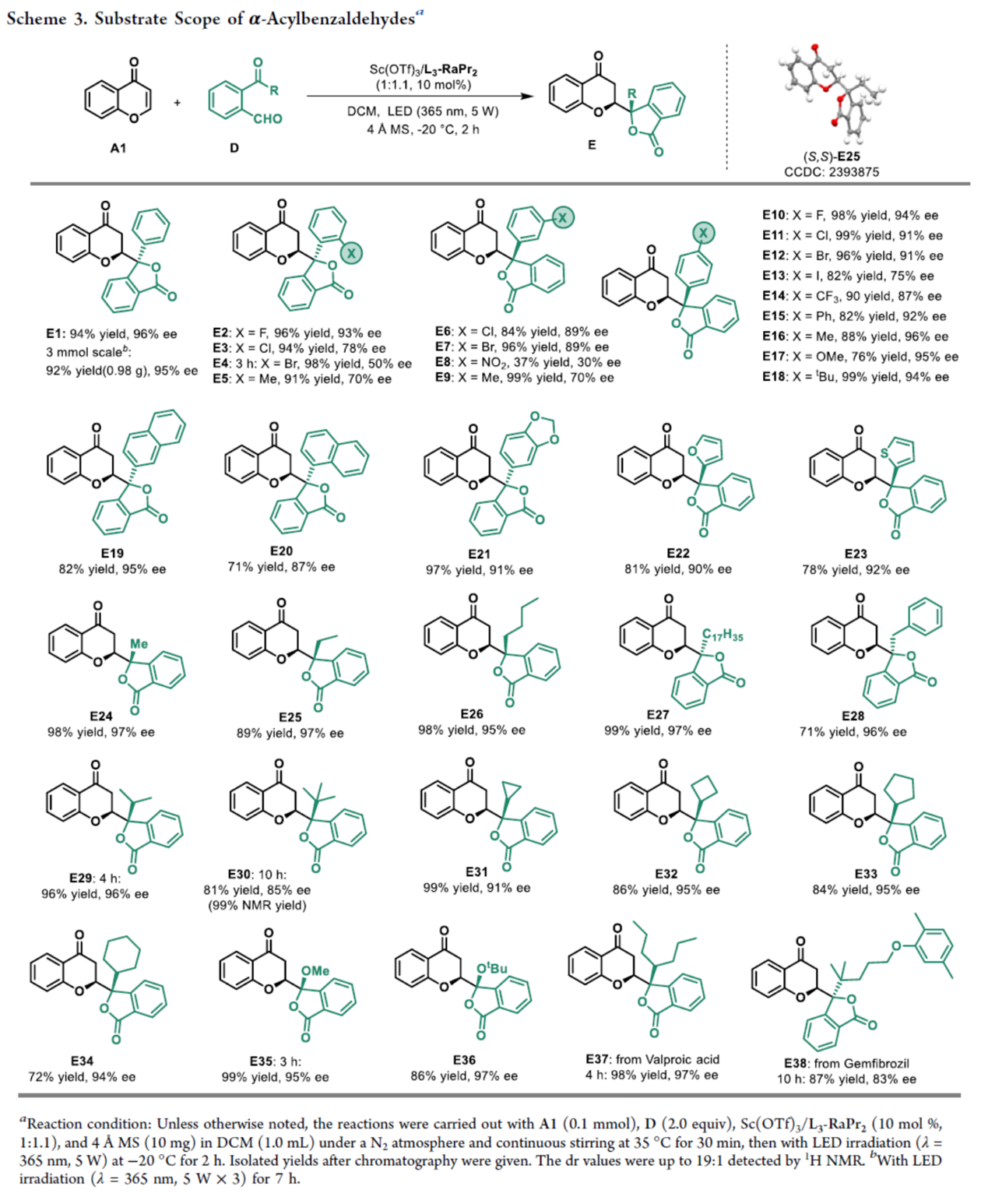
紧接着,作者对α-酰基苯甲醛的底物范围进行了扩展(Scheme 3)。研究结果表明,当α-酰基苯甲醛底物中的R为不同电性取代的芳基、萘基、杂芳基、烷基、环烷基等时,均可顺利进行反应,获得相应的产物E1–E38,收率为37-99%,ee为30-97%。同时,该策略也可用于天然产物以及药物分子的后期衍生化,如E37和E38。
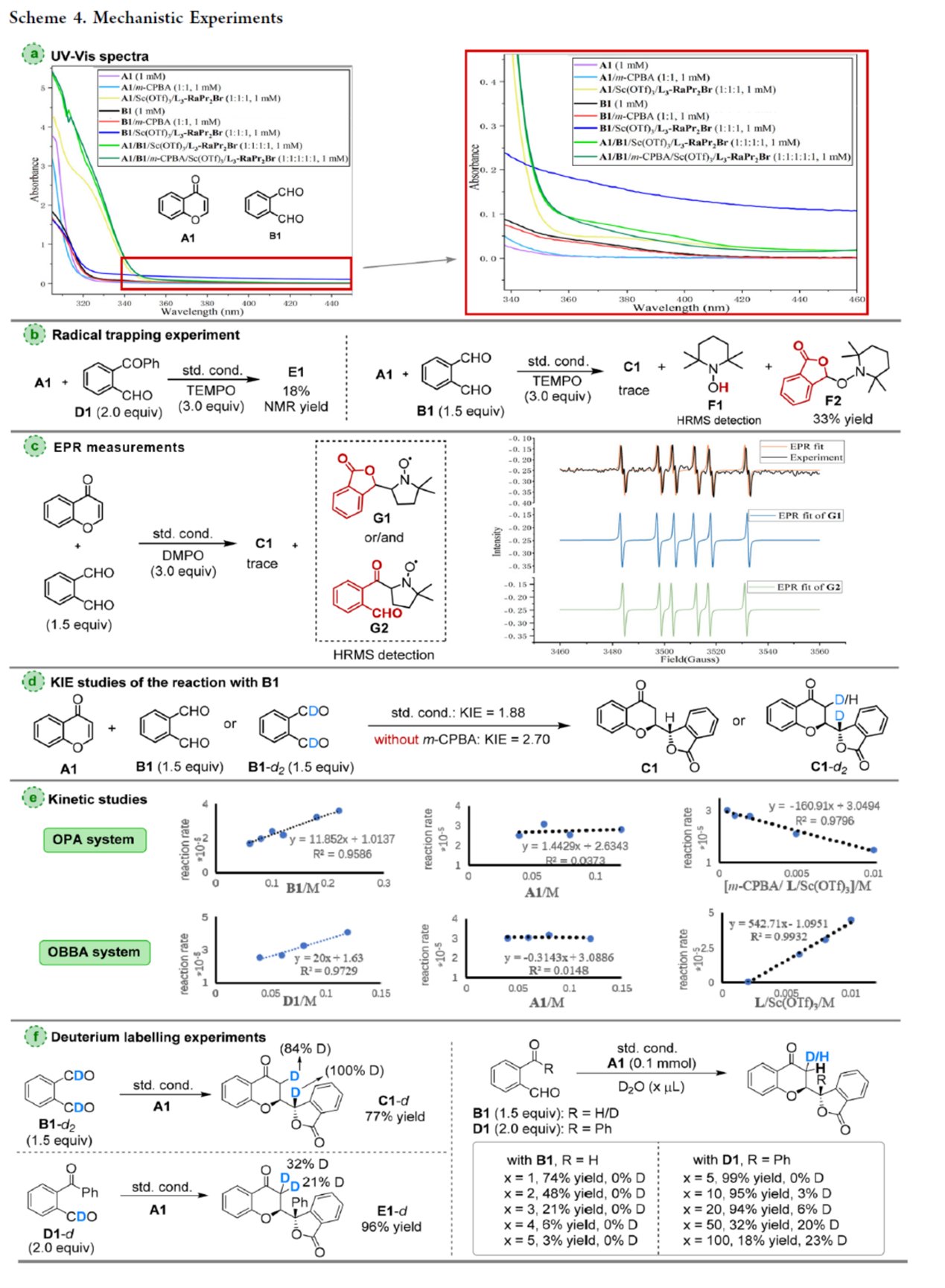
接下来,作者对反应的机理进行进一步研究(Scheme 4)。首先,UV−vis光谱研究表明,催化剂Sc(OTf)3/L3-RaPr2Br与底物A1和B1之间存在配位相互作用(Scheme 4a)。自由基捕获实验结果表明,B1与D1内酯配合物存在差异,且光是内酯自由基形成的关键因素(Scheme 4b)。EPR实验结果表明,反应涉及内酯自由基和酰基自由基的形成(Scheme 4c)。其次,KIE实验结果表明,m-CPBA能促进C−H键断裂,并降低C1形成的反应能障(Scheme 4d)。动力学研究研究结果表明,对于这两种反应,共轭加成步骤均不涉及速率决定步骤(Scheme 4e)。此外,氘代实验结果表明,氢转移步骤中的氢源来自于醛(Scheme 4f)。同时,可推测痕量水参与了质子转移过程,且实验证实外源性重水中的氘可掺入产物E1。
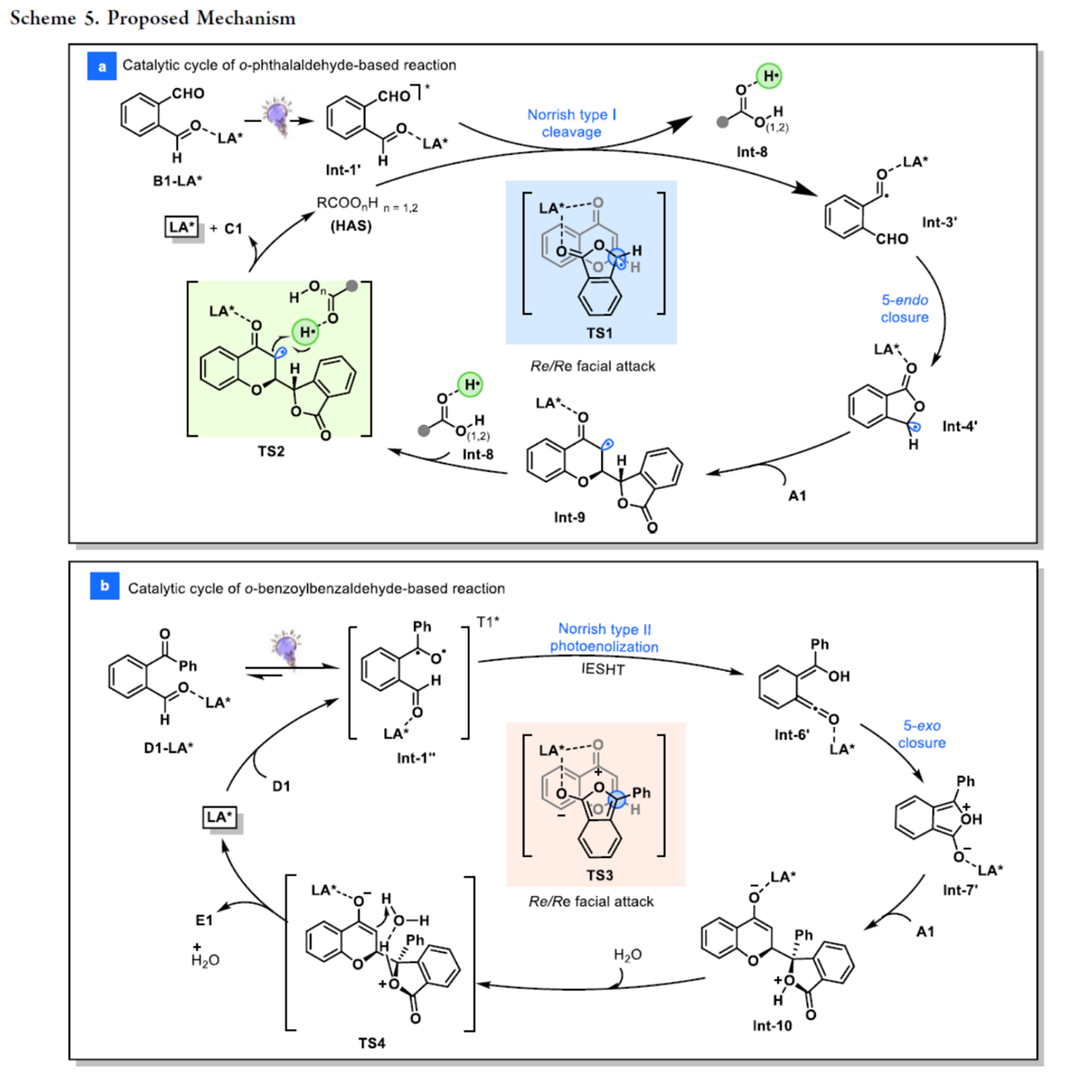
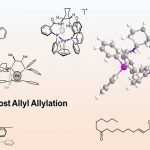
基于上述的实验研究,作者提出如下邻苯二甲醛(OPA)与邻苯甲酰苯甲醛(OBBA)参与的两种独立过程,即自由基加成与极性加成反应机理(Scheme 5)。在OPA反应路径中(Scheme 5a),可见光驱动的Norrish I型断裂激发态B1-LA*配合物在羧酸添加剂作用下攫取氢原子,生成2-甲酰基苯甲酰自由基Int-3′。自由基Int-3′经5-endo环化形成亲核自由基Int-4′,其与色酮反应产生自由基加合物Int-9。其次,Int-8作为氢供体通过过渡态TS2生成产物C1,并释放酸/催化剂。对映选择性决速步为自由基加成过渡态TS1,其优先经Re−Re面进攻生成(S,S)-构型产物C1;实验测得量子产率Φ=0.126,排除链式反应机制。在OBBA反应路径中(Scheme 5b),D1的转化遵循Norrish II型光烯醇化路径:在手性Lewis酸催化剂及光照下,经双自由基物种旋转与系间窜越(ISC)形成三重态激发中间体Int-1″,再通过1,5-氢转移生成Int-6′。随后,经内酯化产生Int-7′,并与色酮经过渡态TS3发生Michael加成,其中手性Lewis酸催化剂将这两种物质结合在一起,进行Re−Re面进攻形成加合物Int-10。中间体Int-10在体系痕量水辅助下质子化(TS4),最终释放目标产物(S,S)-产物E1及催化剂。
总结
四川大学的冯小明等课题组首次报道了利用邻甲酰基苯甲醛/酮作为光烯醇前体,在不添加光催化剂的条件下,通过手性N,N′-二氧化物配体的钪基Lewis酸催化,实现不对称光环化/加成反应,高效合成多种手性内酯衍生物。该策略具有广谱底物适用性与卓越催化效率,可在较短时间内以优异收率和对映选择性获得一系列产物。对照实验和光谱学研究表明,反应机理与2-酰基苯甲醛的光化学性质密切相关。尤其发现羧酸衍生物可作为氢原子梭,加速邻甲酰基苯甲醛内酯化形成自由基中间体,从而将催化剂载量突破性降至0.5 mol%。
参考文献:
[1] S. Cuadros, P. Melchiorre, Eur. J. Org. Chem. 2018, 2018, 2884. doi:10.1002/ejoc.201800081.
[2] J. Kagan, Tetrahedron Lett. 1966, 7, 6097. doi:10.1016/S0040-4039(00)70147-X.
[3] D. A. Harrison, R. N. Schwartz, J. Kagan, J. Am. Chem. Soc. 1970, 92, 5793. doi:10.1021/ja00722a072.
[4] J. C. Scaiano, M. V. Encinas, M. V. George, 1980, 2, 724. doi:10.1039/P29800000724.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
关注Chem-Station抖音号:79473891841
请登陆TCI试剂官网查看更多内容
https://www.tcichemicals.com/CN/zh/
















No comments yet.