作者:石油醚
导读
近日,曼彻斯特大学Nicholas J. Turner教授团队在J. Am. Chem. Soc.上发表了题为 [ Biocatalytic Production of a Key Chiral Intermediate of the HIV Capsid Inhibitor Lenacapavir ] 论文。Turner教授采用底物步进策略,从无活性的Ruegeria sp. TM1040 ATA亲本出发,经八轮定向进化获得高性能变体,成功实现了酮底物5的转氨化获得Lenacapavir核心手性胺(S)-5a。
“Biocatalytic Production of a Key Chiral Intermediate of the HIV Capsid Inhibitor Lenacapavir
Grayson J. Ford, Christopher J. Taylor, Amy E. Hutton, William R. Birmingham, Fei Zhao, Zefei Xu, William Finnigan, Mary Ortmayer, Colin W. Levy, Mark S. Dunstan, Rebecca Crawshaw, Ian Rowles, Anthony P. Green,* and Nicholas J. Turner*
Dongchen CaiYunfei HuangTongyin ChenSiqi LiuXiao Xiao*Baoguo Zhao*
J. Am. Chem. Soc.2026, ASAP. DOI: 10.1021/jacs.6c02519
正文:
Lenacapavir (1)(Sunlenca®,)是由Gilead Sciences研发的全球首个获批的HIV衣壳抑制剂,用于治疗及预防HIV感染。其半衰期长、清除率低、药效强,实现每半年一次注射即可提供近100%的PrEP保护效果。为加速可及性,Gilead Sciences已向六家制造商授予免版税许可,支持向120个低收入国家供应仿制药。但API生产成本高昂,仍是普及的主要障碍,亟需更低成本的合成工艺。
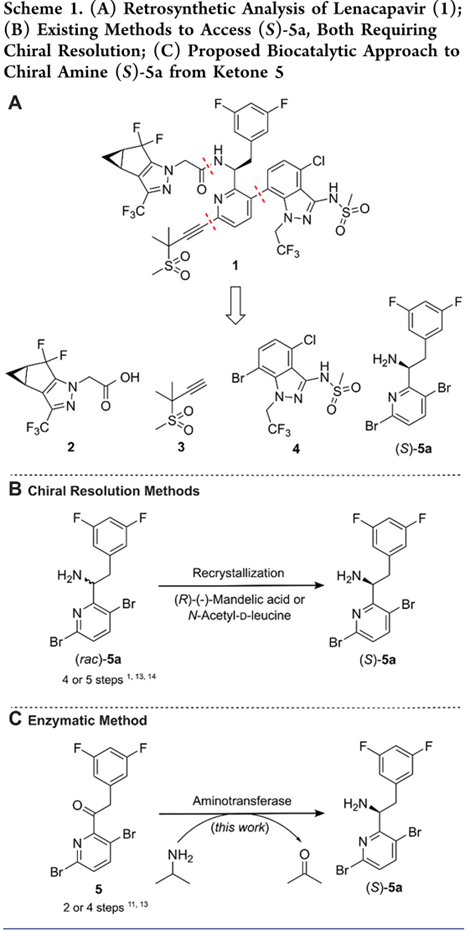
对Lenacapavir (1) 逆合成分析可切分为四个砌块:2、3、4 和(S)-5a(Scheme 1A)。近些年来,各砌块的化学合成已有进展,聚焦于可放大、低成本的中间体/前体路线。但(S)-5a仍依赖两步法:先制备外消旋胺(rac)-5a,再通过与(R)-扁桃酸或N-乙酰-D-亮氨酸共结晶实现动态动力学拆分(Scheme 1B),耗时长、效率低。鉴于生物催化在可持续API生产中日益重要,尤其适用于含手性胺的分子。
目前,转移酶(ATAs)已广泛应用于工业规模S/R-胺的合成,并成功用于多种API生产。但其对大位阻酮(尤其在高底物浓度下)通常活性不足,需深度工程改造。文献调研证实,酮5是迄今报道中位阻最大、最具挑战性的ATA催化底物之一。加之溶解性差,使其成为极具难度的酶工程靶点。近日,曼彻斯特大学Nicholas J. Turner教授报道一种工程化转氨酶(ATA)的开发:针对位阻极大的酮底物5,采用底物步进策略,从无活性的Ruegeria sp. TM1040 ATA亲本出发,经八轮定向进化获得高性能变体。该酶在近工艺条件下实现>98%转化率、>90%分离收率和>99% ee,高效合成lenacapavir核心手性胺(S)-5a。相关工作发表于“J. Am. Chem. Soc.”上。
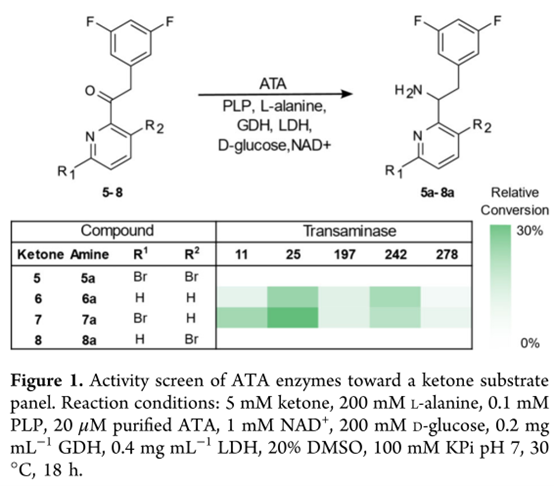
首先,作者以L-丙氨酸为胺供体、结合丙酮酸清除系统,对400余种ATA进行初筛表明未获得任何可检测的反应活性。然而,多种ATA对结构类似物酮6和7(吡啶环上缺失一个或两个溴)表现出活性(Figure 1);而对仅含邻位5-Br取代的酮8则完全无活性,进而表明该取代模式是ATA催化的关键位阻瓶颈。所有筛选的酶中,TA25(此前报道为3FCR-QM-W59L28,30)对6→6a和7→7a的转化率最高(Figure 1)。基于此,以TA25作为起点,通过底物行走的策略开展四轮定向进化(Figure 2):每轮基于理性选择标准,对14–24个位点用NNK密码子随机化;文库变体以96孔板形式表达,采用澄清裂解液+UPLC法实时监测转化率;各轮有益突变经组合建库,最优变体作为下一轮模板。
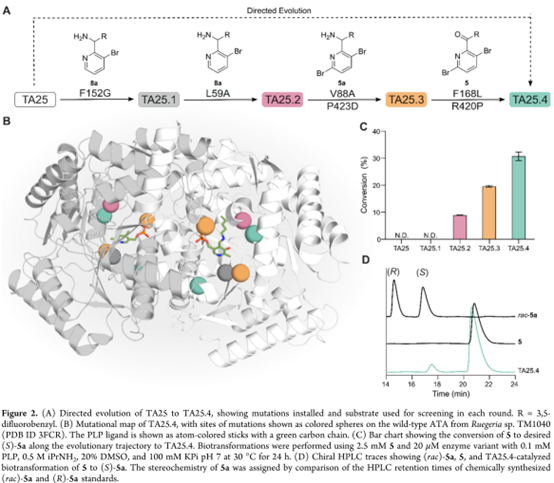
其中,第1–2轮采用脱氨基模式筛选:以(rac)-8a为底物、丙酮酸为胺受体(原始模板对此无活性;Figure 2A)。F152G单点突变(第1轮)赋予TA25.1对8a的微弱活性(Figure 2A,B);该位点虽已知参与PLP结合,但此处F152G是解锁大位阻胺8a活性的关键。L59A突变(第2轮)首次在纯化蛋白中实现酮5的胺化(Figure 2C),虽活性过低无法在裂解液中检出,但其逆反应5a的脱氨基可被检测,故将5a用作第3轮筛选底物(Figure 2A,S2)。 V88A与P423D双突变生成TA25.3,在澄清裂解液中即显示酮5胺化的可测活性,使第4轮起可直接在目标胺合成方向筛选。胺供体选用异丙胺(iPrNH₂):成本低、易去除,且已在工程ATA工艺中验证。四轮进化终获TA25.4(含6个突变),在近工艺条件下(2.5 mM 酮5,0.8 mol% 酶,24 h)实现31%转化率(Figure 2C),且立体选择性优异(>99% ee,得(S)-5a;Figure 2D)
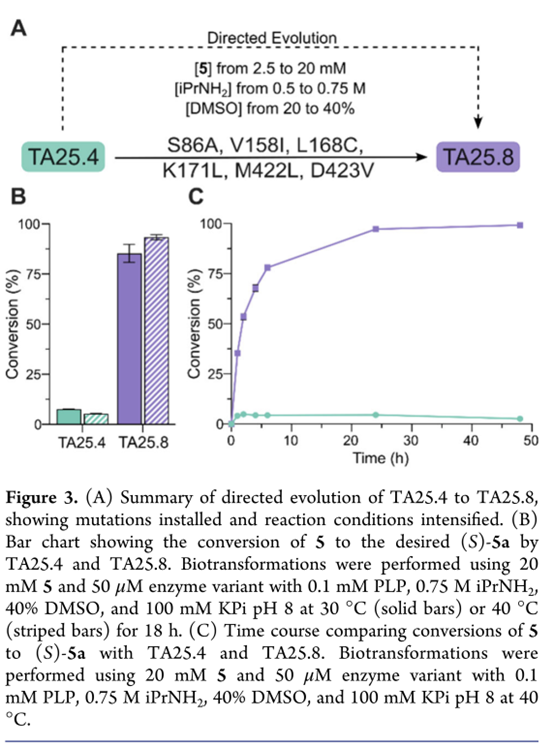
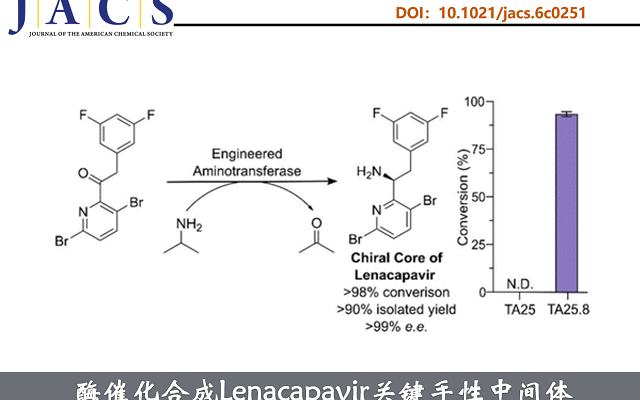
接下来,对商业化工艺进行开发。为此开展四轮定向进化(第5–8轮),每轮对18–47个位点进行NNK随机化,并同步强化反应苛刻度:底物5浓度由2.5 mM(1.0 g/L)梯度提升至20 mM(7.8 g/L);DMSO共溶剂由20%增至40%以改善溶解性;异丙胺供体由0.5 M升至0.75 M(图3A)。经筛选>12,000个变体,获得含有10个突变体的TA25.8其中5个突变位点与机器学习指导的3FCR大位阻底物优化研究重合,但除S86A外,其余突变均不同。进一步,在30°C、20 mM底物负载下,TA25.8(0.25 mol%)18 h转化率达86%,而TA25.4仅8%(Figure 3B)。更关键的是,TA25.8在40°C仍保持高效(18 h转化率94%;Figure 3B),热稳定性显著提升(Tm:57°C→65°C),操作稳定性亦增强(Figure 3B,C)。此外,TA25.8还耐受50 mM高底物浓度,18 h内以0.25 mol%酶量实现65%转化。最终,在制备级转化中(0.25 mol%纯酶),成功获得453 mg lenacapavir前体(S)-5a(98%转化率,90%分离收率,>99% ee)。
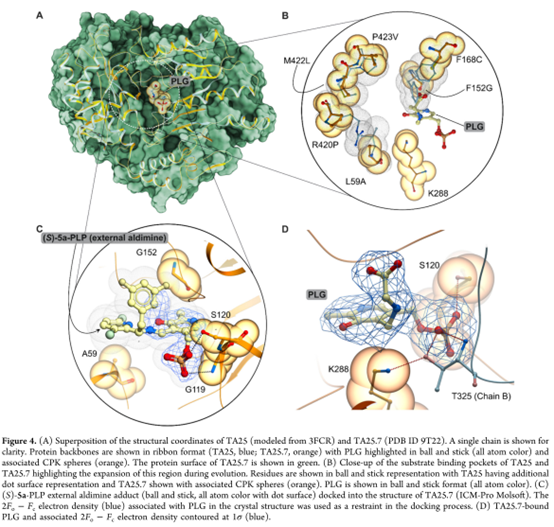
最后,作者通过解析工程化变体TA25.7(PDB ID 9T22)的晶体结构,进一步解释定向进化赋予ATA对底物5的活性。TA25.7与野生型Ruegeria sp. TM1040 ATA(PDB ID 3FCR)主链高度保守(全局RMSD = 0.2 Å),PLP辅因子结合位点几乎无变化(Figure 4A)。结构中辅因子以N-吡哆醛-甘氨酸-5′-单磷酸(PLG)加合物形式存在(Figure 4D),系PLP与结晶缓冲液中甘氨酸自发缩合所致。 结构比对表明:早期引入的F152G和L59A突变协同扩大底物口袋(Figure 4B);后期添加的L168C与M422L进一步拓展活性位点体积。为解析(,进一步构建TA25.7–(S)-5a-PLP外部醛亚胺复合物模型来解析S)-5a结合模式(Figure 4C)。结果显示:二溴吡啶基团嵌入L59A形成的空腔,二氟苯基则占据F152G诱导扩大的疏水口袋;PLP部分构象与晶体中PLG高度一致。
总结
Nicholas J. Turner教授采用底物步进策略,从无活性的Ruegeria sp. TM1040 ATA亲本出发,经八轮定向进化获得高性能变体,成功实现了酮底物5的转氨化获得Lenacapavir核心手性胺(S)-5a。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
关注Chem-Station抖音号:79473891841
请登陆TCI试剂官网查看更多内容
https://www.tcichemicals.com/CN/zh/




















No comments yet.