本文作者:杉杉
导读
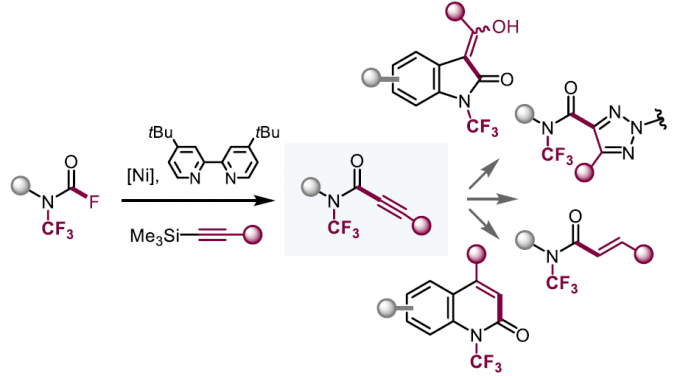
近日,德国RWTH Aachen大学F. Schoenebeck课题组在J. Am. Chem. Soc.中发表论文,首次报道一种采用镍催化的N-CF3氨基甲酰氟 (carbamoyl fluoride)与炔基硅烷之间的偶联反应方法学,进而成功实现一系列N-CF3炔酰胺及其衍生物 (alkynamides)的合成。这一全新的偶联策略具有操作简单、反应条件温和等优势。同时,通过后期的衍生化过程,能够获得一系列目前仍难以合成的重要分子,例如烯基酰胺、羟吲哚或喹诺酮等。
Synthesis of N‑CF3 Alkynamides and Derivatives Enabled by Ni-Catalyzed Alkynylation of N‑CF3 Carbamoyl Fluorides
C. D. T. Nielsen, F. G. Zivkovic, F. Schoenebeck, J. Am. Chem. Soc. ASAP. doi: 10.1021/jacs.1c07780.
正文
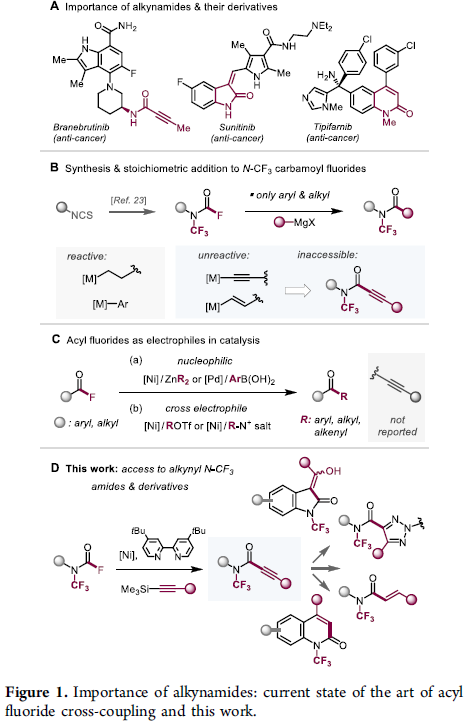
酰胺与炔基化合物是化学、生物学以及材料科学中的两种最为核心的结构单元。通过二者结合产生的炔酰胺骨架同样具有较为重要的应用价值。炔酰胺骨架具有良好的生物活性,能够应用于各类抗癌药物的研究,例如Branebrutinib (Figure 1A)。而且,炔酰胺化合物同样能够作为材料化学中的关键合成前体以及药物化学研究中重要的替代性骨架单元。同时,通过炔酰胺砌块,能够进一步完成药物分子中普遍存在的喹诺酮类与羟吲哚骨架的构建。并且,炔基衍生物同样能够在生物正交化学 (bioorthogonal chemistry)领域中,发挥其重要的价值。此外,通过对炔酰胺骨架的修饰,可以进一步增强其亲电性并抑制剂活性/抗癌活性或其它相关的物理特性,例如溶解性、亲脂性或生物利用度。因此,炔酰胺分子的研究,开始受到化学家的广泛关注。同时,鉴于氟化对于有机分子相关性质的影响,作者假设,通过分子中炔酰胺单元的N-三氟甲基化,能够较好地增强相应分子的亲电性,并伴随亲脂性、溶解性以及其他相关性质的改变。
然而,迄今为止,对于N-CF3炔酰胺化合物的合成却尚未有文献报道。目前在烷基或芳基N-CF3酰胺合成方法学相关的文献报道中,通常需要首先制备出N-CF3氨基甲酰氟 (carbamoyl fluorides),之后选择Grignard试剂,参与后续的转化[1] (Figure 1B)或通过酰胺N-H键的直接三氟甲基化策略,实现N-CF3酰胺分子的构建[2]。然而,采用上述合成策略,均未能成功获得相应的N-CF3炔酰胺类化合物。为首次实现N-CF3炔酰胺类化合物的合成,作者开发出一种将N-CF3氨基甲酰氟直接转化为相应N-CF3炔酰胺的催化策略 (Figure 1D)。
同样地,采用金属催化剂参与的N-CF3氨基甲酰氟中C-F键活化的反应策略,至今仍未有文献报道。其中,对于相应的酰氟 (C-COF)底物,先前已成功地通过Ni、Pd或Ir催化剂的选择,实现有效的活化,并能够较好地进行相应的脱羰或直接烷基化以及芳基化反应过程[3]–[5]。然而,酰氟化合物的直接炔基化反应方法学,至今仍未有相关的研究报道 (Figure 1C)。同时,与酰氟参与的炔基化反应相比,选择过渡金属催化的N-CF3氨基甲酰氟的炔基化方法学中存在的主要挑战在于,R(CF3)N-羰基键同样可能参与相关的氧化加成过程,进而与C-F活化过程存在竞争。事实上,在金属催化条件下,通过活性酰胺参与的交叉偶联反应方法学中,已经观察到上述的竞争反应过程[6]。
最初,作者通过计算研究,确定出一种能够用于化学选择性C-F键氧化加成的优良催化剂,同时,作者对前期已经成功应用于酰氟底物的典型金属催化剂进行进一步研究。有趣的是,计算研究表明,具有膦配体的Ni(0)或Pd(0)催化剂,例如Ni(PCy3)2或Pd(Xantphos),能够优先进行CF3N-C键的氧化加成。
另一方面,作者预测,通过Ni(0)与联吡啶配体的结合,能够使C-F键的氧化加成过程 (ΔΔG⧧ = -6.0 kcal/mol)优先进行。除能够表现出预期的选择性之外,作者通过对C-F键氧化加成的活化自由能 (ΔG⧧ = 13.8 kcal/mol)及其反应能 (ΔGrxn = -18.9 kcal/mol)的计算研究表明,Ni(0)/联吡啶为实现上述C-F键活化过程的一种较为适宜的催化剂。
由此,接下来作者对Ni(0)/联吡啶催化体系参与的N-CF3氨基甲酰氟的炔基化反应进行深入研究。首先。该小组对先前文献报道的能够有效参与Ni催化剂促进的酰氟烷基化或芳基化方法学中的相关偶联参与物 (即RB(OH)2与R2Zn)进行研究。然而,并未获得预期的产物,仅能够回收相应的起始原料。
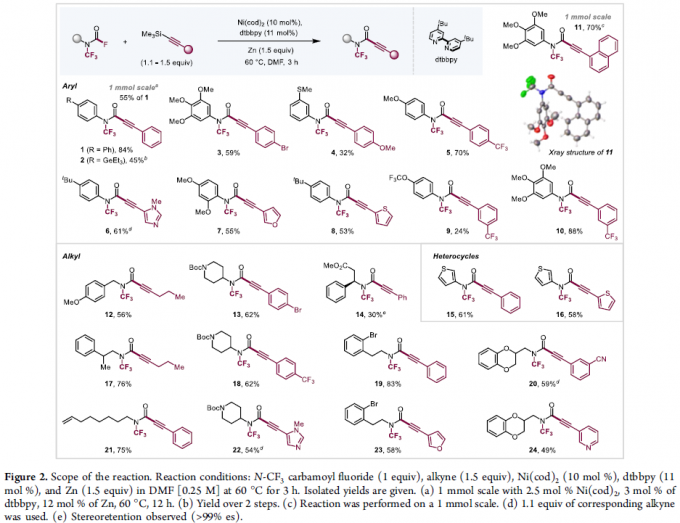
同时,考虑到有机硅化合物良好的亲氟性,作者选择炔基硅烷 (alkynyl silanes)作为反应底物。令人兴奋的是,在选择Ni(cod)2作为催化剂,dtbbpy作为配体,Zn作为还原剂 (抑制Glaser型偶联)时,能够在DMF溶剂中,反应温度为60 oC的条件下,获得84%收率的炔酰胺产物1 (Figure 2)。
在上述的最佳反应条件下,作者对N-CF3氨基甲酰氟与炔基硅烷底物的应用范围分别进行考察 (Figure 2)。研究表明,一系列具有不同基团或官能团取代的芳基以及烷基N-CF3氨基甲酰氟底物,均能够顺利地进行上述的炔基化反应,并获得相应的产物1–24,收率为24-84%。值得注意的是,选择β-苯丙氨酸衍生的N-CF3氨基甲酰氟作为反应底物时,产物14中的手性中心未受影响,然而,却由于肉桂酸酯竞争性消除过程的存在,致使收率显著降低。同时,该小组发现,上述的标准反应条件,对于酰氟与炔基硅烷中的溴代芳基取代基,同样能够良好地进行兼容 (3、13、19以及23),进而表明,上述的炔基化策略具有良好的化学选择性。此外,研究发现,对于带有杂环取代基的炔基硅烷底物,例如吡啶基 (24)、噻吩基 (8、15与16)、呋喃基 (7与23)或咪唑基 (6与22),均能够顺利参与上述的炔基化过程。然而,对于带有强吸电子基团 (例如磺酰基或多重卤素取代基团)取代的芳基N-CF3氨基甲酰氟底物,则存在竞争性的脱羰副反应。值得注意的是,上述的炔基化策略,对于1 mmol规模内的反应,能够进一步将催化剂的负载量降低至2.5 mol%,例如1与11。
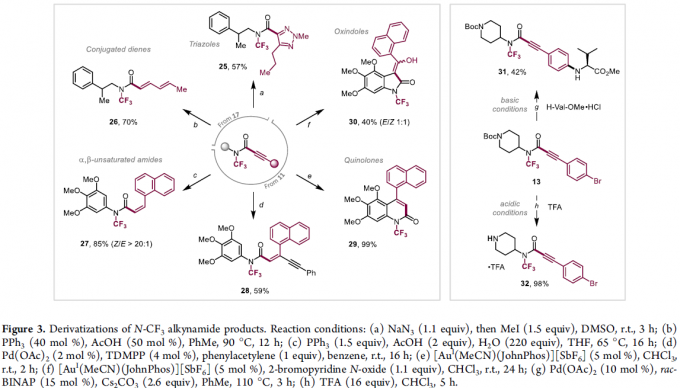
最后,作者对反应的实用性进行研究 (Figure 3)。首先,作者发现,N-CF3炔酰胺化合物17能够与NaN3进行相应的点击反应 (click reaction),并获得57%收率的三氮唑产物25。之后,该小组进一步通过炔酰胺化合物参与的氧化还原异构化或还原以及加成过程,进而获得相应的α,β-不饱和N-CF3酰胺化合物26–28。接下来,作者发现,采用N-CF3炔酰胺化合物作为关键砌块,能够较为容易地合成喹诺酮类 (29)与羟吲哚 (30)衍生物。此外,该小组研究发现,炔酰胺13在酸性条件下,能够去除N-Boc保护基团,进而获得二级胺产物32。同时,在碱性以及升高反应温度的条件下,炔酰胺13中的芳基溴结构单元能够通过进一步的交叉偶联修饰过程,转化为产物31。
总结
德国RWTH Aachen大学Franziska Schoenebeck课题组首次报道一种采用镍催化剂促进的N-CF3氨基甲酰氟与炔基硅烷之间的偶联反应方法学,进而成功获得一系列N-CF3炔酰胺及其衍生物。这一全新的炔基化策略具有实验操作简便、反应条件温和、官能团兼容性高等优势。同时,这一策略为首例在金属催化条件下,通过N-CF3氨基甲酰氟参与的偶联反应。此外,通过后期的衍生化过程,能够较好地完成一系列至今仍难以获得的有机分子的构建,例如烯基酰胺、羟吲哚以及喹诺酮等。
参考文献
[1] T. Scattolin, S. Bouayad-Gervais, F. Schoenebeck, Nature 2019, 573, 102. doi: 10.1038/s41586-019-1518-3. [2] Z. Zhang, J. He, L. Zhu, H. Xiao, Y. Fang, C. Li, Chin. J. Chem. 2020, 38, 924. doi: 10.1002/cjoc.202000132. [3] Y. Zhang, T. Rovis, J. Am. Chem. Soc. 2004, 126, 15964. doi: 10.1021/ja044113k. [4] Y. Ogiwara, Y. Maegawa, D. Sakino, N. Sakai, Chem. Lett. 2016, 45, 790. doi: 10.1246/cl.160223. [5] Y. Ogiwara, D. Sakino, Y. Sakurai, N. Sakai, Eur. J. Org. Chem. 2017, 2017, 4324. doi: 10.1002/ejoc.201700917. [6] (a) C. Liu, M. Szostak, Chem. – Eur. J. 2017, 23, 7157. doi: 10.1002/chem.201605012.(b) J. E. Dander, N. K. Garg, ACS Catal. 2017, 7, 1413. doi: 10.1021/acscatal.6b03277.



















No comments yet.