导读
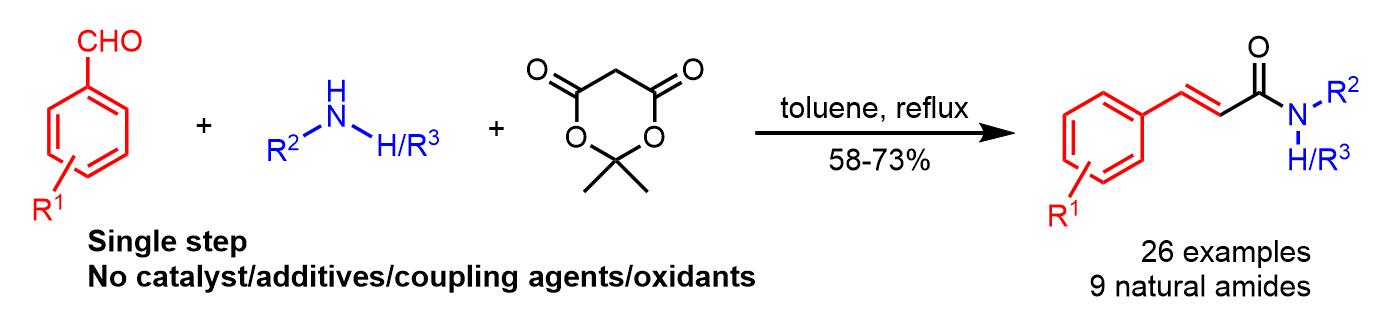
三组分反应是有机实验室最为基本的反应之一,而醛酮胺反应(曼尼希反应)是这类反应中最为经典的代表。近期,印度理工学院Jana教授课题组,通过底物的改变与设计,在Green Chemistry报道了一篇关于醛、酮和麦氏酸三组分一步合成肉桂酰胺和胡椒酰胺类衍生物的文章。该反应条件简单,避免使用文献中各类偶联剂、氧化剂或催化剂等,使反应更加体现原子经济化。作为关键底物的麦氏酸,不仅能醛形成关键的β–羟基酸中间体,同时仅产生丙酮和CO2副产物。
Rapid access to cinnamamides and piper amides via three component coupling of arylaldehydes, amines, and Meldrum’s acid
Santanu Ghosh and Chandan K. Jana
Green Chem., 2019, 21, 5803-5807. DOI: 10.1039/c9gc02937k
正文
肉桂酰胺类衍生物具有广泛地生物活性,如抗癌、抗疟、抗氧化剂、抗菌活性等。此外,肉桂酰胺也是一些天然产物的重要结构单元。因此,大量肉桂酰胺类衍生物被合成报道,用于药物化学领域的相关研究。传统上,肉桂酰胺类衍生物的合成主要通过肉桂酸与胺在偶联剂作用下制备(Scheme 1a)。肉桂醛的氧化酰胺化是另一种合成方法(Scheme 1b)。Wittig反应也是一种制备肉桂酰胺衍生物的方法(Scheme 1c)。然而,多数方法均为多步合成,同时产生一定的副产物(源自偶联剂、氧化剂、膦试剂等)。在此,Jana教授提出了一种通过三组分,一步合成肉桂酰胺和胡椒酰胺衍生物的方案,同时避免使用各类催化剂、试剂或添加剂等。
对于反应的过程,作者提出了设想,首先,麦氏酸(1)与醛经Knoevenagel反应获得烯酮中间体(3),烯酮中间体再与胺(4)进行加成生成酰胺中间体(5),最后经过脱羧反应得到肉桂酰胺(6)。
随后,作者开始对反应条件进行了探索(温度、溶剂、投料比等),最终发现,以甲苯作为溶剂,回流条件下,无需添加任何氧化剂、偶联剂等,直接可以一步合成目标产物。(具体的条件筛选数据,见原始文献。)
紧接着,作者开始对底物的适用性进行了研究。通过改变芳醛的种类(吸电子和给电子的芳醛、杂环醛等),胺的种类(芳香胺、脂肪胺、杂环胺等),均可以获得良好的收率,说明该反应对底物的适应性很强,不受电子效应的影响,空间位阻影响也较少,可以合成多种肉桂酰胺的衍生物。与其它文献比较,一步合成目标产物的产率一般都高于或与文献接近,同时该方法具有原子经济化,仅需一步合成,避免了各类副产物的产生等优势。(具体的底物扩展数据,见原始文献。)
底物扩展之后,作者希望将上述部分底物进行了克级实验,这样更能体现该反应的应用价值。作者选择合成天然肉桂酰胺8a和8b,反映结果和预期一致,均获得良好的收率(Scheme 5)。
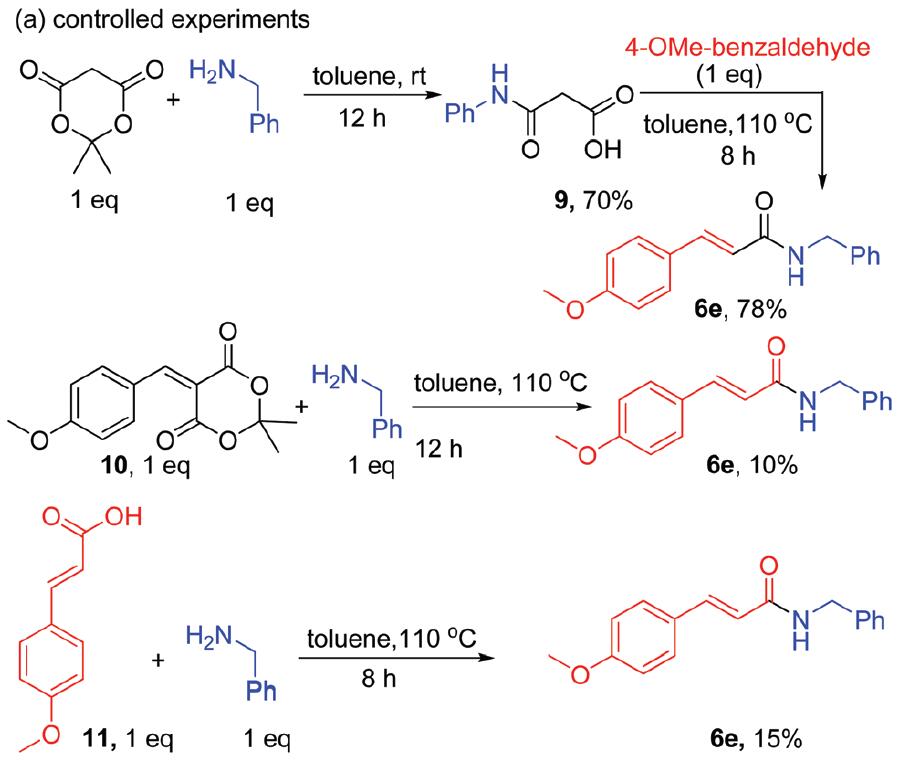
为了验证上述反应机理的正确性,作者进行了一些控制性实验,看是否可以获得目标产物(Scheme 6a)。首先,麦氏酸和苄胺在室温下,生成丙二酸中间体9,紧接着加入芳醛在标准条件下反应,获得目标产物6e。说明该反应需先生成丙二酸中间体9,方可进行下一步反应。随后,我们以最初设想的中间体10(芳醛和麦氏酸经Knoevenagel反应后的产物)与苄胺在标准条件下反应,但仅仅获得少量的产品,说明之前提出的设想机理不正确。此外,作者以肉桂酸和苄胺在标准条件下反应,同样获得少量目标产物,说明肉桂酸也不是反应的主要中间体。
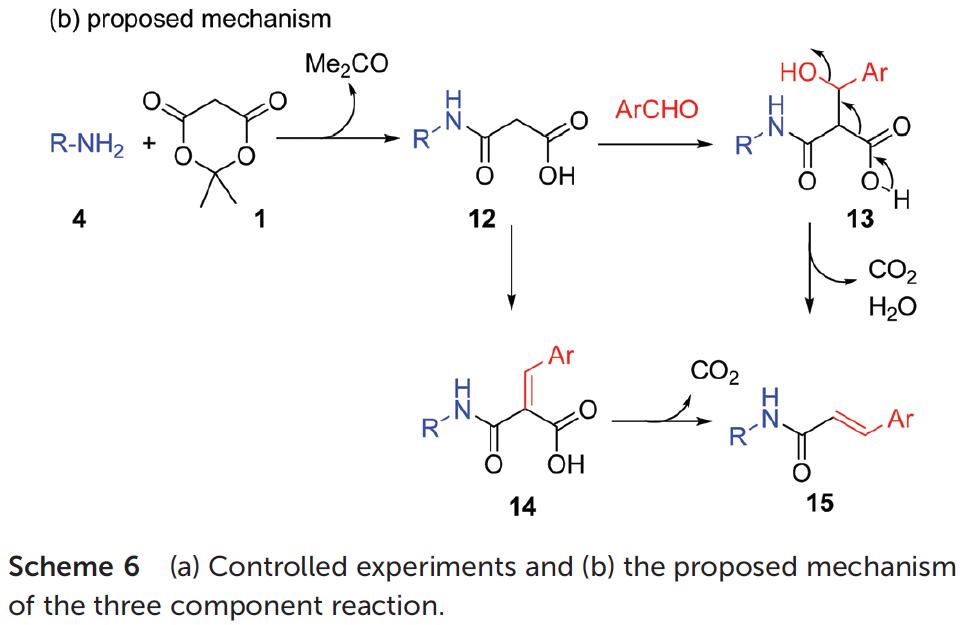
根据上述的实验,作者提出了可能的反应机理(Scheme 6b)。首先,胺与麦氏酸发生加成反应,生成丙二酸中间体12,同时生成副产物丙酮。而获得肉桂酰胺可通过两种可能的方法,一种为中间体12与芳醛经缩合反应可提供β-羟基酸中间体13,加热脱羧脱水获得最终产物。另一种为中间体12与芳醛经Knoevenagel反应生成亚苄基衍生物14,再经脱羧反应,即可获得目标产物。
作者报道了一种三组分(醛、胺和麦氏酸)一步合成多种肉桂酰胺和胡椒酰胺类衍生物的方法,该方法收率高于大部分已知文献。同时,该反应无需使用任何偶联剂、氧化剂或催化剂等,符合原子经济化的标准,引入麦氏酸作为底物,副产物仅有CO2和丙酮。该方法为合成具有医学价值的肉桂酰胺衍生物提供了重要的参考价值。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!






















No comments yet.