本文作者:杉杉
导读
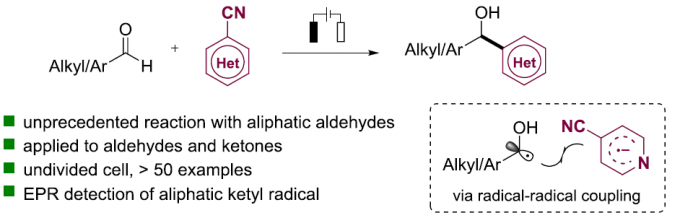
近日,哈尔滨工业大学夏吾炯和杨超课题组合作在Organic Letters上发表论文,报道了一种脂肪族/芳香族醛以及(杂)芳香族酮与氰基(杂)芳烃的电化学还原芳基化反应,从而以中等到良好的收率获得相应的仲醇和叔醇衍生物。机理研究表明,反应过程涉及阴极还原产生羰自由基(ketyl radical)与杂芳基自由基阴离子的偶联过程。
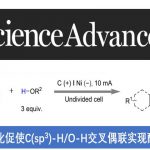
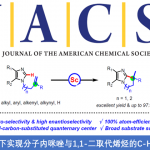
Reductive Arylation of Aliphatic and Aromatic Aldehydes with Cyanoarenes by Electrolysis for the Synthesis of Alcohols
Xiao Zhang, Chao Yang,* Han Gao, Lei Wang, Lin Guo, and Wujiong Xia*
Org. Lett. ASAP DOI:10.1021/acs.orglett.1c00920
正文
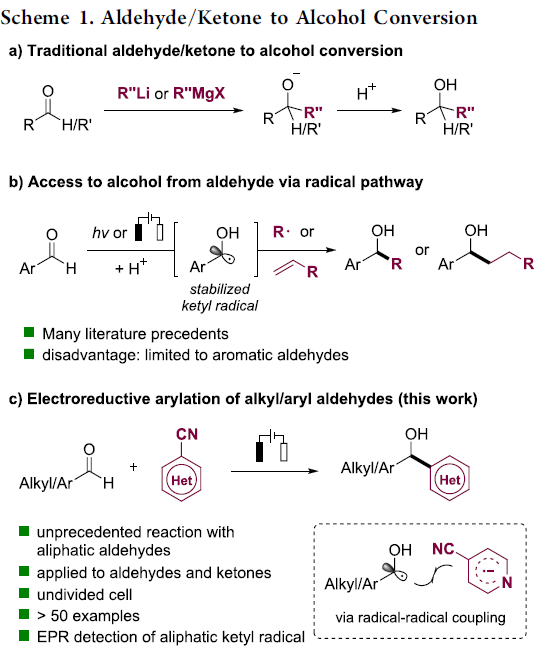
羰基化合物(如醛和酮),广泛存在于各种生物活性分子、药物和功能材料中,同时也是有机化学中常见的骨架。传统合成方法主要通过醛或酮与各种有机金属试剂的亲核加成反应,但具有合成步骤、反应条件苛刻和官能团耐受性低等弊端(Scheme 1a)。近年来,随着光化学和电化学的迅速发展,光电介导的还原芳基化已作为一种绿色环保的氧化还原策略,如通过光诱导或电化学途径将羰基化合物转化为醇(Scheme 1b)。在这两种策略中,羰基化合物被还原以生成稳定的羰自由基,随后与自由基选择性偶联,也可以被不饱和化合物捕获,从而生成醇类化合物。值得注意的是,在大多数情况下,这些策略仅适用于芳香族醛和酮,仅获得苄醇产物。迄今为止,在无强还原剂(如SmI2)或金属溶液(如Na,K溶解在液氨中)辅助时,很少能够通过脂肪族羰基化合物直接合成醇(涉及羰自由基中间体),可能存在两个挑战:(1)脂肪族羰基化合物具有很高的负氧化还原电势;(2)关键的烷基取代羰自由基中间体的寿命不够长。在此,本文将报道一种脂肪族/芳香族醛以及(杂)芳香族酮与氰基(杂)芳烃的电化学还原芳基化反应,从而以中等到良好的收率获得相应的仲醇和叔醇衍生物,涉及阴极还原产生羰自由基与杂芳基自由基阴离子的偶联过程(Scheme 1c)。
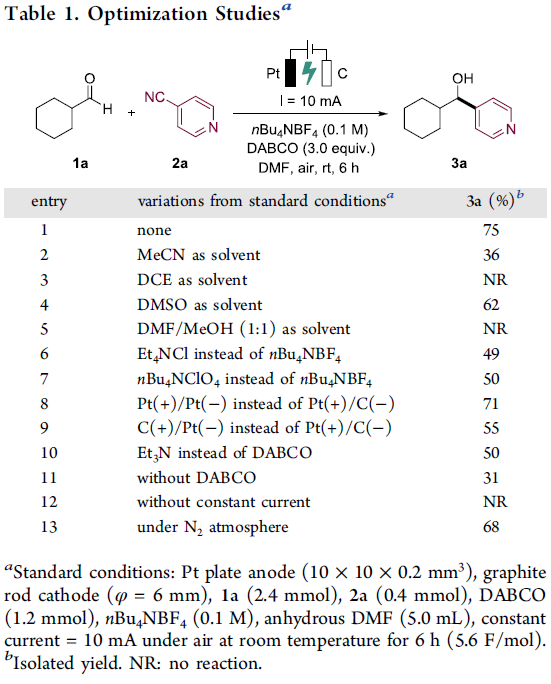
首先,作者以环己烷甲醛1a和4-氰基吡啶2a作为模型底物,进行了相关反应条件的筛选(Table 1)。反应的最佳条件为:以铂板为阳极,石墨棒为阴极,nBu4NBF4为电解质,电流为10 mA,外加入 DABCO,可在DMF溶剂中室温反应,获得75%收率的仲醇3a。
在获得上述最佳反应条件后,作者开始对醛/酮底物1进行了扩展(Scheme 2)。反应结果表明,不同环状脂肪族醛(3a–3e),不同链状脂肪族醛(3f–3u),均可顺利反应。值得注意的是,烯烃(3b,3p,3r和3u),酯(3c),醇(3q)或呋喃(3o)等,均与体系兼容。同时,各种官能化的芳香醛可以高收率转化为相应的醇3v–3ii。值得注意的是,杂芳香醛(如呋喃-2-甲醛),也被有效地转化为相应的产物3ii。此外,一系列苯乙酮衍生物也可与2a进行电化学芳基化反应,以中等到良好的收率提供相应的叔醇3ii-3pp。
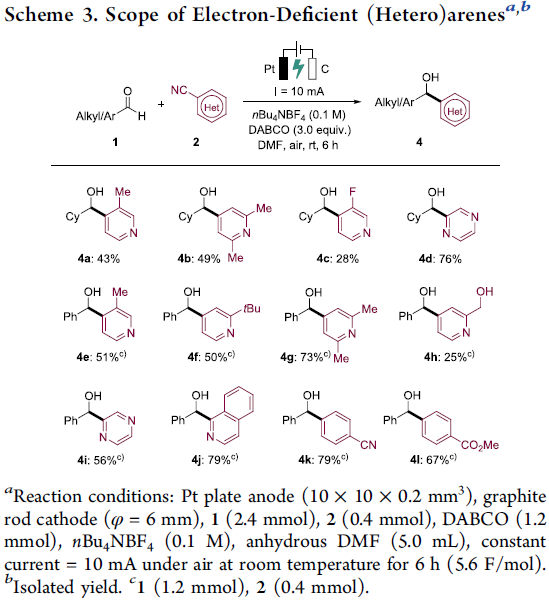
随后,作者对氰基(杂)芳烃2进行了相关的扩展(Scheme 3)。氰基取代的吡啶底物可与脂肪族醛1a进行电化学芳基化反应,获得相应的吡啶醇4a–4c。同时,氰基取代的吡嗪也是合适的底物,获得产物4d,收率为76%。此外,氰基取代的吡啶以及氰基取代的吡嗪和喹啉底物,均可与苯甲醛反应,获得相应的产物4f–4j。值得注意的是,对于缺电子的芳烃(如1,4-二氰基苯和4-氰基苯甲酸甲酯),也可顺利反应,获得产物4k和4l。
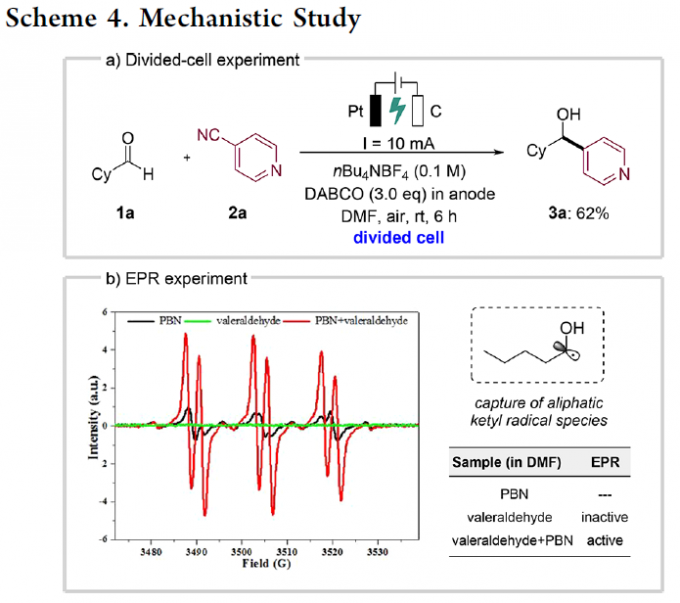
为了进一步了解反应的机理,作者进行相关的对照实验(Scheme 4)。首先,在循环伏安法(CV)中,醛底物和2a都可能发生阴极还原,从而生成相应的自由基中间体。随后,在无隔膜电解实验(divided-cell experiment)中,将DABCO置于阳极,从而获得62%收率的目标产物3a(Scheme 4a)。这些结果表明,石墨棒阴极周围发生了电化学芳基化作用,DABCO仅用作牺牲还原剂,而不是PCET(质子耦合电子转移))试剂。此外,为了进一步了解反应中自由基的起源,作者在恒流下于0.1 M nBu4NBF4/DMF中对戊醛(1g)进行了电子顺磁共振(EPR)实验(Scheme 4b)。由于脂肪族羰自由基的寿命不够长,在戊醛中未检测到明显的信号。当将N-亚苄基-叔丁胺N-氧化物(PBN)引入实验中,通过实验对比,在戊醛和PBN的混合物中观察到信号的快速增长。这些结果表明,戊醛可在阴极被还原以产生关键的脂肪族羰自由基。
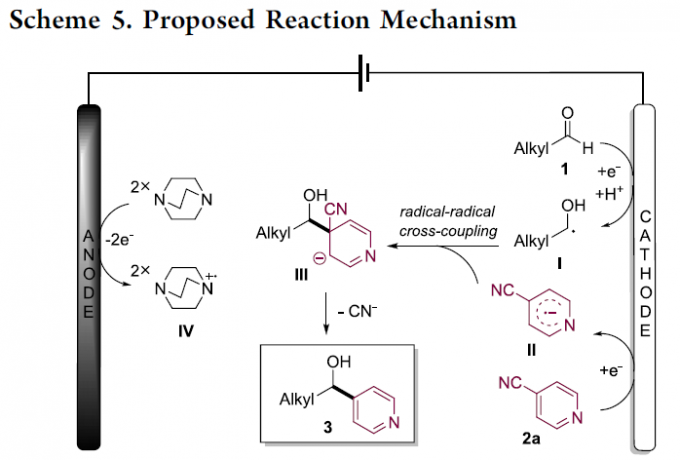
最后,作者提出了一种可能的反应机理(Scheme 5)。首先,羰基化合物1通过阴极电解进行单电子转移(SET)过程,形成关键的羰自由基中间体I。4-氰基吡啶(2a)的阴极还原生成自由基阴离子II。随后,经自由基-自由基偶联生成阴离子中间体III。最后,腈基阴离子经消除,可生成所需的偶联产物3。
总结
哈尔滨工业大学夏吾炯和杨超课题组合作报道了一种高效合成仲醇和叔醇化合物的电化学策略。同时,该反应具有良好的底物范围,各种脂肪族/芳香族醛以及(杂)芳香族酮均可与氰基(杂)芳烃顺利反应。机理研究表明,反应涉及阴极还原产生羰自由基与杂芳基自由基阴离子的偶联过程。



















No comments yet.