本文来自Chem-Station日文版 第一手はこれだ!:古典的反応から最新反応まで3 |第8回「有機合成実験テクニック」(リケラボコラボレーション) webmaster
翻译投稿 炸鸡 校对 HaoHu
这次和理学系实验室网站合作,我们会陆续推出十篇的“有机合成实验技巧”特集。
从第六篇开始将持续为期三篇的“合成化学的第一步!:找遍古典反应到最新反应”系列,这是“合成化学的第一步!:找遍古典反应到最新反应”系列的第三篇,将教大家如何选择实践中用到的合成反应的实验条件。第六篇和第七篇已经为大家介绍了氧化反应・保护基的脱除,还有缩合反应等有机合成化学中常用反应的首选。第八篇为大家介绍交叉偶联反应,内容不仅考虑到了有机合成专业的人员也考虑到了非有机合成专业的人员。
交叉偶联反应的基础
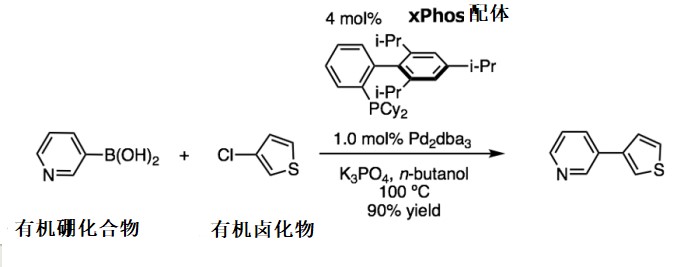
请读者看下面的反应式。这是笔者给大学3年级学生教授有机金属化学的时候举的一个非常有代表性的偶俩反应——铃木—宫浦交叉偶联反应。
当有机硼化合物和有机卤化物在磷酸钾,xPhos配体和Pd2dba3催化剂存在下反应时,可以90%的产率获得偶联产物。反应机理为:有机卤化物的C–Cl键被氧化加成到钯,与硼化合物发生金属转移,随后发生还原消除。
对这个反应完全不知道的同学会很难理解本篇内容,建议这类同学再复习下有机金属化学再来阅读本篇内容。对于那些不明白交叉偶联反应但是想做的同学可以借鉴本篇内容。有些同学明白反应但是却不懂为什么要用这么复杂的试剂和反应条件的同学,建议你们阅读整篇文章。在我教授有机金属化学的课程时,学生们普遍都有以下五个疑问:
- 1.为什么反应物组合得是有机硼化合物和有机卤化物呢?
- 2.为什么要用钯作为催化剂呢?
- 3.配体是怎么影响反应的?
- 4.碱是怎么在反应起作用的?
- 5.反应机理是什么?氧化加成/金属转移/还原消除的机理?
有上述疑问的同学不妨仔细看看有机化学课本上的有关交叉偶联反应历史的介绍,相信你们看完了交叉偶联反应的历史就会明白上述反应条件的含义了。
即使在化学领域,也有许多研究几乎不涉及有机合成。但是,我想让您记住获得诺贝尔化学奖的交叉偶联反应,如果您从事化学研究,那么这个反应的使用频率就会非常的高。
交叉偶联反应的首选反应条件是什么呢?
说了这么多,那么我们本次的主角——交叉偶联反应(铃木—宫浦反应)的首选反应条件是什么呢?
对于偶联反应的初学者来说,偶联反应的反应条件很多,不知道该选择哪一个。当然你可以用SciFinder检索你需要做的实验的反应条件和各种反应底物,如果能找到的反应物就是自己想做的或者和想做的反应物类似而且用到的试剂不是很复杂,价格不是特别昂贵的话就采用那个反应条件了。
但是如果检索不到类似的反应物,但是得立马得做偶联反应那该怎么办呢?
遇到这种情况的话请试试下面的条件。
乙酸钯,三苯膦,碳酸钠,甲苯/水(4:1),80度
从笔者的经验上看这是能保证反应顺利进行的且成本最低的一个反应条件。如果更改了碱,反应变化会很大,如果反应没有进行,试试把碱换成碳酸钾,磷酸钾等。
偶联反应最便宜的首选反应条件
当然不可否认比这个好的反应条件有很多。我下面介绍的是除了这个首选反应条件之外的一些反应条件,我们可以尝试更改一些条件来获得不一样的反应条件(没有学术讨论的意味)。
钯盐:氯化钯或溶解性稍微好一点的氯化钯乙腈络合物,再有Pd(dba)2之类的也可以试试。
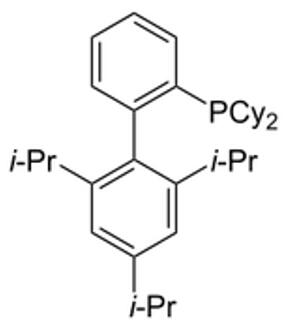
配体:三苯膦是最便宜的,但是如果用三苯膦氧化加成无法进行时,请尝试使用体积大一点的烷基膦(Cy3P。TBu3P)。万能的Buchwald配体可用在很多地方。在众多的Buchwald配体中,推荐读者使用XPhos配体,因为它非常好用。
Xphos
添加剂:在某些情况下,添加冠醚或氯化锂可以显着提高产率。
溶剂:也可以尝试使用THF/H2O溶剂体系和二噁烷/水溶剂体系。
不涉及官能团的交叉偶联反应
以上的内容或许对从事有机合成研究的人来说是不够的。所以我再稍微介绍下近年流行的碳氢键直接活化偶联反应的首选。
上述交叉偶联反应中,偶联剂中需要有官能团存在,例如卤素或硼酸,并且必须进行几个额外的反应以引入官能团。如果可以在不用引入一方或两方偶联剂的官能团的情况下进行偶联反应,则实验效率就会翻倍。这种反应在近十年十分流行,有很多这样的反应条件相继被报道出来。
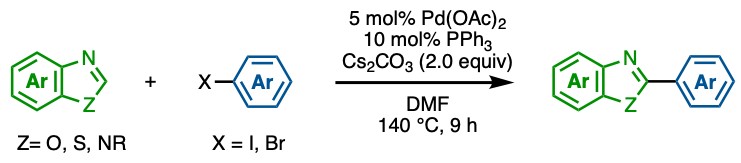
例如,1,3-唑化合物的芳基化反应。这个反应是笔者比较擅长的一个交换反应。在尝试了各种金属,配体和芳基化剂后,探索出的最佳的反应条件如下:
乙酸钯,三苯膦,碳酸铯,DMF,140度[1]
这个反应条件是由大阪大学的三浦教授团队报道出来的初期反应条件,尽管之后有很多新反应条件出现但这个反应条件还是很好用。配体是三苯基膦,非常便宜。当然最好在反应进行后考虑最新的反应条件以进行进一步优化,但三浦教授开发的反应条件足以当做首选了。切记从一开始就千万不要使用廉价的镍或其他的芳基化剂。
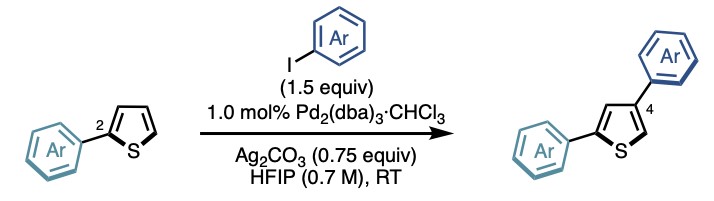
接下来是C3位(β位)芳基化反应生成苯并噻吩和噻吩。作者先前曾报道过类似类型的反应[2a],但这是首选反应条件。
芳基碘・Pd2(dba)3・Ag2CO3, HFIP
这个反应条件是由英国曼彻斯特大学的Larrosa报道的[3]。美中不足的是HFIP有点小贵,但是该反应条件只要室温就可以了。虽然笔者自己报道的反应条件[2b]也不差,但为了做出更好的实验成果还是用了其他人开发的反应条件。
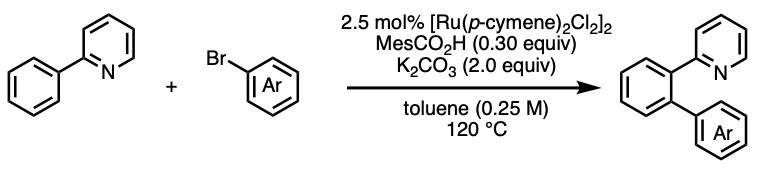
最后,是苯基吡啶的芳基化反应。Ackermann报道的下图的Rh催化反应是首选[4]。
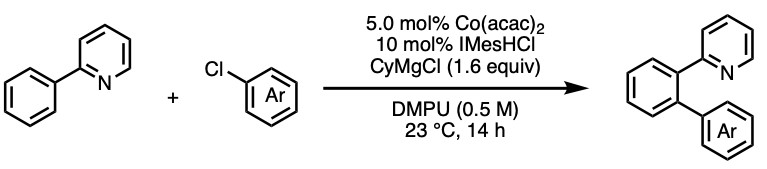
当偶联反应进行的不顺利时不妨试试下面这个反应条件,这个反应条件含有钴催化剂。虽然要加入格氏试剂,但这个反应不需要加热,在室温下就能进行。
自己试试看吧!
以上就是有关交叉偶联反应的反应条件的首选的介绍。至此,我们为期3回的“合成化学的第一步!”到这里也就结束了。如果你手上有最佳的首选反应条件,那么就能很快找到需要的反应物,你的研究也会进行地很顺利,但是笔者还是建议你在做一个新合成反应时也要自己亲自试试不按照文献里建议的反应条件会发生什么结果。
参考文献
- [1] Pivsa-Art, S.; Satoh, T.; Kawamura, Y.; Miura, M.; Nomura, M. Bull. Chem. Soc. Jpn., 1998, 71, 467. DO: 10.1246/bcsj.71.467
- [2] (a)Ueda, K.; Yanagisawa, S.; Yamaguchi, J.; Itami, K. Angew. Chem., Int. Ed. 2010, 49, 8946. DOI:10.1002/anie.201005082 (b) Kirchberg, S.; Tani, S.; Ueda, K.; Yamaguchi, J.; Studer, A.; Itami, K. Angew. Chem., Int. Ed. 2011, 50, 2387. DOI:10.1002/anie.201007060
- [3] Colletto, C.; Islam, S.; Jukiá-Hernández, F.; Larrosa, I. J. Am. Chem. Soc. 2016, 138, 1677. DOI: 10.1021/jacs.5b12242
- [4] Ackermann, L.; Vicente, R.; Althammer, A. Org. Lett. 2008, 10, 2299–2302. DOI: 10.1021/ol800773x
- [5] Punji, B.; Song, W.; Shevchenko, G. A.; Ackermann, L. Chem. Eur. J. 2013, 19, 10605–10610. DOI: 10.1002/chem.201301409
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!


























No comments yet.