本文作者:竹悠
不管是医药、农药还是化学材料中,引入氟元素总会改善原来的性质。在众多的含氟官能团以及氟类似物种,氟甲基芳基醚可以改善挥发性而更适合于生物信息素或制造香水。氟化学发展至今,已产生了众多的氟化方法。最近几年,电化学合成也逐渐走上舞台,丰富了合成方法
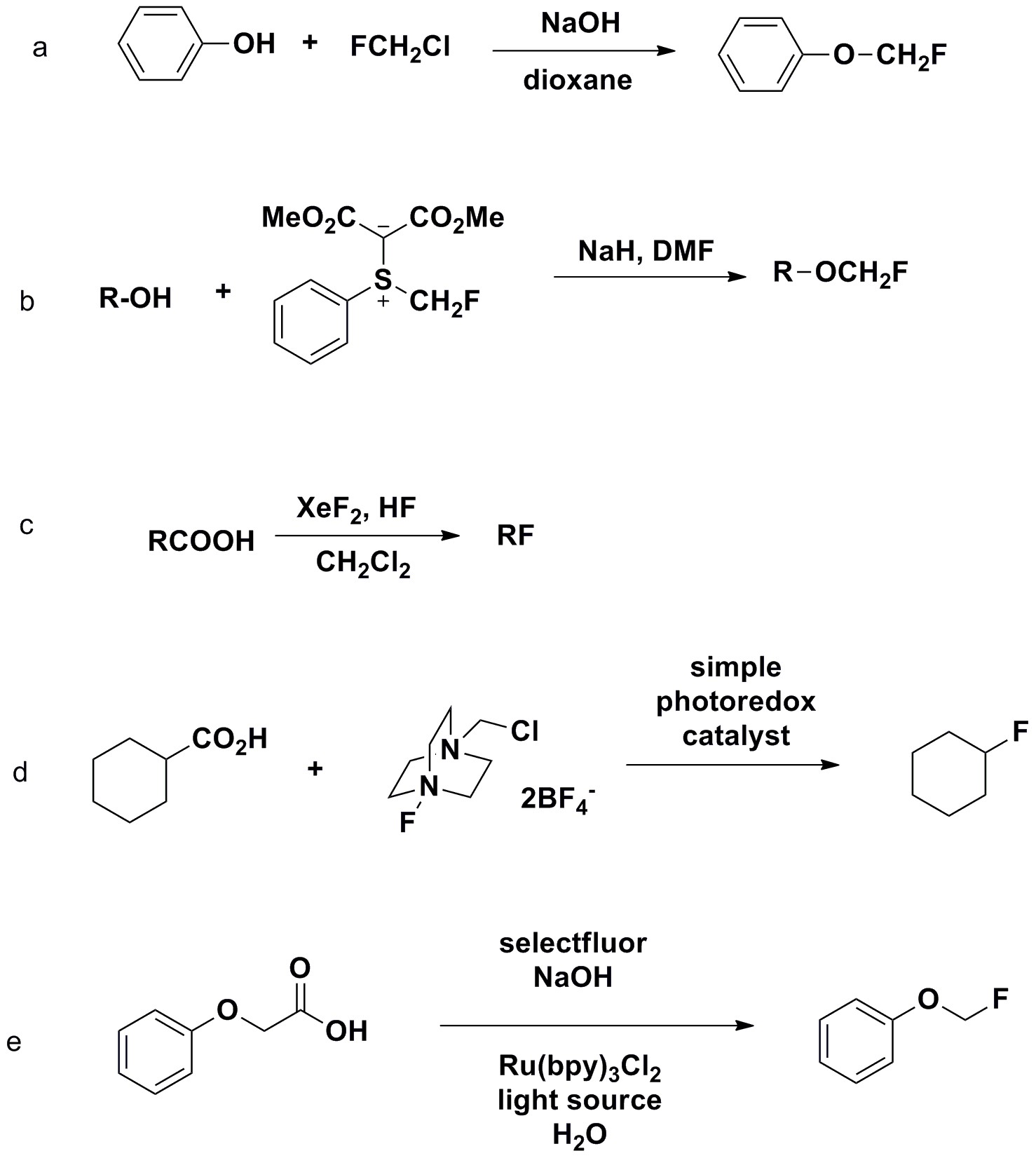
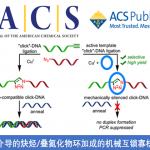
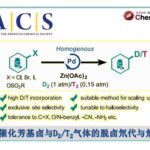
在合成氟甲基芳基醚中,第一例合成氟甲基芳基醚的方法为苯酚在碱性条件下和亲电性的FCH2Cl反应,氯作为离去基团(图1a),但FCH2Cl为温室气体或者和氟化试剂单氟甲基取代的锍叶立德sulfonium ylides反应(图1b),但其氟化试剂制备冗长复杂。另外一种策略是苯氧基羧酸的脱羧氟化反应,如最早报道的XeF2为氟化试剂的自由基反应,XeF2太活泼而难以驾驭(图1c)。MacMillan组将光氧化还原和氟化试剂SelectfuorTM组合,可以将脂肪族的羧酸转化为氟(图1d)。同样是用SelectfuorTMTang等发现在二氯甲烷/水体系中,富电子的芳香羧酸可以生成氟化物。Sammis 和 Hartwig组将AgF2和苯氧羧酸发生Hunsdiecker型氟化反应中(图1e)。但上述方法都存在一个成本较高的缺陷。
图1 不同的氟化反应
电化学作为一种清洁能源,不需要额外的化学试剂,因此不产生污染,而且可以作为氧化剂原位生成活泼中间体,更符合绿色化学的理念,因此电化学合成最近几年逐渐成为热门。
虽然1849年就Kolbe就报道了脱羧反应的电化学反应,两个脂肪族羧酸生成二聚体,但氟化未见报道。最近德国美因兹大学的Siegfried R. Waldvogel报道了不需要金属催化剂,以电化学合成氟甲基芳基醚,论文发表在Chemical Science上:
Michael Berger, John D. Herszman, Yuji Kurimoto, Goswinus H. M. de Kruijff, Aaron Schüll, Sven Ruf, Siegfried R. Waldvogel.
Metal-free electrochemical fluorodecarboxylation of aryloxyacetic acids to fluoromethyl aryl ethers
Chem. Sci. 2020, ASAP. DOI: 10.1039/d0sc02417a
反应条件优化
作者以不分离的反应池为主要反应装置,加入一个简单的石墨双电极Cgr,电流为定值,如图2所示。
图2. 电化学反应池. 图片来源: Chem. Sci.
以4-叔丁基-苯氧基乙酸1a为底物,在溶剂二氯甲烷中的浓度为0.1mol/L,反应参数有:电流大小、电荷、氟化试剂、电极材料。以1,3,5-三甲氧基苯为内标,通过1H NMR表征各反应条件下的产率,各参数的表现如表1所示。
初始条件下,电荷为3F,电流强度为5.5mA cm-2,KF(3.0 eq),18-冠醚-6(3.0 eq),2,4,6-三甲基吡啶(3.0 eq),二氯甲烷中电解质NBu4PF6的浓度为0.1M,生成2a的收率为30%。空白对照实验发现电流和碱非常重要。从优化过程中可以看到,增加KF用量不能提高收率,替换碱为DBU没有产物,使用Py•9HF为氟化试剂,Kolbe反应被抑制,同时产物收率也下降。氟化试剂Et3N•3HF没有任何产物,但是更换为Et3N•5HF后,收率提高至58%,原料也全部消耗了,因此氟化试剂定Et3N•5HF,降低用量(9 : 1)反而提高了收率,用量再提高后会分解电解材料。而且增加KF用量也不会再提高收率,说明氟的增加对反应效果并不好。电流不能太小,为2.8mA cm-2时降低收率47%,但增大至11mA cm-2后不生成产物。理论电荷为2.0F,但将应用电荷从3.0F降至2.5F后导致收率下降。降低碱的用量也降低收率。最后来看电极材料,无论是铂电极、硼掺杂金刚石BDD电极或玻璃碳都没有产物(entry11-13),石墨箔((entry 14)与等静压石墨电极效果相当。
底物扩展
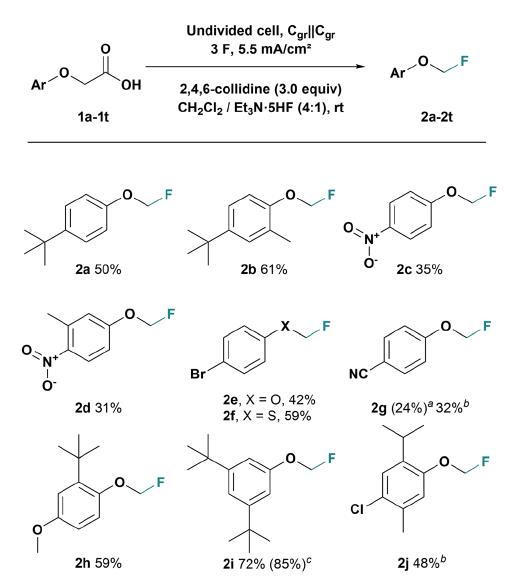
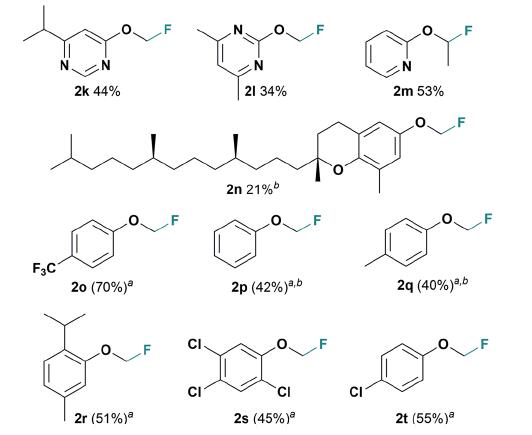
类似于4-叔丁基-苯氧基乙酸的α,α二甲基化的底物没有生成期望的季碳氟化物,虽然季碳碳正离子更稳定,但季碳氟化物可能在电化学中不稳定或发生了消除反应。苯环上其他位置的取代基可以生成产物,见图3。如甲基2b,硝基2c、2d,溴2e以及氰基2g等,富电子的二叔丁基取代物2i收率最高达72%,扩大规模至2.5mmol后收率又提高至85%。天然产物维生素E的氟化物2n收率为21%。总体而言,电极材料石墨纸电极比等静压石墨电极效果好。
图3. 不同的底物及收率. 图片来源: Chem. Sci.
反应机理
最后,让我们一睹电化学反应的机理,这个反应类似于Pseudo-Kolbe型电化学合成,电子在连接羧酸部位的发生转移,而不是发生在羧酸本身。芳氧基羧酸1在阳极氧化为自由基阳离子Ⅰ,然后等排为氧鎓离子Ⅱ,脱羧后生成自由基Ⅲ,但自由基Ⅲ的溶剂化能力差,容易再次被氧化为氧鎓离子Ⅳ,等排为碳正离子Ⅳ,随后被氟亲核试剂进攻,生成醚2,如图4所示。
图4. 可能的反应机理. 图片来源: Chem. Sci.
总结
电化学合成,使用直接使用直流电为试剂来源,在阳极发生氧化,与其他化学氧化试剂而言,本质更加清洁和安全。作者以羧酸这一广泛存在的官能团转为为氟,将来可以应用在药物或其他底物的后期修饰上。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!






















No comments yet.