本文作者:杉杉
导读
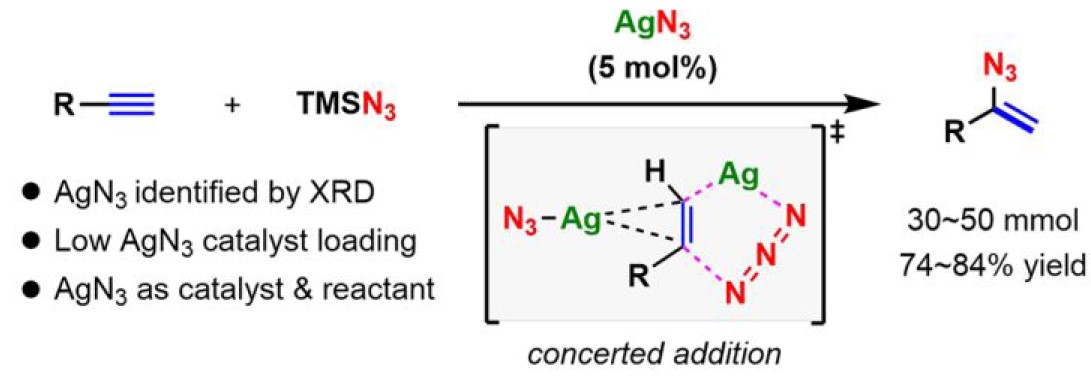
炔烃的加氢叠氮化反应作为合成叠氮乙烯基最为直接的方法,东北师范大学毕锡和教授课题组早在2014年就使用Ag2CO3作为催化剂,实现此类反应,然而,由于催化剂的高负载量(20 mol%Ag)从而限制其实用性,此外,确切的反应机理仍然不清楚。近日,东北师范大学毕锡和教授课题组在美国化学学会杂志(Journal of the American Chemical Society)发表论文,基于对银盐转化的X-射线衍射研究,从而发现AgN3作为该反应中真正催化物质,因此,作者研究了AgN3催化下末端炔烃的加氢叠氮化反应。反应结果表明,AgN3作为一种高效的催化剂(低至5 mol%,即使放大至50 mmol,也同样有效)。此外,对照实验和相关的理论计算表明,通过六元过渡态的协同加成机理比经典的乙炔银机理更受青睐。
AgN3-Catalyzed Hydroazidation of Terminal Alkynes and Mechanistic Studies
Shanshan Cao, Qinghe Ji, Huaizhi Li, Maolin Pang, Haiyan Yuan, Jingping Zhang, and Xihe Bi
J. Am. Chem. Soc. ASAP DOI: 10.1021/jacs.0c00836
正文
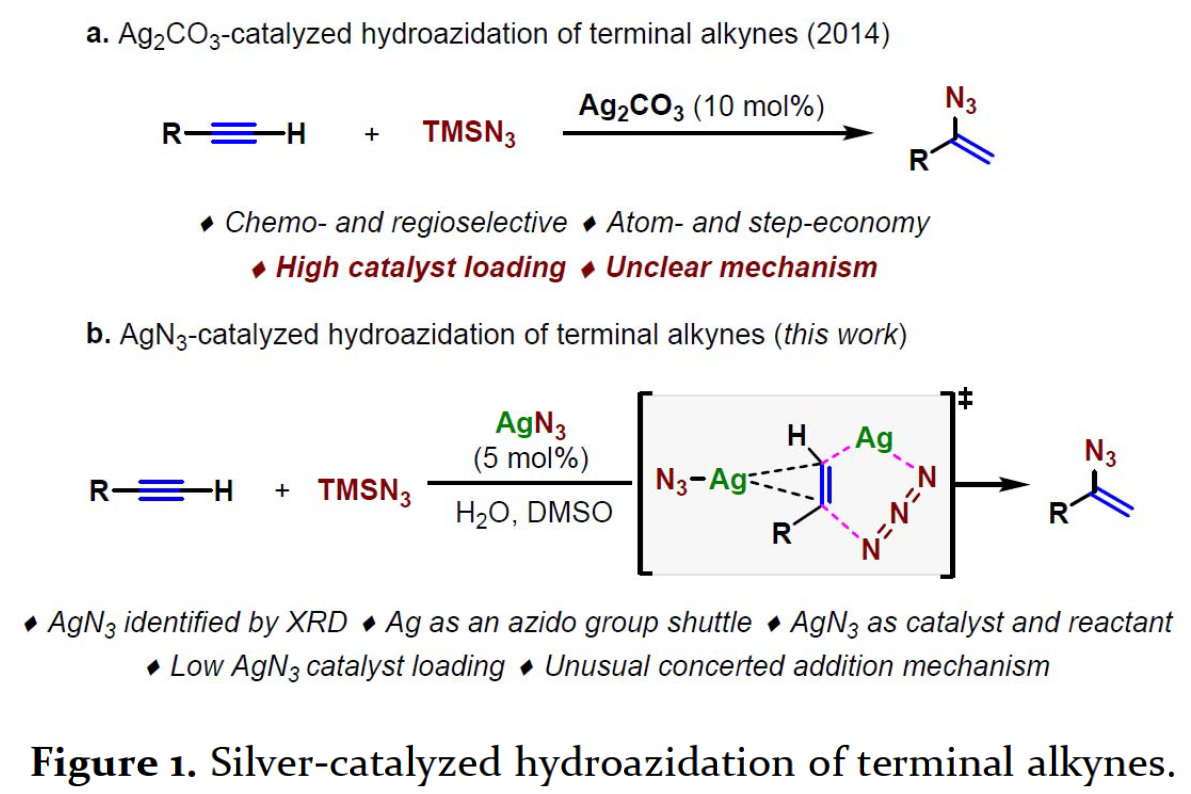
炔烃作为有机合成中重要的底物之一,而通过催化剂将C≡C转化为一些具有重要价值的官能团具有重要的意义。炔烃的加氢官能团化(具有原子经济性)是获得官能团化烯烃的一种高效途径,而炔烃的加氢叠氮化反应也是获得α-乙烯基叠氮化物的最为直接的方法(有机合成中的通用结构单元)。然而该反应主要通过叠氮化物阴离子向活化炔烃进行迈克尔加成。对于一些未活化炔烃而言,并没有有效的方法,直到2014年,本课题组报道了Ag2CO3作为催化剂,实现末端炔烃加氢叠氮化反应(Figure 1a)。然而,由于存在反应机理尚不清楚、使用高负载量银盐(20 mol%Ag)等问题,从而限制了该方法的实用性。
在过渡金属催化的反应中,如果能够将有机金属中间体进行相关的分离和鉴定,对于了解反应的机理至关重要。然而,对于银催化反应过程的研究则更具挑战性(原位形成的有机银中间体容易发生去金属-质子化反应)。因此,非常需要一种能够在反应过程中识别银中间体的技术。通过大量的研究,作者发现X-射线衍射(XRD)可用于识别金属催化剂在反应过程中的活化或失活行为。在此,东北师范大学毕锡和教授课题首次使用XRD对银催化有机反应进行了相关的研究,发现Ag2CO3可迅速转化为AgN3,从而确定了AgN3作为实际的催化物质(Figure 1b)。尽管有文献报道将AgN3作为某些银催化反应的可能中间体,但尚无任何光谱学数据支持。此外,AgN3用于炔烃加氢叠氮化反应时具有高效性,即使较低的负载量(5 mol%)和放大反应(高达50 mmol)均取得较好的结果。最后,对照实验研究和理论计算进一步阐明了AgN3的催化机理。
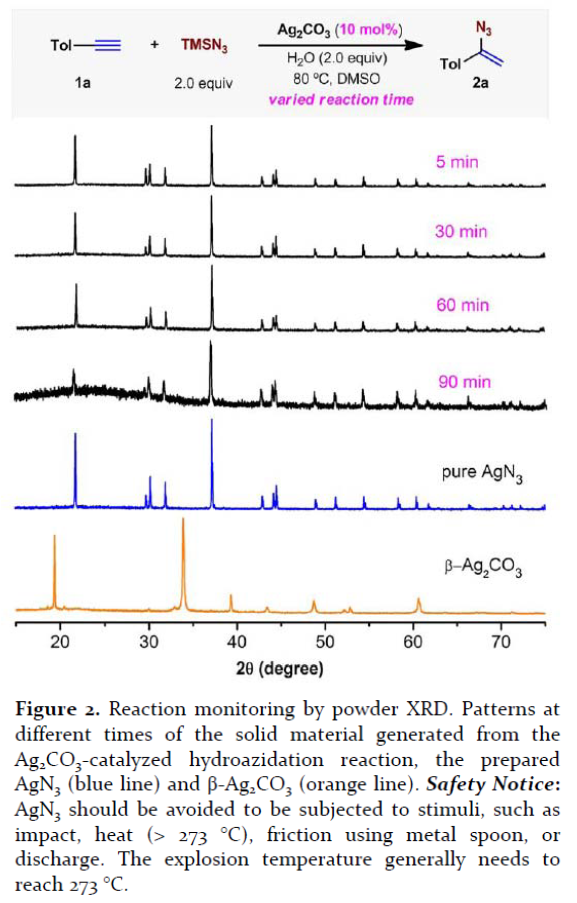
首先,作者选择对甲苯基乙炔1a作为模型反应物,对Ag2CO3催化的加氢叠氮化反应进行了相关的XRD研究(Figure 2)。XRD分析结果表明,Ag2CO3可在5min内快速且完全转化为AgN3,而叠氮化乙烯产物2a尚未观察到。此外,其它几组对照实验与纯AgN3的对比说明,该反应中AgN3作为真正的催化物。同时,该方法作为首次使用XRD对银盐催化有机反应的研究。
为了进一步证实Ag2CO3可高效的转化为AgN3(Figure 3a),作者在不使用炔烃和水的情况下,用三甲基叠氮化硅(TMSN3)与Ag2CO3反应,通过XRD分析可知,Ag2CO3可快速且完全转变为AgN3,同时副产物六甲基二硅氧烷[(CH3)3Si-O-Si(CH3)3](1H、13C和29Si NMR光谱法和MS分析确认)。此外,该反应代表了银盐参与的无机新反应。同时,为了合理化反应过程,作者也进行了相关的DFT计算,结果表明Ag2CO3可在标准条件下快速且平稳地转化为AgN3。
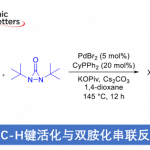
首先,作者以1,3-二甲基吲哚1a和N,5-二甲氧基吲哚-1H-羧酰胺2a作为模型底物,进行了相关 [4+2]环化反应条件的筛选(Table 1 ,entry 4,entries 9-10)。
基于上述的讨论,作者首先制备AgN3催化剂,并在80℃的水中将底物对甲苯基乙炔1a和TMSN3进行相关的加氢叠氮化反应的研究(Figure 4a)。反应结果表明,转化率随AgN3负载量的增加而增加,甚至低至5mol%的AgN3都可以完全转化,从而以89%的NMR收率获得所需的叠氮化乙烯基产物2a。这些结果表明,AgN3作为该类反应中高催化活性的真正催化物质。此外,作者还对溶剂进行了筛选(Figure 4b),当使用DMSO时可获得86%分离收率的叠氮化乙烯产物2a,除DMF(收率54%)外,其他溶剂(如CH3CN、THF和1,4-二恶烷)全部无效。
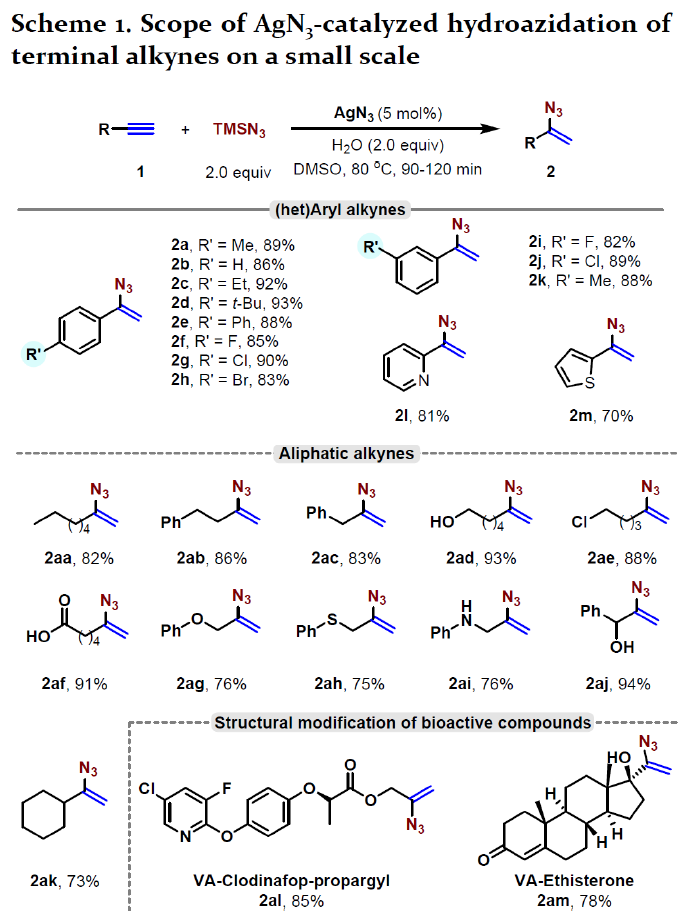
在获得上述最佳反应条件后,作者开始对了AgN3催化的加氢叠氮化反应的底物范围进行了扩展(Scheme 1)。不同取代的芳基炔烃,不受电子效应和定位效应的影响,均可顺利反应,获得相应的叠氮化物2a–2k(收率82-93%)。杂芳基炔烃(2-吡啶基和2-噻吩基乙炔),同样可以转化为相应的杂芳基乙烯基叠氮化物2l(81%)和2m(70%)。随后,作者对烷基炔烃也进行了扩展,如正己基、苯乙基和苄基取代的炔烃分别以82%、86%和83%的产率获得相应的产物2aa–2ac。此外,一些带有敏感性基团(如羟基、氯、羧基、醚、硫醚和氨基等)的烷基炔烃,均能顺利反应,从而以较高收率(75-94%)获得产物2ad–2aj 。环己基乙炔同样以73%的收率获得2ak。值得注意的是,该反应还适用于生物活性化合物炔草酯(clodinafop-propargyl,1al)和炔孕酮(ethisterone,1am)的直接修饰,分别以85%和78%的收率获得相应的乙烯基叠氮化物2a1和2am。反应结果表明,AgN3在末端炔烃的加氢叠氮化反应中具有出色的催化活性,同时也是AgN3在有机反应中首次利用。
随后,作者对该反应进行了相关的放大实验,从而进一步证明实用性(Scheme 2)。作者发现,底物芳基炔烃1a、1b和1g,可在30-50 mmol上放大,从而以89%、77%和79%的产率获得相应的产物2a、2b和2g。另外,具有醚(2ag)、硫醚(2ah)、羟基(2aj)、受保护的氨基(2an)或环己烯基(2ao)基团的官能化脂肪族炔烃,同样适合放大反应,获得所需的乙烯基叠氮化物,具有较高的产率。值得注意的是,在这些反应中均使用了5mol%的AgN3,进一步证明了AgN3作为末端炔烃的加氢叠氮化反应的高效催化剂。
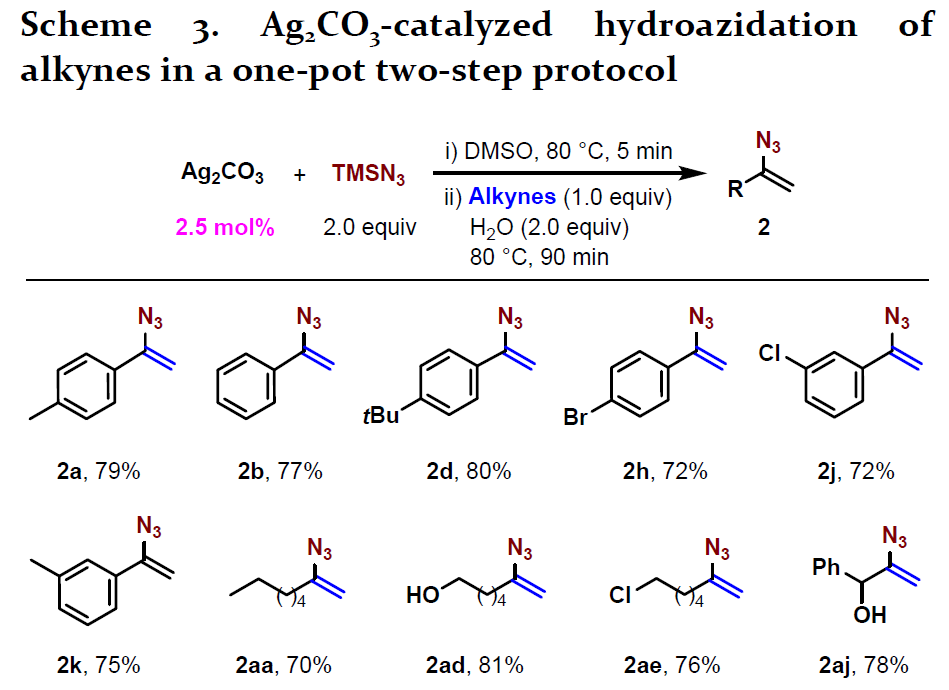
紧接着,为了避免AgN3使用过程中潜在的爆炸性危险,作者开发一种一锅两步法的方案,同样使用Ag2CO3作为催化剂以实现类似的高效催化(Scheme 3)。当作者对一锅两步实验中可能影响反应结果的因素的进行了深入研究时,作者发现,应在原位形成AgN3后应加入水,否则会明显抑制催化活性。从Ag2CO3到AgN3的转化过程中同时形成了含絮凝物,并覆盖在AgN3颗粒的表面。最终,作者通过一锅两步法,使用低负载量的催化剂Ag2CO3,实现加氢叠氮化反应,并且底物范围很广泛,以70-81%的产率获得了相应的乙烯基叠氮化物。
为了进一步了解反应的机理,作者进行了相关对照和氘代实验(Scheme 4)。当使用两当量的D2O时,1b与TMSN3反应以85%的收率获得氘代产物[D] –2b(氘代和非氘代分别占36%、36%、14%和14%(Eq. 1))。而以氘化底物[D] –1b作为底物时,以相似的收率(86%)获得[D] –2b,尽管单氘化产物的收率很低(10%和6%)(Eq. 2)。上述两个结果表明,由炔烃Csp-H键断裂形成乙炔银中间体。随后,在不使用AgN3时,以乙炔化银[Ag]-1b作为反应物,同样获得叠氮化乙烯2b和炔烃1b(比例为1:2.8)的混合物(Eq. 3)。该反应证明了,炔烃和乙炔银之间存在快速平衡,同时作者也通过DFT计算得到了证实。相反的,如果在相同条件下使用内部炔烃1b-Me作为底物(Eq. 4),则不会发生反应。
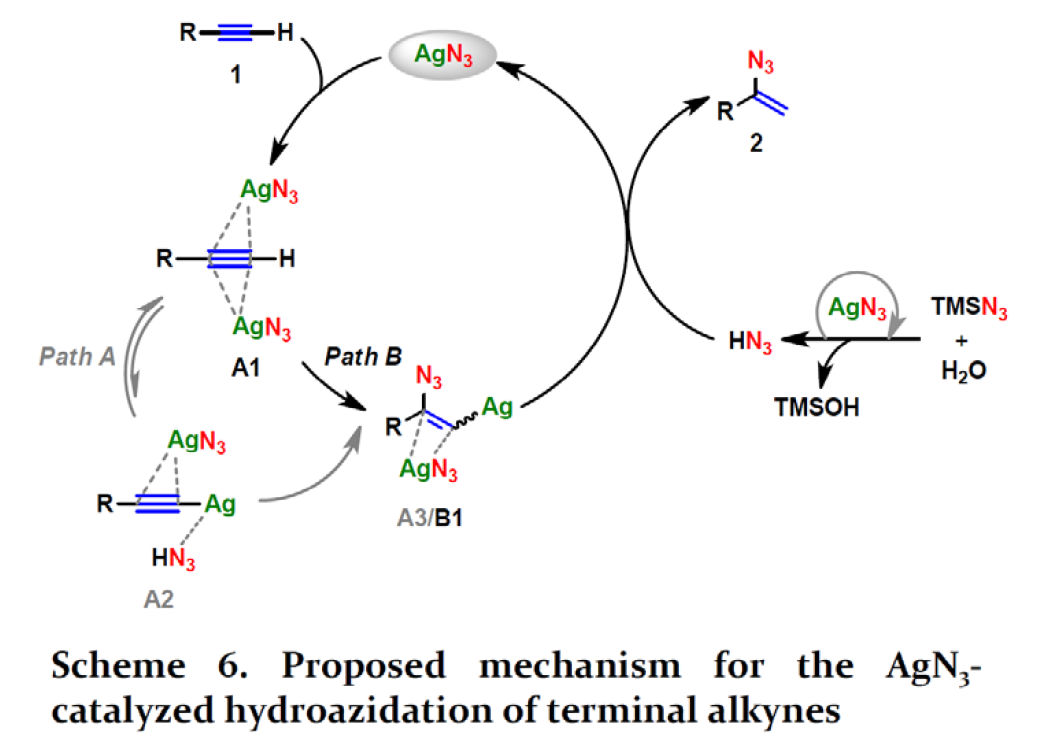
根据上述的实验和相关计算数据的总结,作者提出了两种可能的反应机理(Scheme 6)。首先,由AgN3与炔烃1形成具有两个AgN3分子的Ag-π络合物A1。A1可能会发生炔烃的Csp-H键断裂,从而得到AgN3-Ag-HN3络合物A2,再经亲核加成即可获得烯基银中间体A3(Path A)。或者,A1与炔烃1经阳离子银和叠氮基阴离子的协同加成,也可以产生烯基银中间体B1(A3和B1是异构体,Path B)。最后,A3或B1的质子化形成HN3,并获得叠氮化乙烯基产物2,其中HN3生成的水可与TMSN3反应从而继续完成催化循环。
总结
东北师范大学毕锡和教授课题组报道了一种高效的AgN3催化末端炔烃的加氢叠氮化反应。XRD研究表明,AgN3作为Ag2CO3催化反应中真正有效的催化剂。此外,Ag2CO3和TMSN3之间可生成AgN3(新的无机反应),并通过DFT计算使其进一步合理化。同时,AgN3催化剂具有高效(负载量低至5 mol%)且实用性(可放大至30-50 mmol))。DFT计算揭示,协同加成机理比逐步乙炔化银机理更有利。总之,作者首次提出将AgN3用作有机合成中的催化剂,并实现末端炔烃加氢叠氮化反应,同时进一步阐明了催化机理。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!
















No comments yet.