本文作者:海猫
导读
近日,南京大学的魏辉教授课题组在分析化学杂志上发表论文,报道了使用基于杂原子掺杂的石墨烯来构建用于检测芳香族农药的比色纳米酶传感器阵列。当不同的农药被吸附在石墨烯上时,纳米酶的活性位点可能被不同地掩盖,从而导致其过氧化物酶模拟活性的不同程度的降低。根据这一原理,作者通过传感器阵列成功地分辨出了5至500 μM的五种农药,并实现了对每种农药的不同浓度和两种混合农药的不同比例的区分。通过成功地区分土壤样品中的农药,进一步验证了传感器阵列的实际应用。这项工作不仅提供了一种简便且经济高效的方法来检测农药,而且为食品安全和环境保护做出了积极贡献。
Nanozyme Sensor Arrays Based on Heteroatom-Doped Graphene for Detecting Pesticides
Yunyao Zhu, Jiangjiexing Wu, Lijun Han, Xiaoyu Wang, Wei Li, Hongchao Guo, and Hui Wei
Anal. Chem. ASAP DOI: 10.1021/acs.analchem.9b05110
正文
农药可以保护作物免于虫害以及规范植物的生长,一直以来被广泛的使用。但是很多农药都很难降解,会在土壤中堆积而导致土壤硬化以及环境污染。在作物中的农药经过长时间的堆积会对人类的健康产生影响,因此发展有效检测农药的方法是很有必要的。目前已经有很多检测方法,比如GC-MS,LC-MS以及SERS(surface-enhanced Raman scattering)等,它们可以高灵敏度及选择性的检测农药,但是往往需要昂贵的仪器以及复杂的操作。其他诸如ELISA和生物传感器检测的方法中,使用的酶和抗体都比较昂贵并且容易失活。因此,发展简单有效检测农药的方法是很有必要的。
纳米材料因其光致发光、荧光等性质,已经有其被研究者用于农药检测的报道。而具有类酶活性的纳米材料在农药检测中具有优势,因为它们的价格相对较低,并且稳定性比较好。不过到目前为止还没有使用多元纳米酶检测农药的报道。
传感器阵列是一种可以识别和区分不同分析物的方法,通过同时产生交叉响应的阵列数据来完成。在此之前,使用传感器阵列检测农药也已经有了广泛的研究,比如基于染料,发色试剂以及金属纳米颗粒等的比色传感器阵列、基于石墨烯量子点的化学发光传感器阵列、基于石墨烯量子点和染料的荧光传感器阵列、基于酞菁的石英晶体微平衡传感器阵列等。虽然近年来已经开发出了生物活性小分子、蛋白质和细胞的纳米酶传感器阵列,但还没有被用于检测农药的研究。
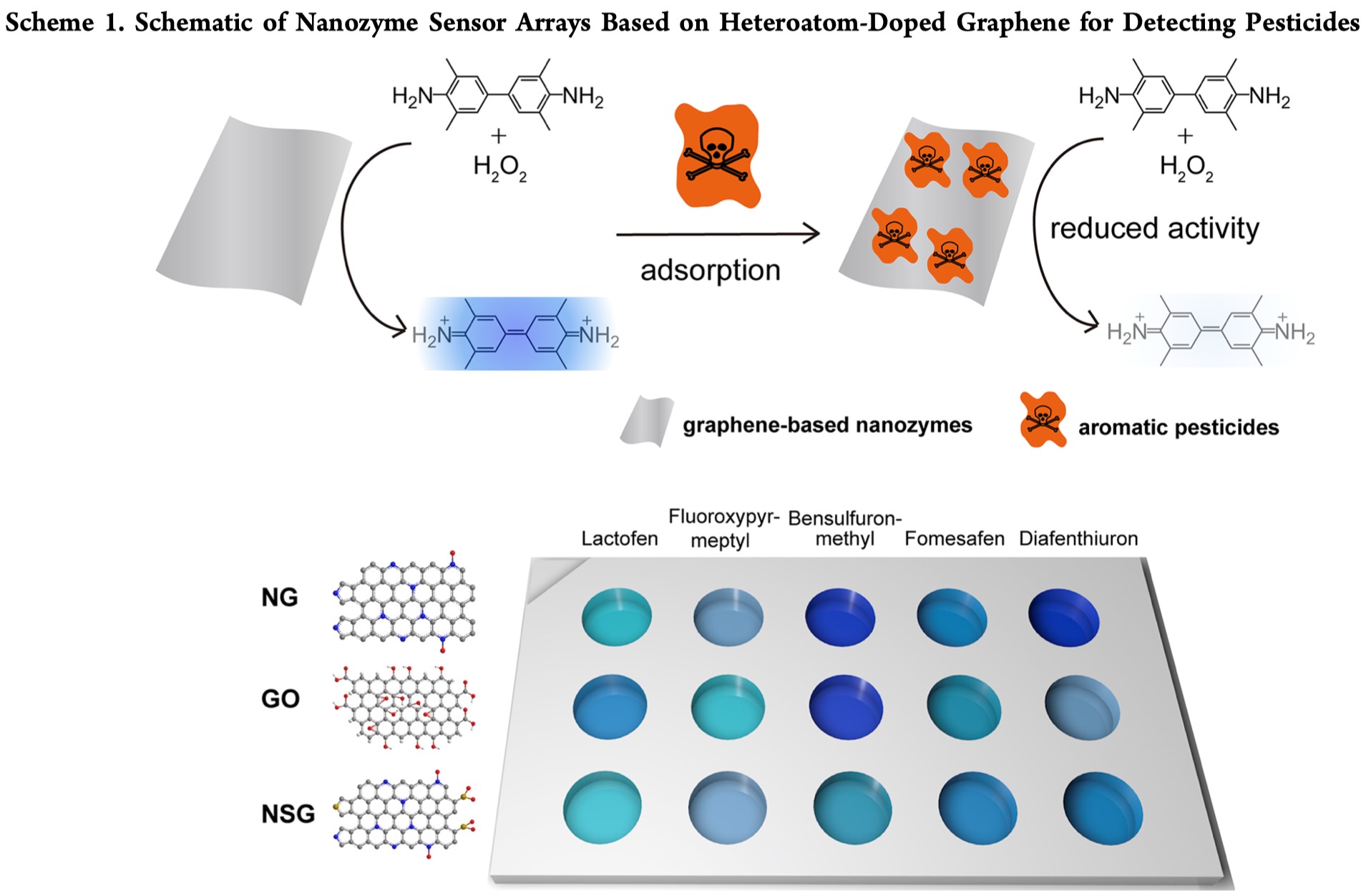
因此,作者将传感器阵列和纳米酶结合在一起,构建了纳米酶传感器阵列,用于成本较低的农药检测(Scheme 1)。使用了氮掺杂石墨烯(NG)、氮硫共掺杂石墨烯(NSG)和氧化石墨烯(GO)这3种具有类过氧化物酶活性的石墨烯材料,催化3,3′,5,5′-四甲基联苯胺二盐酸盐(TMB)与过氧化氢反应产生蓝色。在芳香族农药存在的情况下,基于石墨烯纳米酶的活性位点被吸附而掩盖,导致模拟过氧化物酶活性的降低、蓝色减弱。作者用这三种石墨烯材料构建的传感器阵列来分辨lactofen,fluoroxypyr-meptyl,bensulfuron-methyl,fomesafen和diafenthiuron这五种农药,并且验证了区分土壤样品中的农药和两种不同比例的混合农药的可行性。
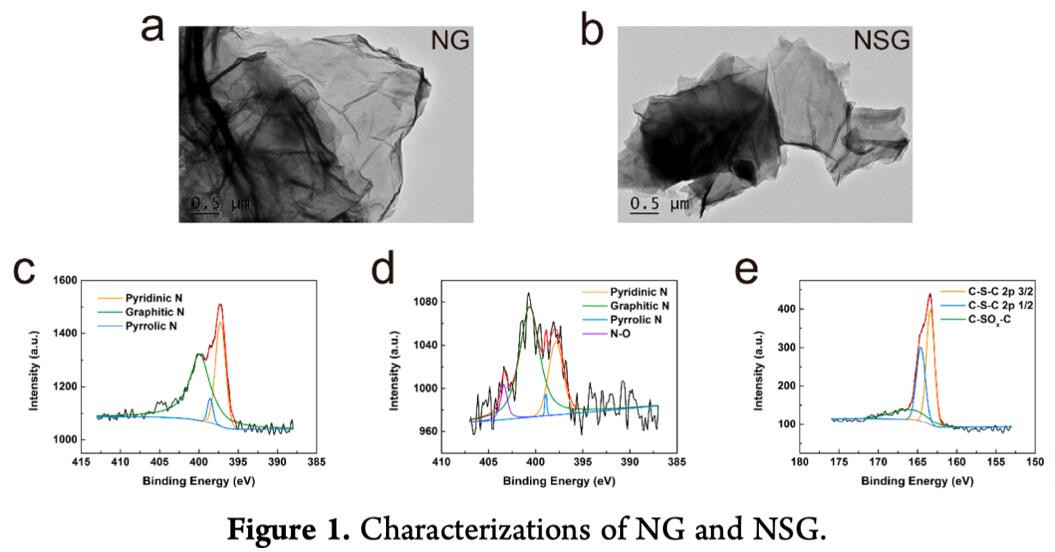
首先,作者成功合成了NG和NSG,并由TEM图像和XPS光谱证实(Figure 1)。由Figure 1a和1b所示,NG和NSG都具有与GO相似的薄膜形态。NSG和NG中N 1s的高分辨光谱被去卷积为特征峰,包括吡啶N,吡咯N和石墨N,结合能分别为398.56,397.24和399.89 eV(Figure 1c和1d)。NSG的N-O峰非常弱(403.37 eV)。NSG中S 2p的高分辨光谱被解卷积为C-S-C 2p 3/2,CS-C 2p 1/2和C-SO x -C,结合能分别为163.35、164.58和166.02 eV(Figure 1e)。
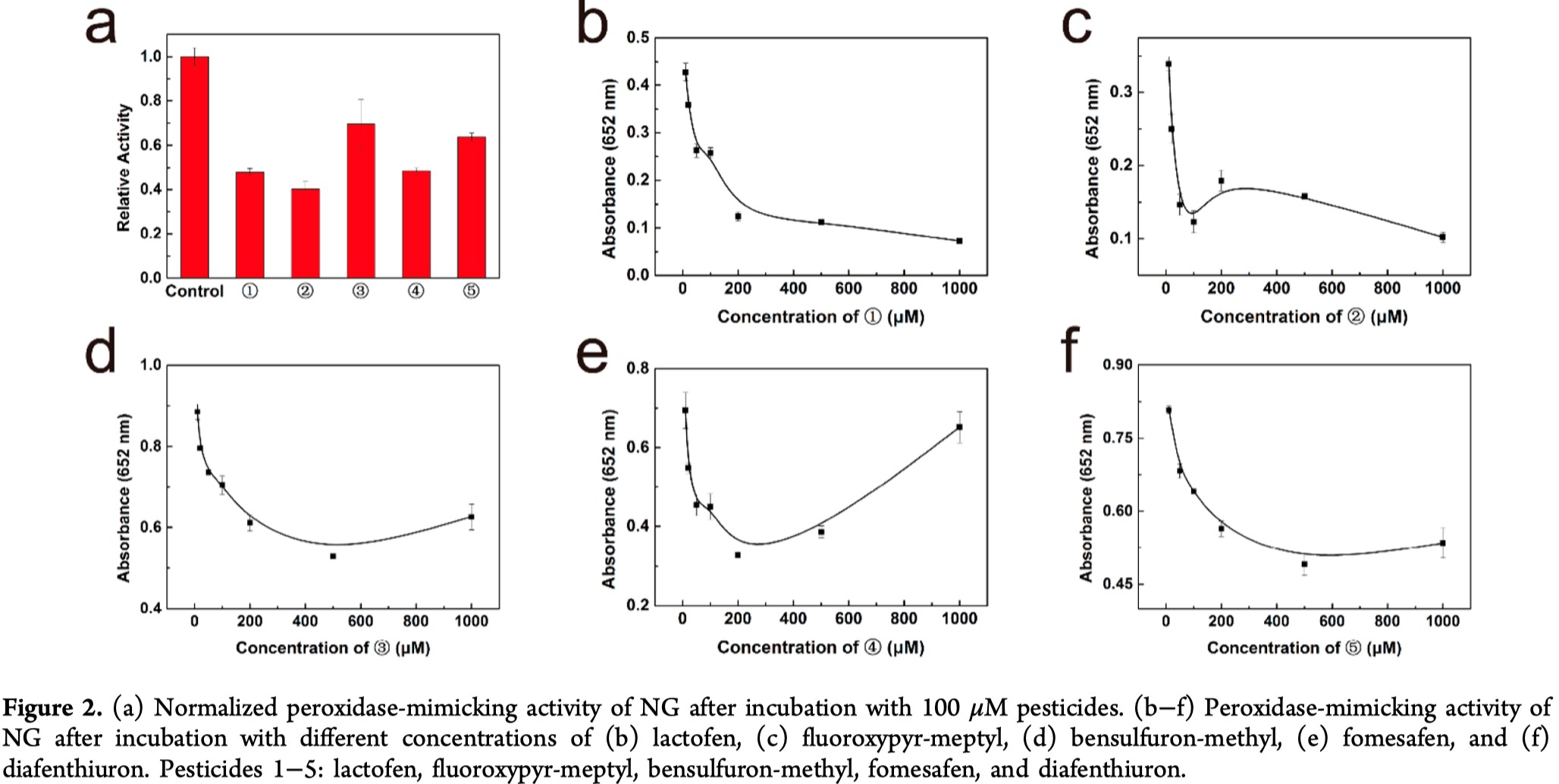
接下来,作者通过在过氧化氢存在下催化TMB的氧化来研究GO,NG和NSG的过氧化物酶模拟活性。所有三种材料均在652 nm处显示出特征吸收峰,表明其具有良好的过氧化物酶模拟活性(详见SI)。然后,作者评估了农药对三种石墨烯过氧化物酶模拟活性的影响。如Figure 2a所示,100 μM的各种农药对这三种纳米酶有不同的影响。对于NG和NSG来说,所有的农药均会抑制他们的过氧化物酶模拟活性,这是由于石墨烯对具有芳香结构的农药的吸附。对于GO,lactofen和bensolfuron-methyl的抑制作用可以忽略不计,而fomesafen甚至可以增强其过氧化物酶模拟活性。这可能是因为fomesafen的酸性有利于TMB的吸附而导致的。
作者进一步研究了不同浓度农药的抑制作用。Figure 2b-f显示了与不同浓度的农药孵育后NG,GO和NSG的过氧化物酶模拟活性。随着农药浓度的增加,各石墨烯在652 nm处的吸光度呈下降趋势,说明了农药对酶活性的抑制作用。应该注意的是,当农药浓度高达500和1000 μM时,吸光度反而会增加。这是因为这些农药的酸度有利于TMB在纳米酶上的吸附,从而导致更好的过氧化物酶模拟性能,再加上这些农药的不良溶解性也可能有助于吸光度的增加。基于这些结果,我们证明了不同的农药对这三种纳米酶具有不同的调节作用。
为了进一步研究基于石墨烯的纳米酶与农药之间的吸附相互作用,作者进行了分子动力学计算,来探究活性位点如何被农药阻断。根据之前的研究,NG中的石墨N和GO中的羧基被验证为模拟过氧化物酶的催化活性位点。因此,作者构建了具有石墨N和带有羧基的GO的NG模型。对于NSG模型的实验结果表明,NSG的活性并未提高,但随着氮和硫共掺杂而有所降低,作者假设靠近噻吩S的石墨N是活性位点,并构建了三种可能的模型(详见SI)。然后,作者对五种农药在这些掺杂的石墨烯表面上的吸附进行了计算,优化后的结果阐明了农药在石墨烯表面上的可能结合位点和方向。在NG和NSG中,农药通过π-π堆积相互作用吸附在NG和NSG的表面上,将那些活性石墨N位点封闭,如Figure 3所示。对于GO,农药也通过π-π堆积相互作用吸附在GO的表面,将羧基封闭。除π-π堆积相互作用外,fomesafen和羧基之间也可以形成氢键,从而导致更高的亲和力和更强的抑制作用。
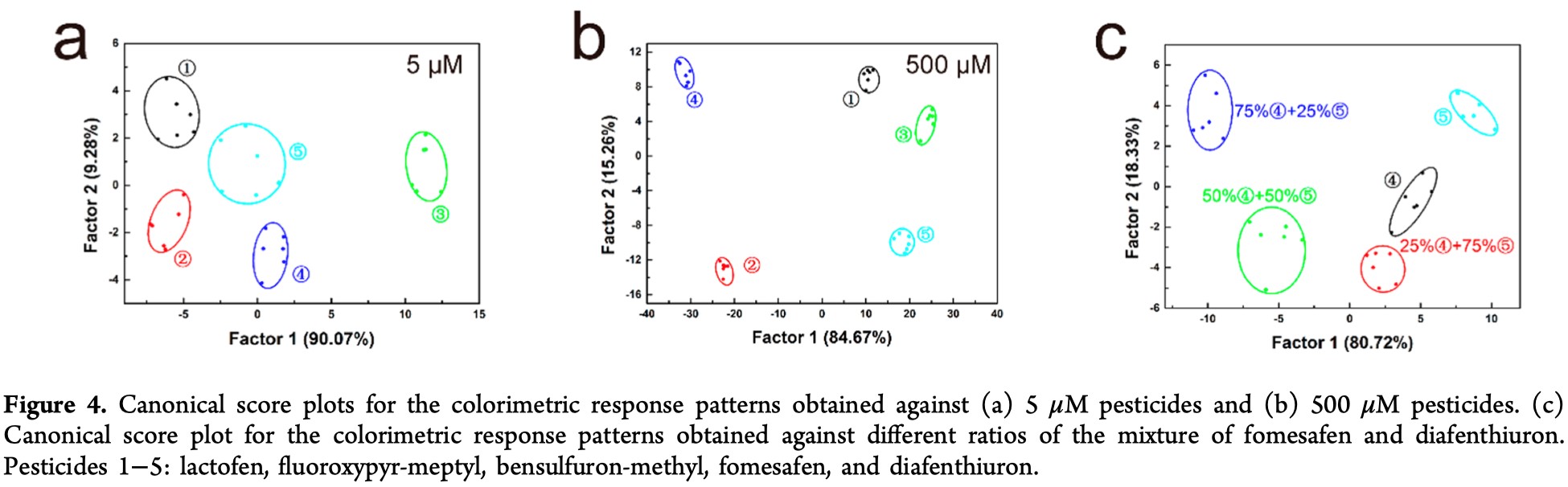
确定了纳米酶对各农药的响应不同之后,作者将这三种纳米酶用于构建传感器阵列来区分相同浓度的不同农药。通过收集A/A0值构建比色响应模式,并通过线性判别分析(LDA)将比色响应模式转换为2D典型分数图。由Figure 4a和4b可看出,在5-500 μM的宽浓度范围下,五种农药被很好的分成五个组,并且跟彼此区分的很开。
然后作者验证了其区分两种不同比例混合农药的可行性。Fomesafen和diafenthiuron都是白色粉末,且都可以喷洒在大豆田中,仅通过肉眼很难区分它们的混合物。作者设计了不同的比例,并用传感器阵列对其进行区分(Figure 4c)。具有不同摩尔比的混合物被很好的分成了五个组,并且彼此分离,这证明了传感器阵列对农药的多重检测能力。
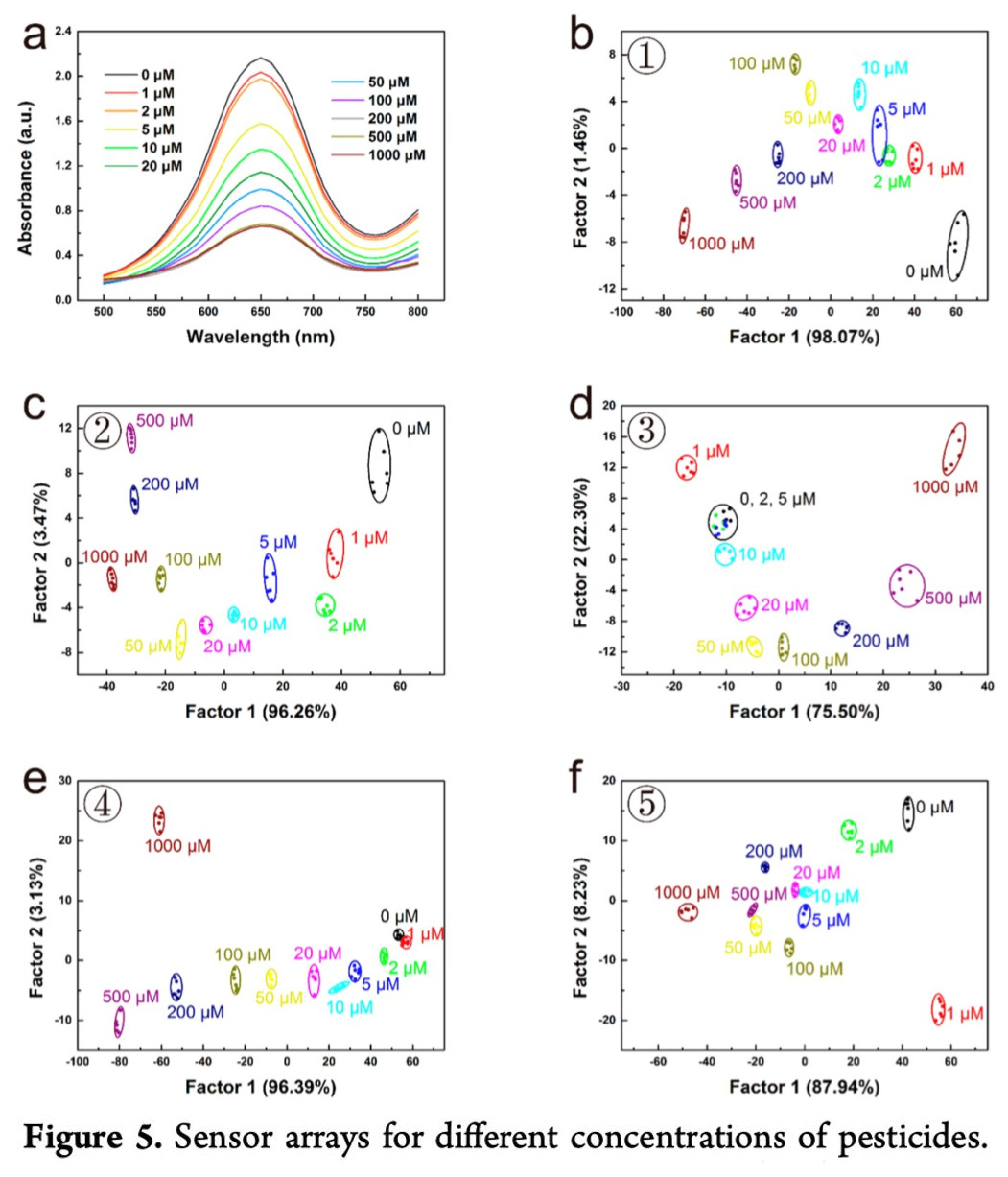
此外,作者还使用传感器阵列来区分每种农药的不同浓度(0至1000μM的11种浓度)。Figure 5a显示了在与不同浓度的农药一起孵育后,在过氧化氢存在下,NG催化的TMB的吸收光谱,并通过LDA获得了针对不同农药的2D典型评分图。对于lactofen,除了2和5 μM,其他浓度可以完全分离。对于bensulfuron-methyl,0、2和5 μM合并为一组,但九个组彼此分开。对于fluoroxypyr-meptyl,fomesafen和diafenthiuron,所有11种浓度均被明确区分。因此,纳米酶传感器阵列在区分大多数农药的不同浓度时表现出良好的性能。
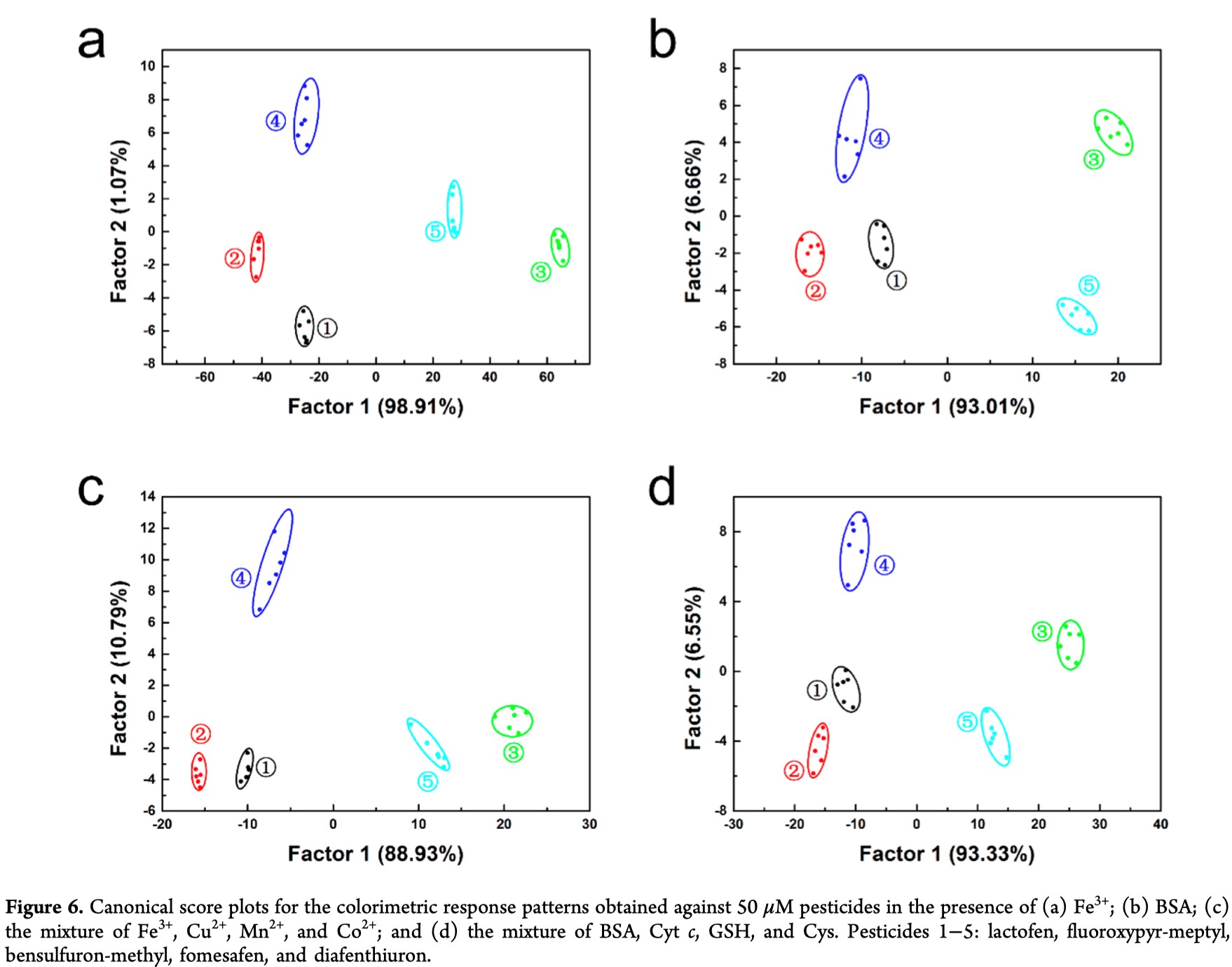
为了进一步验证传感器阵列的实际应用,作者研究了在存在干扰物的情况下区分农药的可行性。金属离子,生物硫醇和蛋白质都可能会影响石墨烯的过氧化物酶模拟活性。如Figure 6所示,在Fe3+;BSA;Fe3+/Cu2+/Mn2+/Co2+的混合物;以及BSA/Cyt c/GSH/Cys的混合物的分别存在下,该传感器阵列都成功地区分了50 μM的不同农药。这些结果证明了在存在干扰物的情况下区分不同农药的可行性。
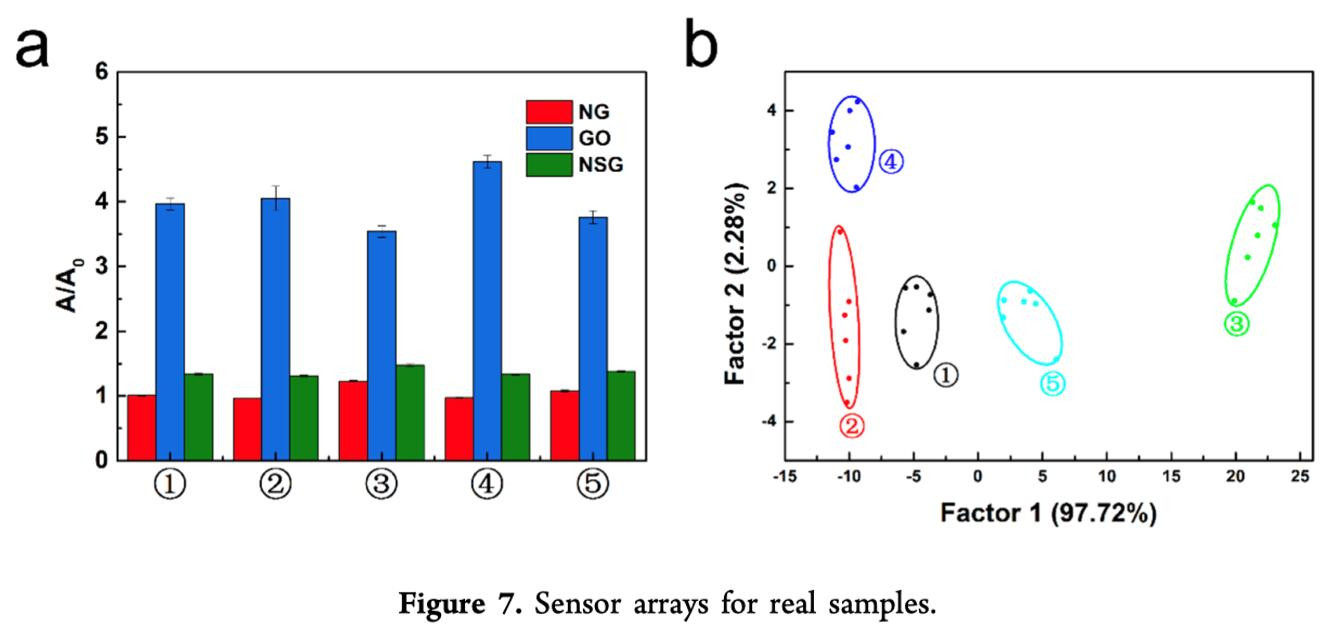
最后,作者探究了在实际样品中区分农药的可行性。他们将土壤样品均质后溶于水中,并通过离心来进一步处理。将上清液与不同的农药混合,得到5 mM的样品。如Figure 7a所示,每种农药都有特定的比色响应模式。通过LDA将比色响应模式转换为2D典型分数图(Figure 7b),可以看到五种农药被很好地分为五类。该结果证明了通过纳米酶传感器阵列区分真实样品中农药的可行性。因此,无论是在干扰物的存在下还是在实际样品中,对农药的成功判别都验证了传感器阵列进行实际应用的可能性。
结语
南京大学的魏辉教授课题组基于杂原子掺杂的石墨烯构建了纳米酶传感器阵列。在芳香族农药的存在下,纳米酶的活性位点被吸附而掩盖,导致其模拟过氧化物酶活性降低。制备的纳米酶传感器阵列在区分五种不同农药和每种农药的不同浓度方面均表现出良好的性能。此外,作者还验证了区分两种混合农药的不同比例和实际样品中农药的可行性。这项工作提供了一种交叉响应且成本经济的方法来检测芳香族农药,并有望将这一方法应用于检测更多农药中。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.