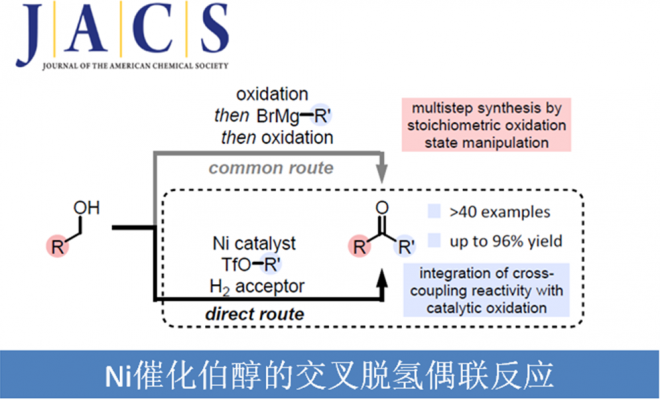
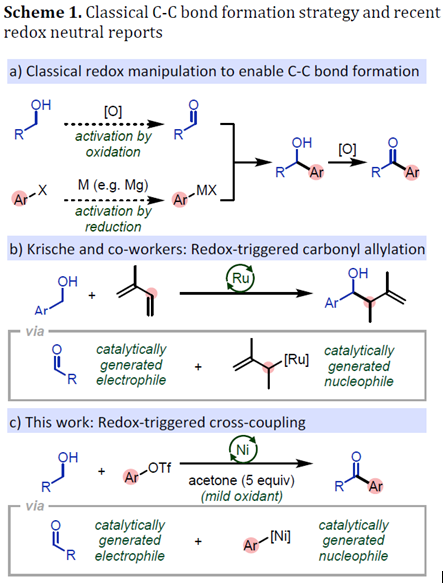
格氏试剂与醛的反应是C-C键形成最重要策略之一。其中,醛是通过醇发生氧化反应得到的,而格式试剂是由等当量的有机卤化物与金属Mg发生还原反应制得,最后格氏试剂再与醛反应得到产物酮也需要氧化反应。因此,合成产物酮相当于经历了3次氧化还原步骤。这种传统的制备酮的反应原子利用率较低,造成了严重的经济浪费(Scheme 1a)。最近,Krische课题组报道的Rh催化醇与二烯直接发生羰基烯丙基化反应。该策略将多重氧化反应与构建复杂产物转化为简单的催化步骤,克服了传统方法中原子利用率低的问题(Scheme 1b)。受到该报道的启发以及之前的工作,加拿大渥太华大学Stephen G. Newman团队报道了Ni催化伯醇的交叉脱氢偶联反应。相关研究成果发表于
Ketone Synthesis by a Nickel-Catalyzed Dehydrogenative Cross-Coupling of Primary Alcohols
Verheyen, T.; van Turnhout, L.; Vandavasi, J. K.; Isbrandt, E. S.; Borggraeve, W. M. D.; Newman, S. G.* J. Am. Chem. Soc. 2019, Just Accepted Manuscript
DOI: 10.1021/jacs.9b03280
论文作者介绍:
论文作者:Stephen G. Newman 助理教授
教育背景:
- BSc, Dalhousie University
- PhD, University of Toronto
- NSERC Postdoctoral Fellow, MIT
获奖情况:
- 2007, CSC Silver Medal
- 2008, University Medal in Chemistry
- 2008, Dalhousie University Silver Medal
- 2011, Boehringer Ingelheim Prize
- 2013, UofT Chair’s Doctoral Medal
- 2015, Thieme Chemistry Journal Awardee
- 2016, Visiting Professor – KU Leuven
- 2016, John Charles Polanyi Prize
- 2018, Ontario Early Researcher Award
- 2019, CNC-IUPAC Travel Award
- 2014-2019, Tier 2 Canada Research Chair
研究方向:Transition metal catalysis, flow chemistry, green chemistry strategies
论文概要:
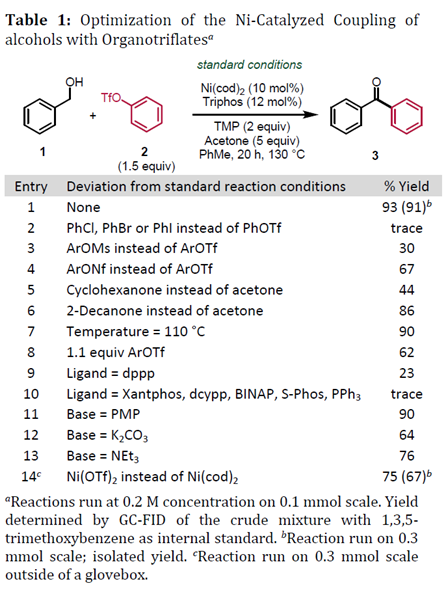
以苄醇1和三氟甲磺酸苯酯2为模板底物,作者对反应条件进行反复筛选,确定最优条件(Table 1):10 mol% Ni(cod)2和12 mol% Triphos为催化剂,TMP为碱,5 equiv丙酮为氢受体,甲苯为溶剂,在130 ℃条件下反应20 h,能以93%的收率得到相应产物。
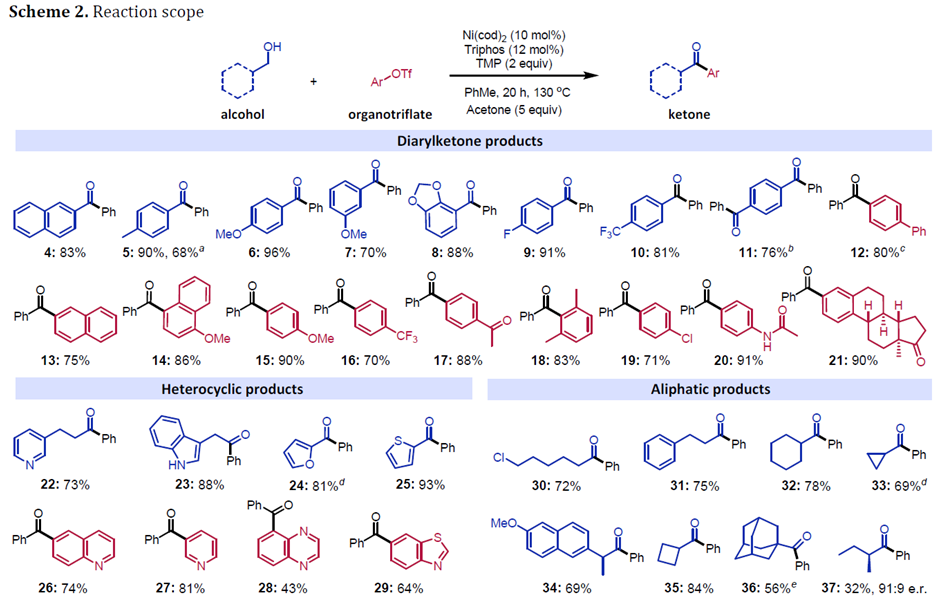
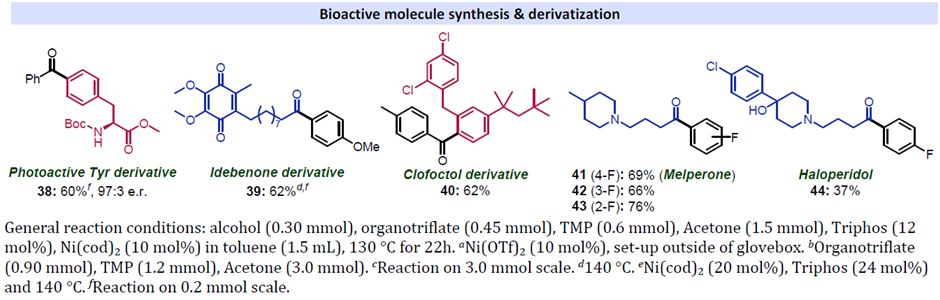
 在最优反应条件下,作者对交叉偶联反应的底物范围进行了考察(Scheme 2)。各种芳基取代的醇、含芳基氯、酰胺、雌酮骨架的醇、各种杂环醇、各种脂肪醇如环己基醇、环丙基醇、环丁基醇以及1-金刚烷甲醇均能较好的适应反应条件,能以良好的收率得到相应产物。各种芳基取代、杂环取代的三氟甲磺酸酯也具有良好的耐受性,能以较高的收率得到相应产物。通过简单的衍生反应,作者可以合成具有光学活性的酪氨酸衍生物38和含酮抗精神病药41和44。同时,阿尔茨海默氏症治疗药艾地苯醌和抗菌药可转化为新型酮39和40。
在最优反应条件下,作者对交叉偶联反应的底物范围进行了考察(Scheme 2)。各种芳基取代的醇、含芳基氯、酰胺、雌酮骨架的醇、各种杂环醇、各种脂肪醇如环己基醇、环丙基醇、环丁基醇以及1-金刚烷甲醇均能较好的适应反应条件,能以良好的收率得到相应产物。各种芳基取代、杂环取代的三氟甲磺酸酯也具有良好的耐受性,能以较高的收率得到相应产物。通过简单的衍生反应,作者可以合成具有光学活性的酪氨酸衍生物38和含酮抗精神病药41和44。同时,阿尔茨海默氏症治疗药艾地苯醌和抗菌药可转化为新型酮39和40。
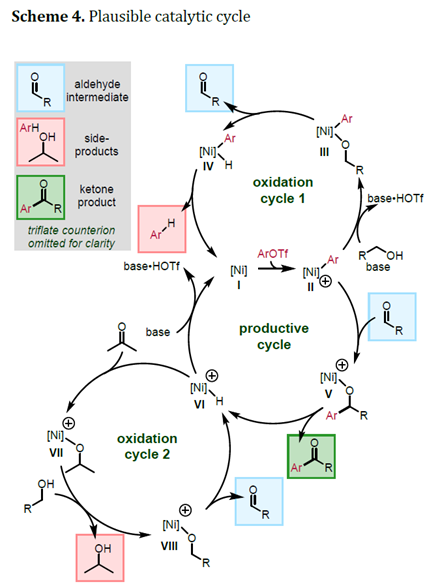
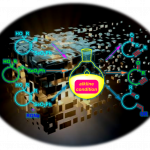
紧接着,作者做了一系列对照试验。通过对照实验的机理,作者推测可能的机理:首先,Ni(0)催化剂I与有机三氟甲磺酸酯反应生成氧化加成中间体II。II与醇反应可形成醇盐III(氧化循环1)。III发生β-氢消除反应可得到醛和Ni-氢化物IV, IV发生还原消除可生成I和还原的有机三氟甲磺酸酯。另一方面,芳基镍II可与醛发生插入反应生成醇盐V。V发生还原消除可生成产物酮和Ni-氢化物IV。Ni-氢化物IV可还原丙酮添加剂生成醇和络合物VII,生成的醇可以继续与起始原料的醇结合生成VIII。VIII经历β-氢消除过程生成醛,同时金属氢化物VI再生(氧化循环2)。
论文总结评价:
加拿大渥太华大学Stephen G. Newman团队报道了Ni催化伯醇的交叉脱氢偶联反应,能以高收率得到一系列酮。该反应原子利用率高,为交叉脱氢偶联反应提供了一种新的途径。
参考文献:
- Anastas, P.; Eghbali, N. Chem. Soc. Rev. 2010, 39, 301. DOI: 10.1039/B918763B
- Ketcham, J. M.; Shin, I.; Montgomery, T. P.; Krische, M. J. Angew. Chem., Int. Ed. 2014, 53, 9142. DOI: 10.1002/anie.201403873
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.