- 概要
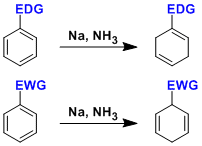
芳香族化合物在液氨/醇的混合溶液中,跟碱金属(Li, Na, K)或者碱土金属(Ca, Mg)反应的话,会被还原成1,4-环己二烯。对单取代的苯来说,得到反应产物根据取代基是供电性(EDG)的还是吸电性(EWG)的不同而不同。
α,β-不饱和羰基化合物,共轭二烯,炔烃等也能用该反应还原。特别是炔烃作为底物反应的话,可以选择性得到E-式烯烃。 (参考:炔烃的Birch还原)。该反应也可以用于脱苄基・苯磺酰基等保护基。
Li/DBB(4,4′-di-t-bulylbiphenyl)、Na/naphthalene等更加温和的还原条件相比于使用液氨的Birch反应来说对官能团的耐受性更强。
如果用短脂肪链的胺替代液氨的话,胺作为质子源,可以相对升高温度反应,其还原能力也随之变强(Benkeser还原)。
- 参考文献
・Birch, A. J. J. Chem. Soc. 1944, 430.
・Birch, A. J. J. Chem. Soc. 1945, 809.
・Birch, A. J. J. Chem. Soc. 1946, 593.
・Birch, A. J. J. Chem. Soc. 1947, 102, 1642.
・Birch, A. J. J. Chem. Soc. 1949, 2531.
<Benkeser reduction>
・ Benkeser, R. A.; Robinson, R. E.; Landesman, H. J. Am. Chem. Soc. 1952, 74, 5699. DOI: 10.1021/ja01142a041
・ Benkeser, R. A.; Robinson, R. E.; Sauve, D. M.; Thomas, O. H. J. Am. Chem. Soc. 1955, 77, 3230. DOI: 10.1021/ja01617a025
・ Benkeser, R. A.; Belmonte, F. G.; Kang, J. J. Org. Chem. 1983, 48, 2796. DOI: 10.1021/jo00165a003
<review>
・Watt, G. W. Chem. Rev. 1950, 46, 317. DOI: 10.1021/cr60144a003
・Birch, A.J. Quart. Rev. 1950, 4, 69.
・Birch, A.J.; Smith, H. Quart. Rev. 1958, 12, 17.
・Kaiser, E. M. Synthesis 1972, 391. DOI: 10.1055/s-1972-21889
・Caine, D. Org. React. 1976, 23, 1.
・Hook, J. M.; Mander, L. N. Nat. Prod. Rep. 1986, 3, 35. DOI: 10.1039/NP9860300035
・Schultz, A. G. Acc. Chem. Res. 1990, 23, 207. DOI: 10.1021/ar00175a001
・Mander, L. N. Comprehensive Organic Synthesis 1991, 8, 489.
・Rabideau, P. W.; Marcinow, Z. Org. React. 1992, 42, 1.
・Birch, A. J. Pure Appl. Chem. 1996, 68, 553. doi:10.1351/pac199668030553
・Schultz, A. G. Chem. Commun. 1999, 1263. DOI: 10.1039/A901759C
・Subba Rao, G. S. R. Pure Appl. Chem. 2003, 75, 1443. [PDF]
・Donohoe, T. J.; Thomas, R. E. Nat. Protoc.2007, 2, 1888. doi:10.1038/nprot.2007.245
・Zimmerman, H. E. Acc. Chem. Res. 2012, 45, 164. DOI: 10.1021/ar2000698
- 反应机理
最终生成的烯烃的位置选择性,是由阴离子中间体的稳定性所决定的。EWG取代基能够稳定本位生成的阴离子中间体,而相反EDG取代基的话使得该中间体更不稳定 。(参考:J. Am. Chem. Soc. 1993, 115, 2205., Acc. Chem. Res. 2012, 45, 164.)
醇的添加是为了防止体系中生成的强碱NH2–引起的不可预料的异构化。
碱金属对于苯环的还原反应的相对速度 Li(360)>Na(2)>K(1)。
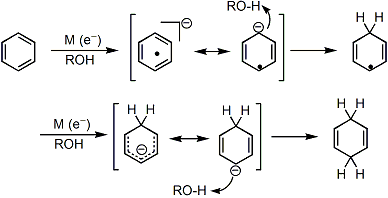
-
反应实例
Birch还原中生成的由吸电子取代基稳定化的碳阴离子会接着跟卤烷,醛等亲电试剂反应生成碳-碳键。以下给出了一个实例 [1]。
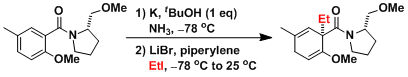
- 实验步骤
吡咯类的Birch还原[2]
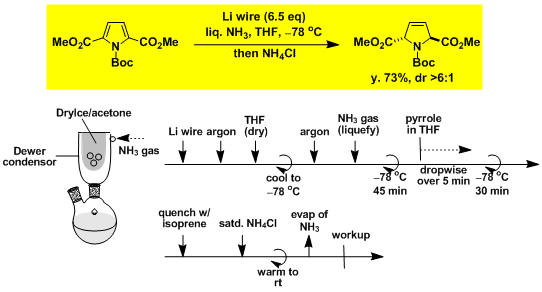
※氨气的沸点大约是-33℃、常用Dewer冷却器低温浓缩而不是Dimroth冷却器。
※聚四氟乙烯的搅拌子会在Birch还原条件下被腐蚀、变黑。最好用玻璃的搅拌子。
※对于锂金属丝、预先用戊烷洗去表面附着的油后,用剪刀剪成小块使用。
※如果有活性中间体生成的话,溶液颜色会变成深蓝色。
※异戊二烯经常作为自由基还原剂猝灭的目的而在本反应中被使用到。
-
实验技巧
- 参考文献
[2] Donohoe, T. J.; Thomas, R. E. Nat. Protoc. 2007, 2, 1888. doi:10.1038/nprot.2007.245