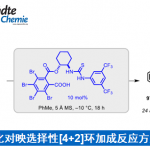
- 概要
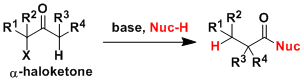
α-卤代酮受到醇盐的进攻、羰基的两个α位之间成键的同时生成酯基。如果用氢氧化钠做碱,则得到产物是羧酸。环状酮的情况下会缩环形成较小的环。
β-卤代酮发生同样的反应称作Homo-Favorskii重排、α位没有氢不发生烯酮化的底物发生的反应称作Quasi-Favorskii重排。
- 基本文献
・Favorskii, A. E. J. Russ. Phys. Chem. Soc. 1894, 26, 590.
・Favorskii, A. E. J. Russ. Phys. Chem. Soc. 1905, 37, 643.
・Favorskii, A. E. J. Ptakt. Chem. 1913, 88, 658.
・Favorskii, A. E.; Bozhovskii, V. N. J. Russ. Phys. Chem. Soc. 1914, 46, 1097.
・Fort, A. W. J. Am. Chem.Soc. 1962, 784, 2620, 4979.
・Review: Kende, A. S. Org. React. 1960, 11, 261.
- 反应机理
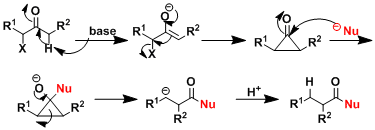
反应生成的中间体是环丙醇,它受到醇盐或是氢氧根离子的亲核进攻,环被打开。
- 反应实例
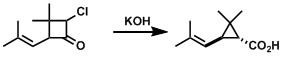
环状酮的Favorskii重排,会发生具有代表性的环缩小反应[1]。
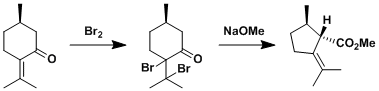
(+)-epoxydictymene合成[2]的第一步反应。
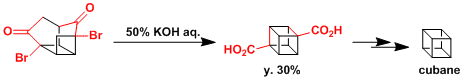
Eaton等人将这一反应作为Cubane全合成[3]的关键步骤。
- 实验步骤
- 实验技巧
- 参考文献
[2] Jamison, T. F.; Shambayati, S.; Crawe, W. E.; Schreiber, S. L. J. Am. Chem. Soc. 1997, 119, 4353. DOI: 10.1021/ja970022u
[3] Eaton, P. E. et al. J. Am. Chem. Soc. 1964, 962, 3157.