本文作者:CZM
硅是地壳中含量(26.4%)仅次于氧的元素。普通生活中接触到的含硅物质最常见的包含:石英、水晶、玻璃、硅基芯片等。有机合成中常见的试剂如氯硅烷以及其衍生化的产物参与的反应,如Mukaiyama Aldol、Mukaiyama-Micheal 加成、Hiyama偶联、Stetter反应、Flemiing氧化等。这些试剂主要参与的是极性反应。而硅试剂参与的自由基反应则以其具有的独特的性质,在方法学研究中运用日益广泛。
1.1:硅-碳性质对比
硅与同族的碳元素性质相近。但也有很大的不同:首先从元素结构上说:硅的共价半径为1.17埃,而碳的共价半径为0.77埃。这个差别使得硅化合物的基团间排斥少,电子云间的β-立体电子位阻效应小,使得成为α-芳基迁移无法实现的一个原因之一。[1]
甲基自由基的构象为:平面型的,而硅基自由基则为角锥型。如下图:
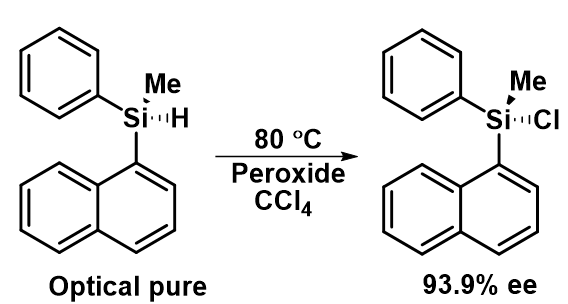
自由基的构象带来的问题是手性前体的立体构型保持与否问题。烷基C中心自由基很容易引起消旋。手性化合物的自由基中间体的消旋过程存在两种可能性:中间体自由基为平面构型(极少情况)或者形成的自由基发生快速翻转。手性硅化合物产生的硅基自由基中间体则会构象保持。计算化学表明结构最为简单的SiH3·室温下的翻转能垒为+5.4kcal,一旦增加位阻与极性基团,翻转能垒更高[2],传统解释认为这或许与Si-H键中硅的杂化轨道中p成分含量相关。
1.2:硅的α-效应、β-效应
与碳对比,硅元素处于第三周期,存在空的3d轨道,这对α-位自由基具有共轭稳定化作用:自旋离域产生的稳定性:(TMS)3Si• > (TMS)2Si(•)Me > (TMS)Si(•)Me2 > Me3Si•。空d轨道的存在使得硅基化合物存在一个著名的β-效应,如下的碳正离子会与硅正离子存在一个桥状过渡态,最终主要的结构为硅中心的硅基正离子重排产物。硅基的α-稳定性为0.5kcal/mol,而β效应稳定化能为3kcal/mol。
加上最后热力学驱动形成比烷基自由基稳定的硅中心自由基,最终的稳定化能将更高,这也是β效应促进重排的重要原因。
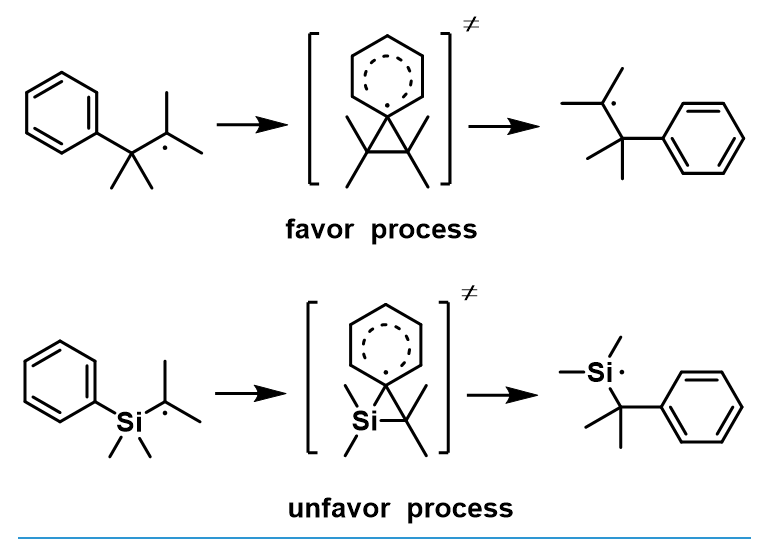
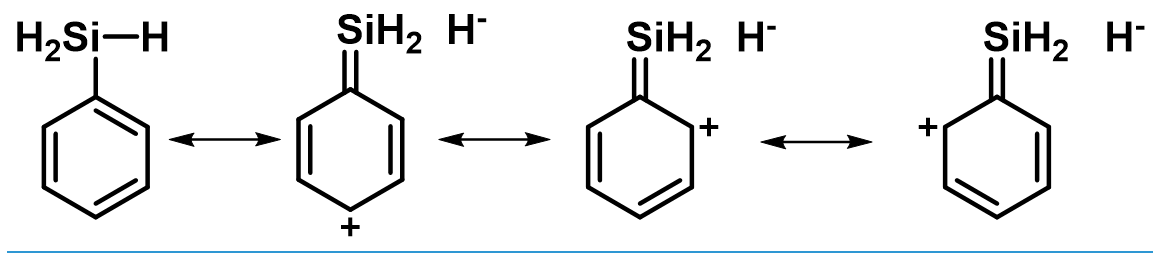
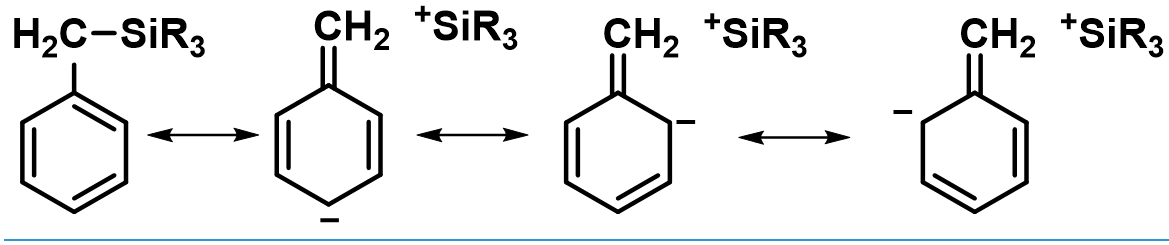
硅的α-效应在芳基取代中的定位效应表现出类似吸电子取代基的性质,即:在间位芳香亲电取代,而苄硅由于存在β-效应则会表现出相反的:邻、对位定位效应:
硅定位效应:α效应:
硅定位效应:β效应:
硅的β效应使得相应的活性中间体极易重排。那么对应的α效应引起的重排也有一些数据:
取代基中α-迁移的难易程度为:Ph>H>>Me,其中苯基的迁移能垒约为0~1.5kcal。
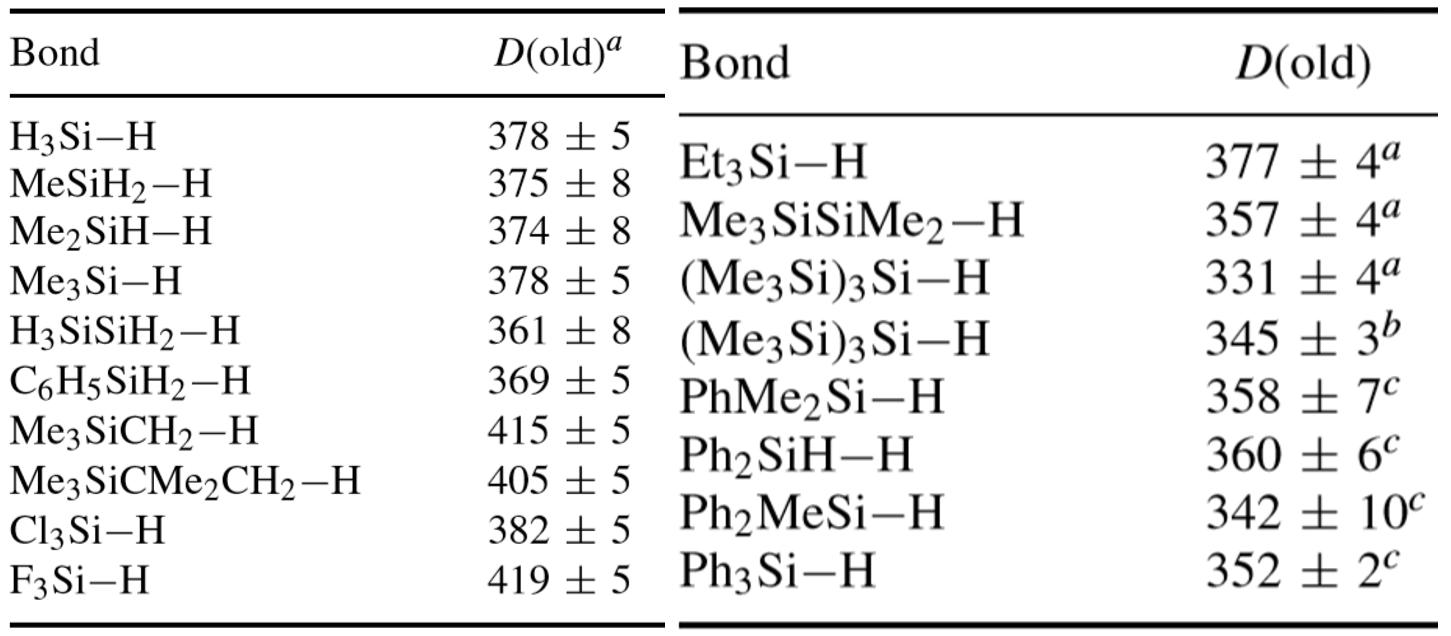
1.3:Si-H键的键解离能
键解离能在自由基化学中衡量一个键均裂额能力,Si-H键的键解离能(BDE)大小规律有助于指导HAT过程中产生硅基自由基的能力。硅基自由的化学性质则会在下面一章节中详细描述。[3]
列出上面的Si-H键的BDE。强烈自燃试剂硅烷的BDE为90kcal/mol,增加甲基对BDE没有明显变化;而增加苯基则会显著降低BDE,平均每增加一个苯基会降低2kcal/mol的键能。每增加一个TMS也会降低BDE:3kcal/mol。但是增加F、Cl等强拉电子基团时,则会增加BDE,平均每个F会增加3kcal/mol。这些数据将有助于针对不同的底物设计出相应的取代基来实现速率匹配。
1.4:硅自由基的形成
常见的自由基中,主要见到的是碳中心自由基,这一方面与其合成应用的价值导向使得碳自由基备受关注相关外,其次还与相对于其它原子中心自由基(O、N、Cl、Br),碳中心自由基相对较稳定从而较容易形成有关。与碳同族的硅自由基其实相比碳自由基具有类似的形成方式,且更容形成,接下来将对比两者的常见的形成方式。
第一种方式是直接的氢转移过程。常见的Si-H键能为90kcal/mol,而常见的普通烷基C-H键在95kcal以上,而N-H和O-H则是在105kcal/mol附近。因而其它类型自由基中间体对Si-H的氢转移过程较快也较容易实现,常见的主要为叔丁氧自由基拔氢,速率接近溶剂扩散速率。Si-H除了被氢受体实现氢转移外,还可以被强氧化剂单电子氧化实现。
其次是Si-Y键的均裂,这个过程可以是光照实现也可以是热裂解,这个主要是受Y基团的影响。常见的是Si-Si键的紫外光照均裂,而Si-B键则可以在300nm以上的条件下实现均裂产生相应的Si自由基与硼自由基。
参考文献
- [1] J. Am. Chem. Soc. 1977, 99, 26, 8402. doi.org/10.1021/ja00468a005
- [2] Acc. Chem. Res. 1981, 14, 8, 246. doi.org/10.1021/ar00068a004
- [3] J. Am. Chem. Soc. 1994, 116, 18, 8304. doi.org/10.1021/ja00097a042
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!




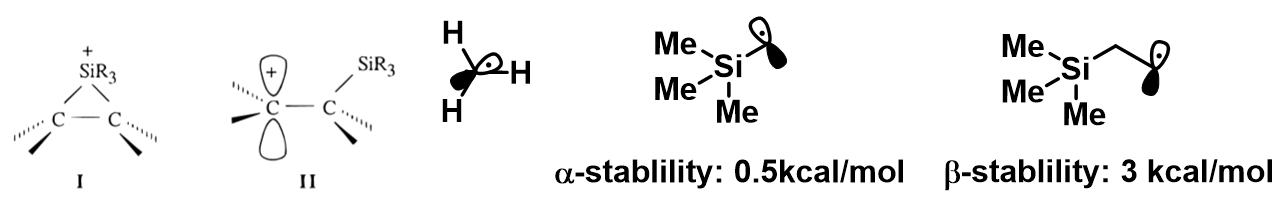

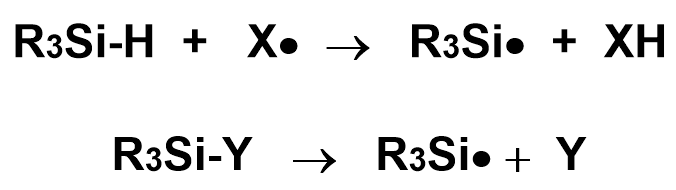

















No comments yet.