作者:杉杉
导读:
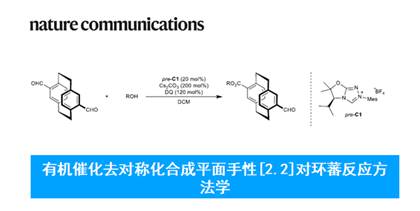
近日,捷克Charles大学的Jan Veselý课题组在Nat. Commun.中发表论文,报道一种全新的有机催化前手性二甲酰基[2.2]对环蕃 (diformyl[2.2]paracyclophanes)与醇的去对称化酯化反应方法学,涉及关键的Breslow中间体的形成,进而成功完成一系列平面手性[2.2]对环蕃(planar chiral [2.2]paracyclophanes)分子的构建。
Organocatalytic desymmetrization provides access to planar chiral [2.2]paracyclophanes
V. Dočekal, F. Koucký, I. Císařová, J. Veselý, Nat. Commun. 2024, 15, 3090. doi: 10.1038/s41467-024-47407-0.
正文:
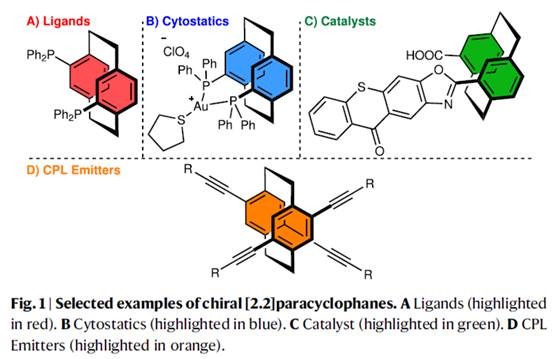
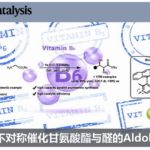
手性[2.2]对环蕃骨架广泛存在于各类配体、细胞因子抑制剂、催化剂、圆偏振光发射体等物质中(Fig. 1)。并且,诸多研究团队已经成功设计出多种利用对映体分离或各种拆分方法[1]构建手性[2.2]对环蕃分子的合成转化策略。然而,此类策略存在底物范围窄、收率低等弊端。受到钌催化不对称转移氢化反应方法学[2]以及手性N-杂环卡宾诱导的无金属有机催化去对称化反应方法学[3]相关研究报道的启发,这里,捷克Charles大学的Jan Veselý课题组报道一种全新的有机催化前手性二甲酰基[2.2]对环蕃与醇的去对称化酯化反应方法学,进而成功完成一系列平面手性[2.2]对环蕃分子的构建。
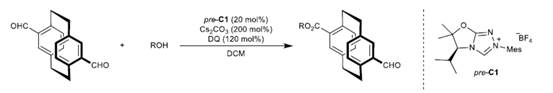
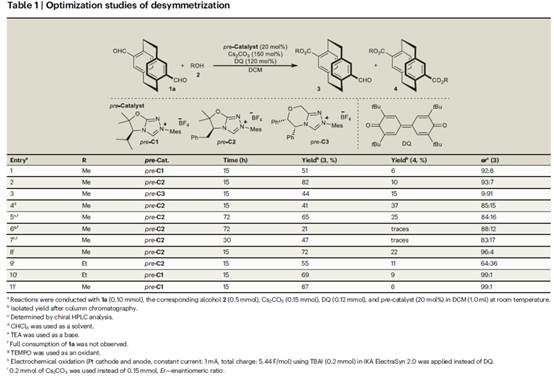
首先,作者采用二甲酰基[2.2]对环蕃衍生物1a与醇衍生物2作为模型底物,进行相关反应条件的优化筛选 (Table 1)。进而确定最佳的反应条件为:采用甲醇作为底物,pre–C1作为预催化剂,DQ (Kharash reagent, 3,3’5,5’-tetra-tert-butyldiphenoquinone)作为氧化剂,Cs2CO3作为碱,在DCM反应溶剂中,反应温度为室温,最终获得87%收率的产物3 (99:1 er)。
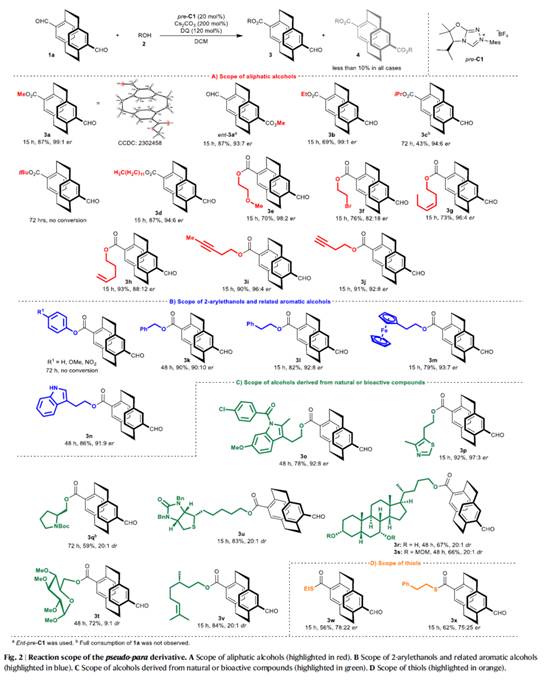
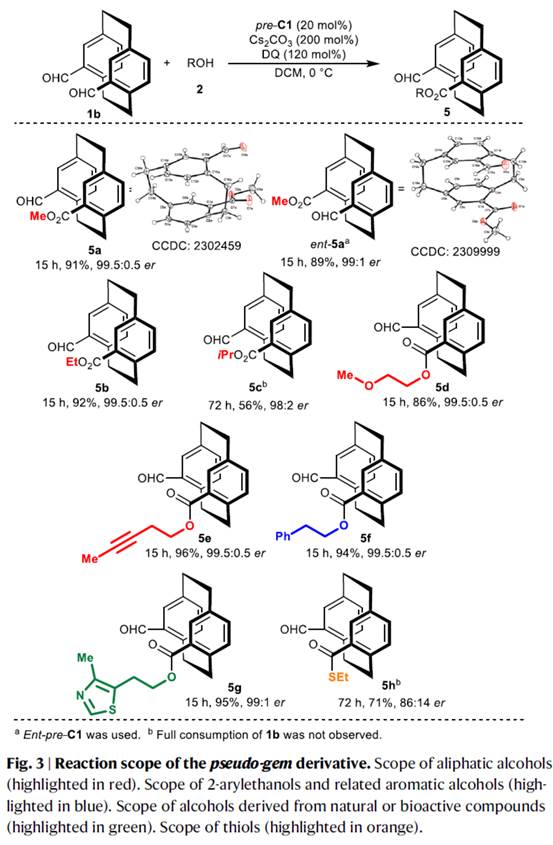
在上述的最佳反应条件下,作者分别对一系列pseudo–para derivative底物 (Fig. 2)以及pseudo–gem derivative底物 (Fig. 3)的应用范围进行深入研究。


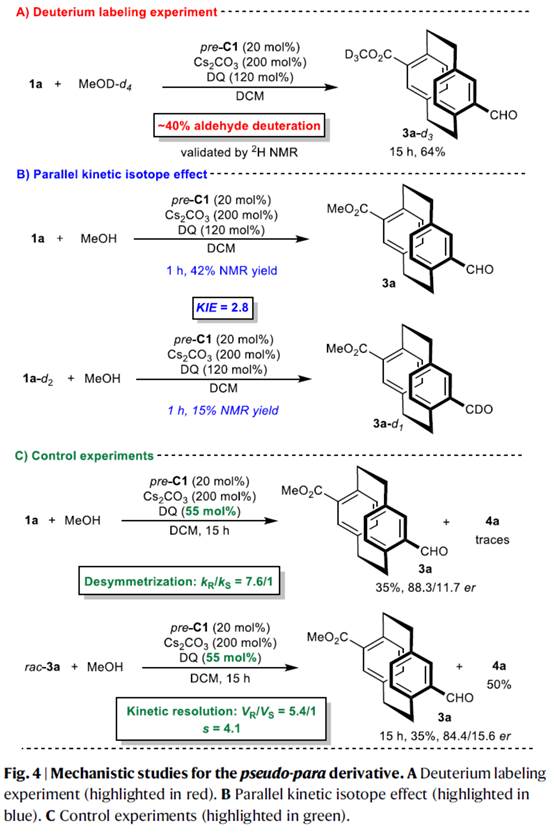
接下来,作者对上述去对称化酯化过程的反应机理进行进一步研究 (Fig. 4与Fig. 5)。

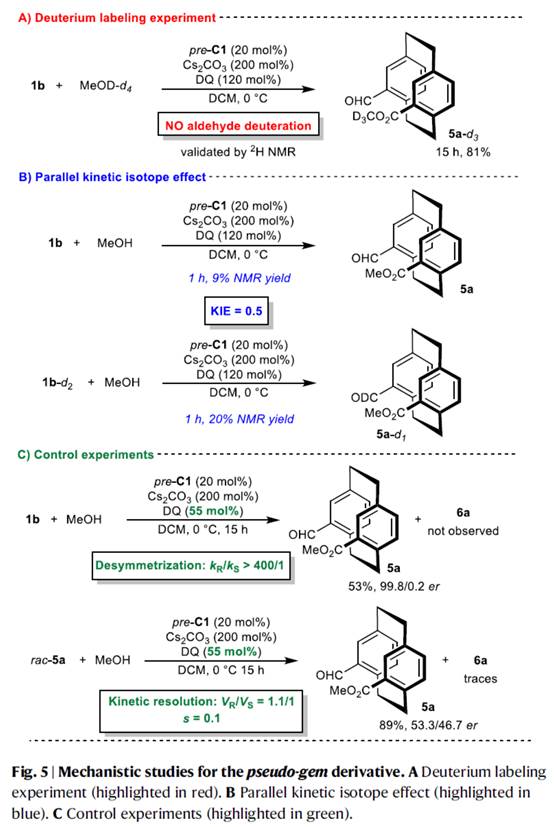

之后,该小组通过如下的一系列研究进一步表明,这一全新的去对称化酯化策略具有潜在的合成应用价值 (Fig. 6)。
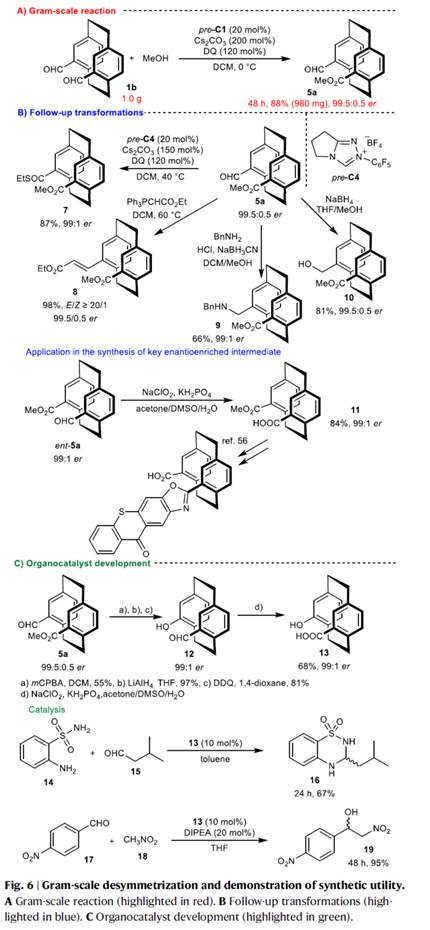
总结:捷克Charles大学的Jan Veselý课题组报道一种全新的有机催化前手性二甲酰基[2.2]对环蕃与醇的去对称化酯化反应方法学,进而成功完成一系列平面手性[2.2]对环蕃分子的构建。这一全新的去对称化合成转化策略具有操作简单、无需金属催化剂、底物范围广泛以及优良的官能团兼容性等优势。
参考文献:
- [1] M. L. Delcourt, S. Felder, S. Turcaud, C. H. Pollok, C. Merten, L. Micouin, E. Benedetti, J. Org. Chem. 2019, 84, 5369. doi:10.1021/acs.joc.9b00372.
- [2] M. L. Delcourt, S. Felder, E. Benedetti, L. Micouin, ACS Catal. 2018, 8, 6612. doi:10.1021/acscatal.8b01872.
- [3] R. Song, Y. Xie, Z. Jin, Y. R. Chi, Angew. Chem. Int. Ed. 2021, 60, 26026. doi:10.1002/ange.202108630.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.

















No comments yet.