作者:石油醚
导读:
近日,日本理化学研究所(RIKEN)的侯召民(Zhaomin Hou)教授课题组利用半夹心型稀土金属络合物为催化剂,通过联烯C(sp2)−H键选择性活化,首次实现了电子无偏的联烯与非活化烯烃的[2+2]环加成反应。该反应具有100%的原子经济性、出色的非对映选择性(d.r. > 19:1)、广泛的底物范围、良好的官能团耐受性等优点,为多官能团取代的甲基烯环丁烷化合物和环丁烯化合物的构建提供了一种高效、高区域和立体选择性的合成方法。相关工作发表在Angew. Chem. Int. Ed.上,日本理化学研究所侯召民主任研究员和丛雪丰研究员为该论文通讯作者,论文的第一作者为东京工业大学博士研究生徐文轩。
“Regio- and Diastereoselective Formal [2+2] Cycloaddition of Allenes with Amino-Functionalized Alkenes by Rare-Earth-Catalyzed C(sp2)–H Activation
Wenxuan Xu, Xuefeng Cong*, Kun An, Shao-Jie Lou, Zhenghua Li, Masayoshi Nishiura, Tetsuro Murahashi, Zhaomin Hou*
Angew. Chem. Int. Ed. 2022, ASAP. doi: 10.1002/anie.202210624”
正文:
环丁烷与环丁烯是非常重要的四元碳环化合物,它不仅是有机合成中的重要原料、中间体,也是天然产物、药物活性分子的重要结构单元。因此,发展高效、高选择性的合成四元碳环的方法受到了广泛关注。联烯作为一类含1,2-累积二烯基官能团的化合物,在与烯烃的[2+2]环加成反应中扮演了独特的角色。尽管分子内联烯与烯烃的[2+2]环加成反应得到了很好地发展,但是分子间的电子无偏的联烯与非活化的烯烃的[2+2]环加成反应仍未实现。
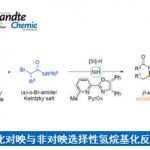
近日,日本理化学研究所(RIKEN)的侯召民(Zhaomin Hou)教授课题组长期致力于半夹心型稀土金属烷基化合物开发及其在烯烃聚合与C−H键活化反应中应用的研究(Acc. Chem. Res., 2015, 48, 2209−2220)。近年来,该半夹心型稀土金属烷基络合物的多样性也为催化剂的开发与设计及其在反应立体控制等方面的优异表现提供了可能(J. Am. Chem. Soc., 2020, 142, 5531−5537;Angew. Chem. Int. Ed., 2022, 61, e202115996.)。最近,该研究团队利用半夹心型稀土络合物为催化剂,通过对联烯C(sp2)−H选择性活化,实现了首例联烯与非活化烯烃的区域和立体选择性的[2+2]环加成反应。由于联烯独特的结构特点,该类化合物拥有多个反应位点,因而通常面临化学、区域和立体选择性等问题。该研究团队利用半夹心型稀土络合物独特的催化活性和选择性,实现了联烯C(sp2)−H键区域选择性的活化,随后利用胺基的配位导向作用,与非活化烯烃发生区域和立体选择性的环加成反应(图1)。
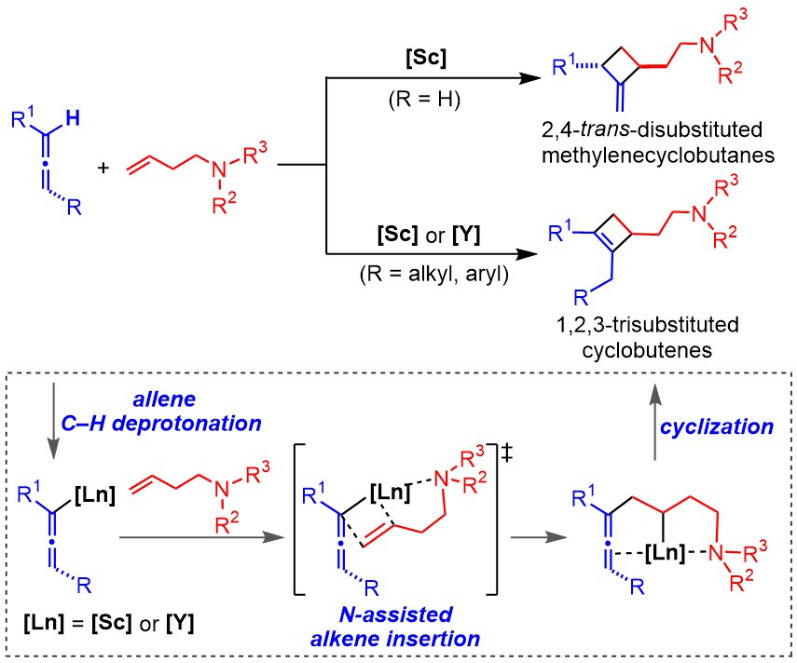
图1. 稀土金属催化联烯C(sp2)−H键活化与烯烃的非对映选择性的[2+2]环加成反应
作者选用单取代联烯与胺基官能化的烯烃作为底物,系统地考察了溶剂、催化剂和温度时间等因素对反应的影响,并得到了最佳反应条件。随后,作者以最优的Sc-1为催化剂的条件下对单取代联烯与胺基官能化的烯烃的底物普适性进行了详细的考察。如图2所示,不同官能团取代的单取代联烯1和胺基官能化的烯烃2均表现出高的反应活性,并单一选择性优异收率地得到反式选择性的2,4-双取代甲基烯环丁烷化合物。值得一提的是,该催化体系可以很好的兼容卤素、醚、硫醚、芳基、杂芳基以及硅基等官能团。

图2. 钪催化单取代联烯与烯烃的的[2+2]环加成反应(部分底物)
同时,在最优的反应条件下,作者也进行了1,3-双烷基联烯与烯烃的反应的底物普适性考察。如图3所示,不同官能团取代的1,3-双烷基联烯4和胺基官能化的烯烃2均表现出高的反应活性,与单取代联烯不同的是,该反应以优异的收率和区域选择性生成了1,2,3-三取代环丁烯化合物作为主产物。
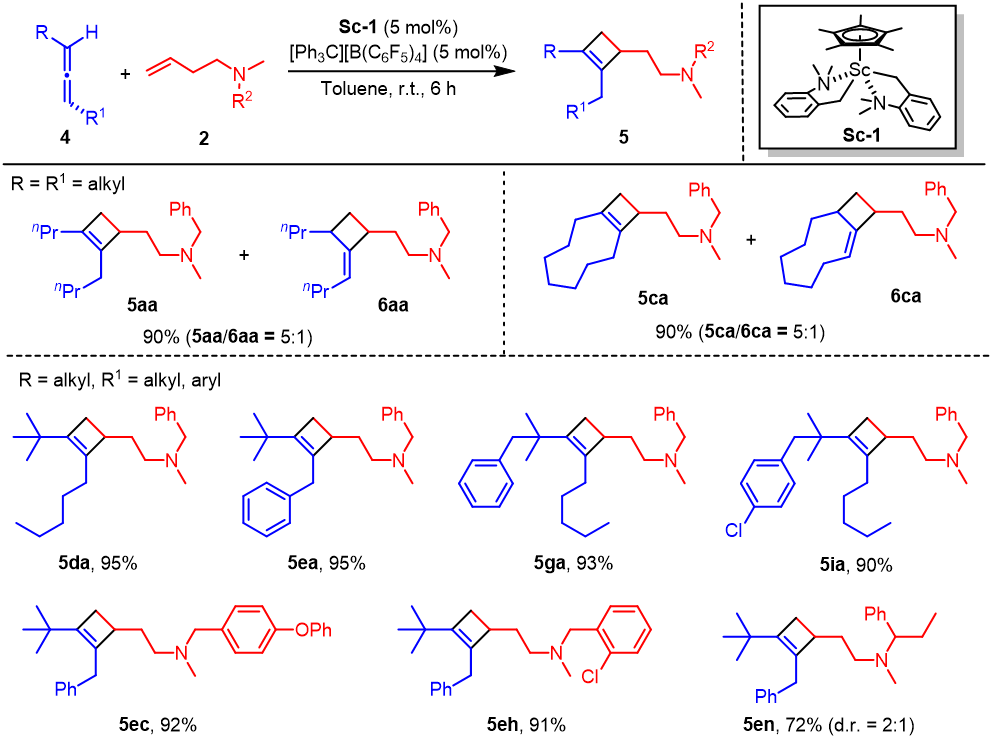
图3. 钪催化1,3-双烷基联烯与烯烃的的[2+2]环加成反应(部分底物)
而后,作者还对1-芳基-3-烷基联烯与烯烃的反应进行了考察。如图4所示,C5Me5配体络合的钇配合物对该反应显示了更好的选择性,具有优异的底物适用性,能够兼容含有不同官能团的1-芳基-3-烷基联烯4和烯烃2,以优异的收率和区域选择性得到1,2,3-三取代环丁烯化合物。
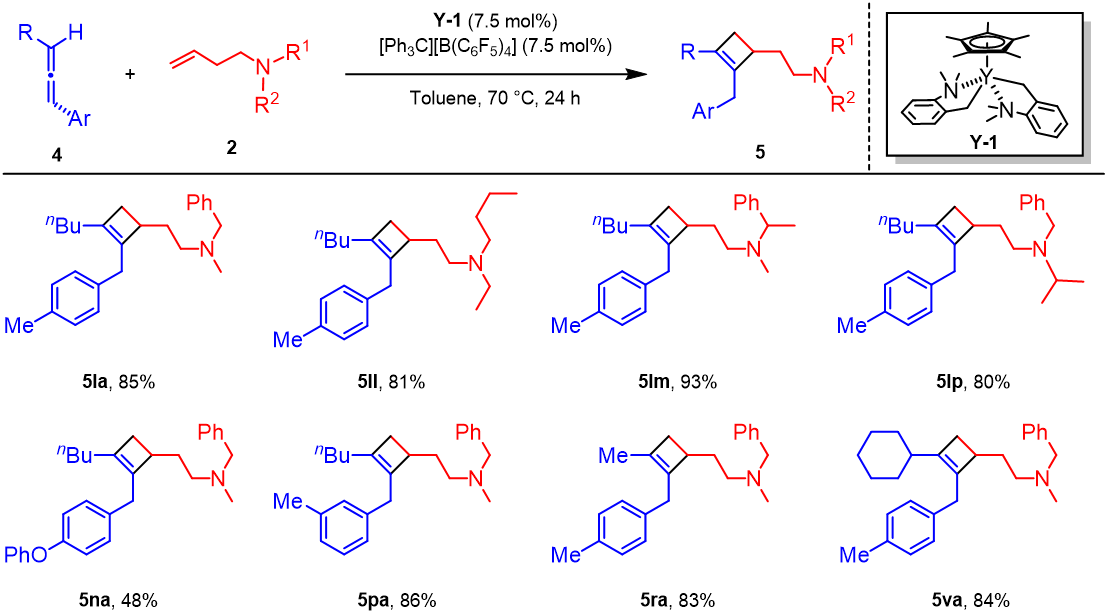
图4. 钇催化1-芳基-3-烷基联烯与烯烃的的[2+2]环加成反应(部分底物)
最后,作者通过氘代标记及动力学等实验对反应机理进行了初步的研究和探讨,证明了反应的关键启动步骤是稀土金属络合物对联烯C(sp2)−H键的活化。
总结:
在该工作中,侯召民教授团队利用半夹心型稀土金属络合物为催化剂,通过联烯C(sp2)−H键选择性活化,首次实现了电子无偏的联烯与非活化烯烃的[2+2]环加成反应。该反应具有100%的原子经济性、出色的非对映选择性(d.r. > 19:1)、广泛的底物范围、良好的官能团耐受性等优点,为多官能团取代的甲基烯环丁烷化合物和环丁烯化合物的构建提供了一种高效、高区域和立体选择性的合成方法。
(侯召民教授供稿)
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载





















No comments yet.