导读
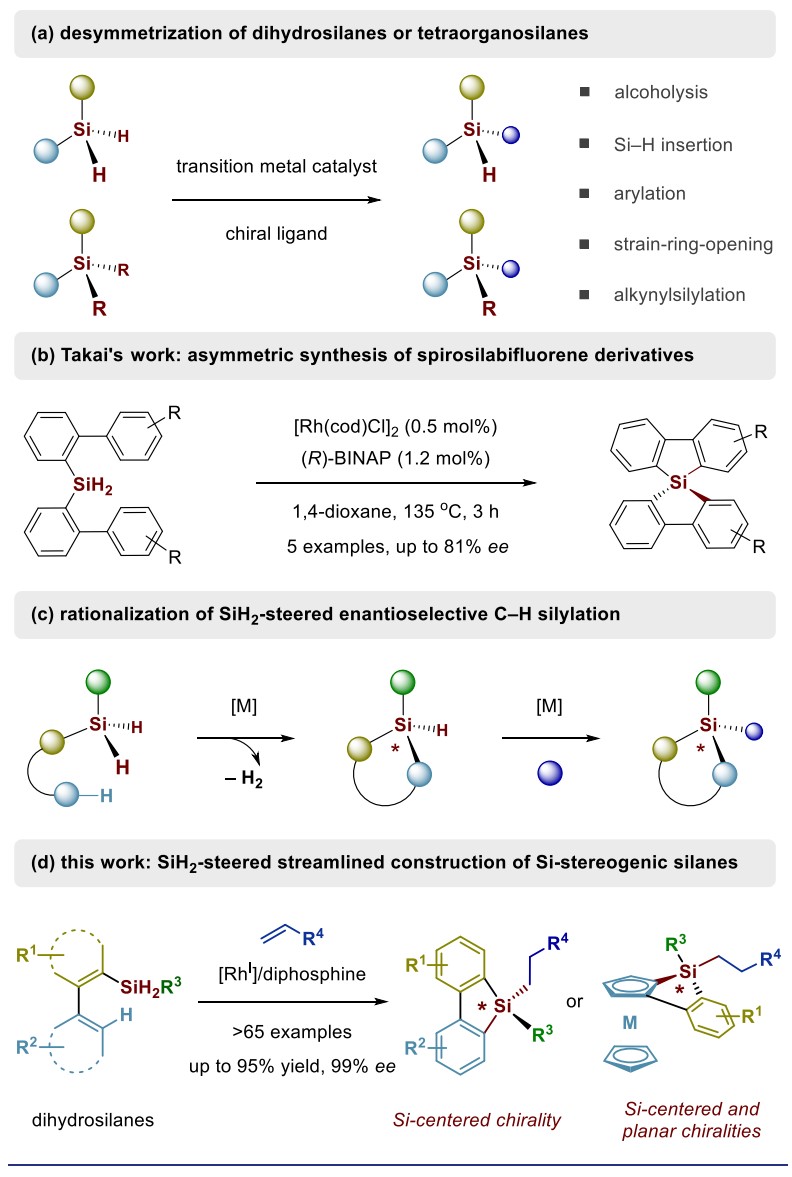
基于不对称催化策略构筑立体硅烷是一项具有挑战性的工作。化学家制备的有机硅化合物在合成化学、材料科学和药物中有着广泛的应用。[1]但是固有的长碳硅键阻止了致密过渡态的形成以及硅原子通常与相对相似的基团结合,这使得在催化过程中对映体面或基团难以进行对映体识别。另外,空的3d轨道使硅原子很容易形成高价的五配位或六配位中间体。目前,传统获取对映体纯或对映体富集立体硅烷的形式有限,主要基于手性助剂进行光学和动力学拆分,因此,探索高效的不对称合成方法,利用简单原料制备对映体富集的高功能化立体硅烷具有深远的意义。在过去的二十年里,许多研究一直致力于应用手性过渡金属催化剂催化立体硅烷的不对称合成,主要基于二氢硅烷或者四取代硅的去对称化合成(图1a),但是往往存在底物范围较窄、官能团耐受性差或对映体选择性低等问题。[2]
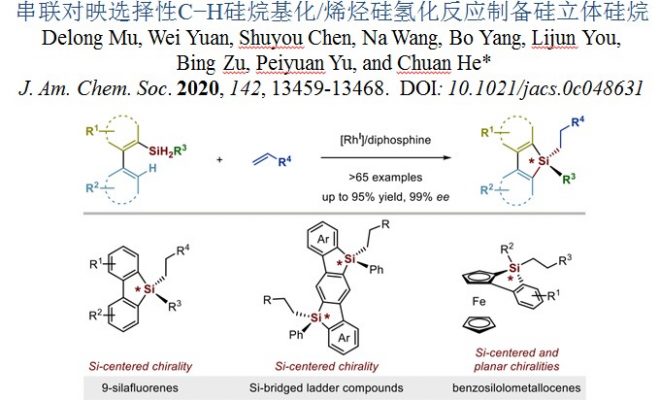
近年来,过渡金属催化C−H键硅烷化反应发展成为一种合成有机硅化合物强有力的手段。作者认为,硅烷基不仅可以用作导向基团,还可以在对映选择性C−H活化过程中实现硅立体中心的功能化,这将提供更有效、直接的方式来构建立体硅烷。到目前为止,仅有Takai、Kuninobu等报导的通过二氢硅烷制备立体双(联苯)硅烷(图1b)。[3,4]作者设想,以过渡金属为催化剂,设计二氢硅烷为载体的适当手性反应,实现SiH2导向的对映选择性C−H硅烷化,获取相应的不对称单氢硅烷,然后立即捕获单氢硅烷,进一步发生反应,提供不对称四取代立体硅烷(图1c)应该具有可行性。基于上述研究背景,南方科技大学Chuan He等报导了基于各种二氢硅烷,通过对映选择性C−H硅烷化/烯烃硅氢化反应制备各种复杂和功能多样的四取代硅烷(图1d)。相关成果发表于:
“Streamlined Construction of Silicon-Stereogenic Silanes by Tandem Enantioselective C-H Silylation/Alkene Hydrosilylation”
Delong Mu, Wei Yuan, Shuyou Chen, Na Wang, Bo Yang, Lijun You, Bing Zu, Peiyuan Yu, and Chuan He* J. Am. Chem. Soc. 2020, 142, 13459-13468. DOI: 10.1021/jacs.0c04863
图1. 构筑立体硅烷
论文概要
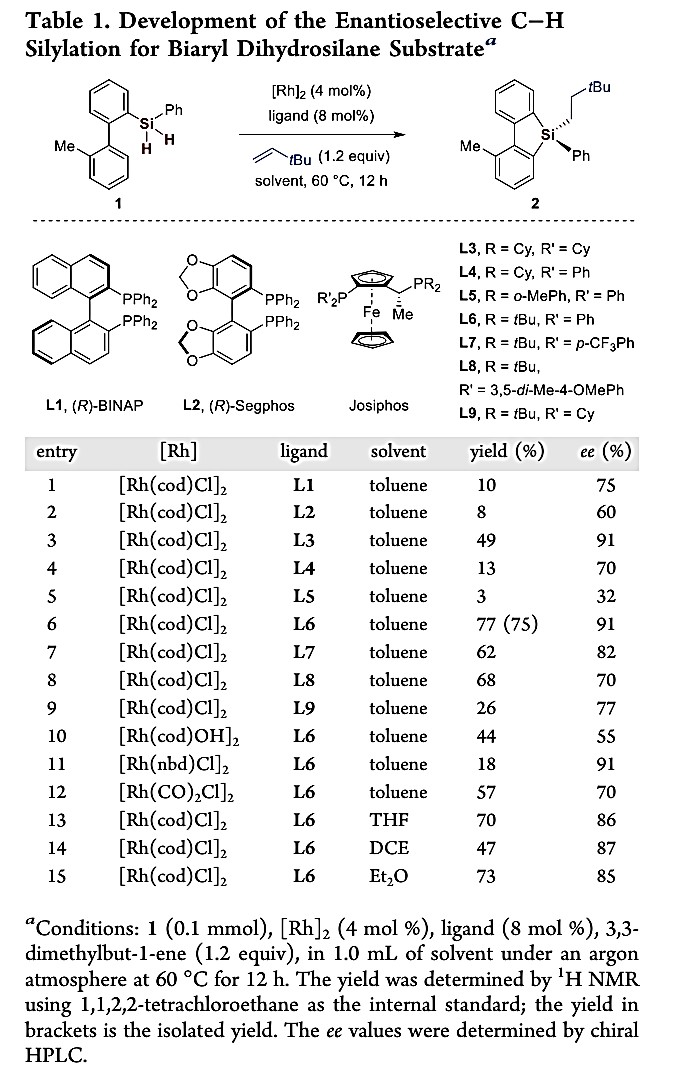
条件筛选:作者首先进行了条件筛选。以二氢硅烷1为底物,在适当的过渡金属催化剂存在下,可能经历SiH2控制的C−H六元金属环中间体,进行该对映选择性C−H硅烷化反应。作者尝试了多种铑(I)和铱(I)以及各种手性配体,只得到少量C−H硅烷化的单氢硅烷,并且二氢硅烷原料在很多情况下都发生分解。之后,作者经过多次努力,发现当用4 mol% Rh(cod)Cl二聚体催化前体,加双齿膦配体,如BINAP(L1)或Segphos(L2),在1.2当量的3,3-二甲基-1-丁烯存在下,与二氢硅烷1发生反应,尽管收率较低,但能以60−75%的ee值得到四取代立体硅烷产物2(表1,entry 1&2)。值得注意的是,烯烃参与了反应而不是作为氢受体,且该反应无需外加氧化剂。作者进行进一步的条件优化和配体筛选,发现市售的Josiphos配体(L6)具有良好的反应效果,可将反应的对映选择性提高至91% ee,收率提高到75%(表1,entry 3-9)。其他的铑(I)催化剂降低了收率(表1,entry 10-12)。作者也对溶剂进行了筛选,对于THF、DCE或Et2O,其产量和ee值均较低(表1,entry 13−15)。最终作者选定Rh(cod)Cl2为催化前体、L6为配体、甲苯为溶剂为最优反应条件。
表1. 条件筛选
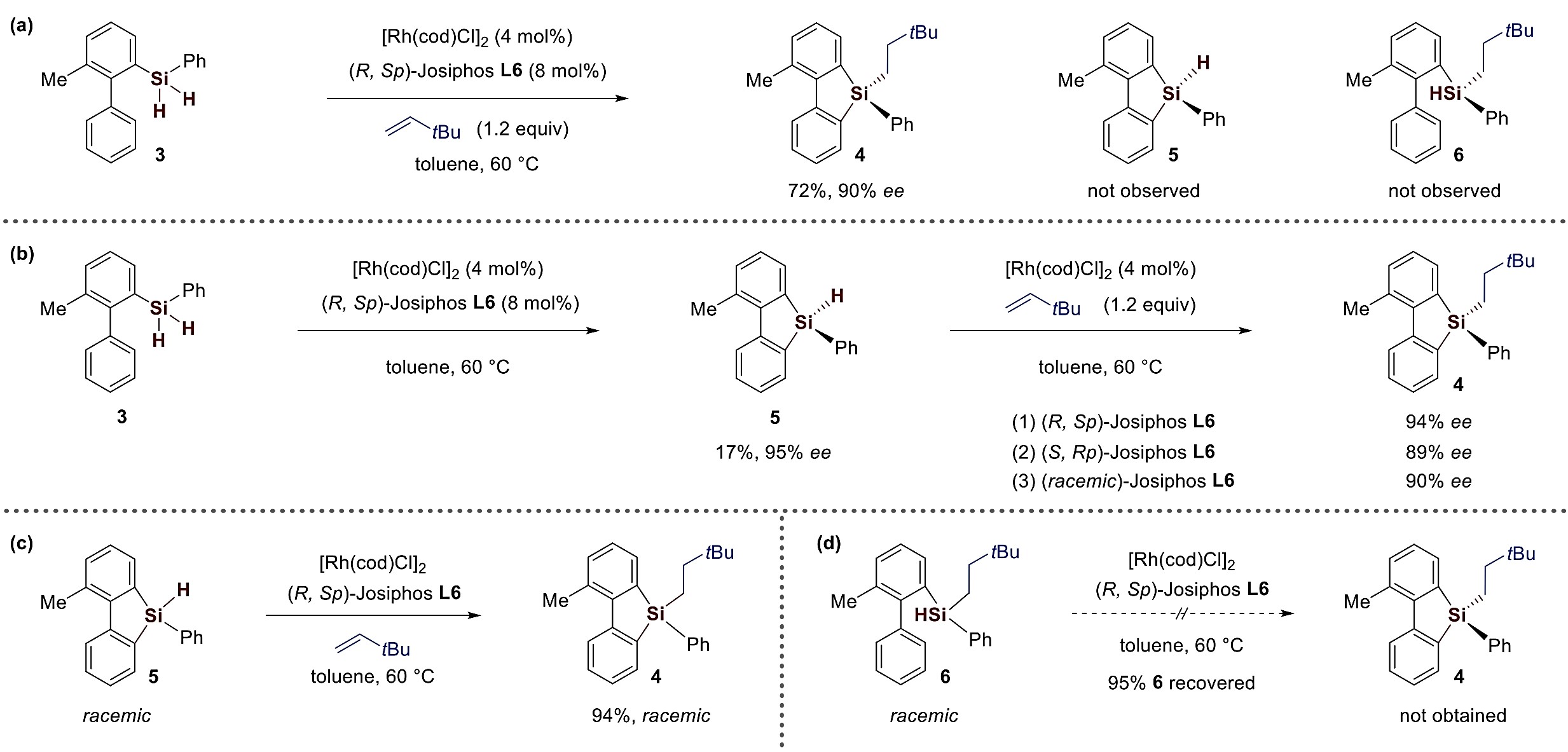
机理研究:作者进行了控制实验以及机理研究。在优化条件过程中,作者利用同一芳环上含有甲基取代的二氢硅烷底物3进行了尝试,得到产物4具有90% ee(图2a)。在优化条件中,如果反应不加烯烃,可通过C−H活化/硅烷化得到5,收率为17%(图2b)。尽管收率低,但是95% ee明显表明立体决定步骤是SiH2控制的C−H活化/硅烷化过程。单氢硅烷5进一步与3,3-二甲基-1-丁烯在Rh催化条件下发生反应,使用(R,Sp)-Josiphos L6、(S,Rp)-Josiphos L6或(外消旋)-Josiphos L6中的任一种,均能提供相同的四取代硅烷4,且对映选择性保持。当外消旋单氢硅烷5在使用(R,Sp)-Josiphos L6下进行反应,得到了外消旋产物4(图2c)。此外,作者还制备了外消旋单氢硅烷6,标准反应条件下无反应发生(图2d)。这些结果进一步表明单氢硅烷5是该反应的关键中间体。
图2 控制实验
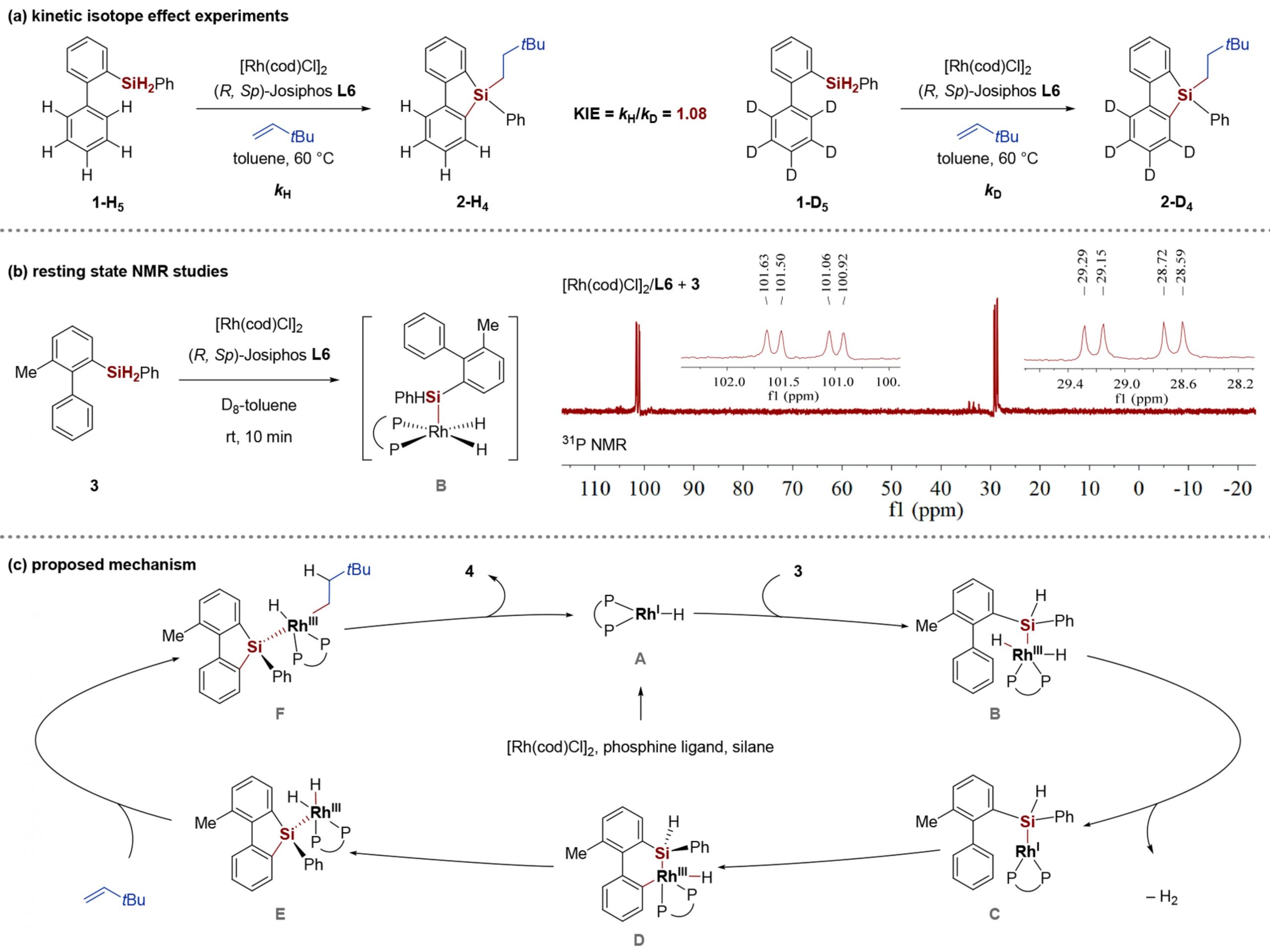
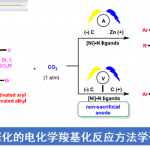
接下来,作者使用1-H5和1-D5进行了两个平行的动力学同位素效应(KIE)实验(图3a)。反应得到的kH/kD值为1.08,动力学同位素效应排除了碳氢键断裂是该反应的决速步的可能性。此外,还研究了二氢硅烷3与[Rh(cod)Cl]2,Josiphos-L6的反应,并监测其31P和1H室温核磁共振谱图(图3b)。两组峰分别为P(tBu)峰101.3 ppm(dd,JRh−P = 140.9 Hz,JP−P = 32.6 Hz),P(Ph)2峰28.9 ppm(dd,JRh−P = 136.5 Hz,JP−P = 32.6Hz)。此外,还观察到两个铑氢物种(−6.28和−3.32 ppm)的1H核磁谱图(图3b)。这些信号表明铑硅二氢化合物中间体B的形成。因此,作者建议该SiH2控制的对映选择性C-H硅烷化/烯烃硅氢化过程机理如图3c所示。首先,经Rh(cod)Cl2二聚体与手性膦配体,生成Rh(I)催化剂物种A,在二氢硅烷1的存在下,经Si−H氧化加成生成中间产物B。然后还原消除二氢,从中间体B生成Rh(I)硅烷络合物C,随后进行对映选择性C−H键活化,提供中间产物D,然后还原消除中间产物D形成C−Si键和Rh(I)氢化物种,立即进行氧化加成进入第二个Si−H键,提供中间产物E。最后,在中间体E中插入烯烃生成中间体F,最后还原消除完成催化循环,再生具有催化活性的Rh(I)物种。
图3 不同取代的丙烯酸底物拓展
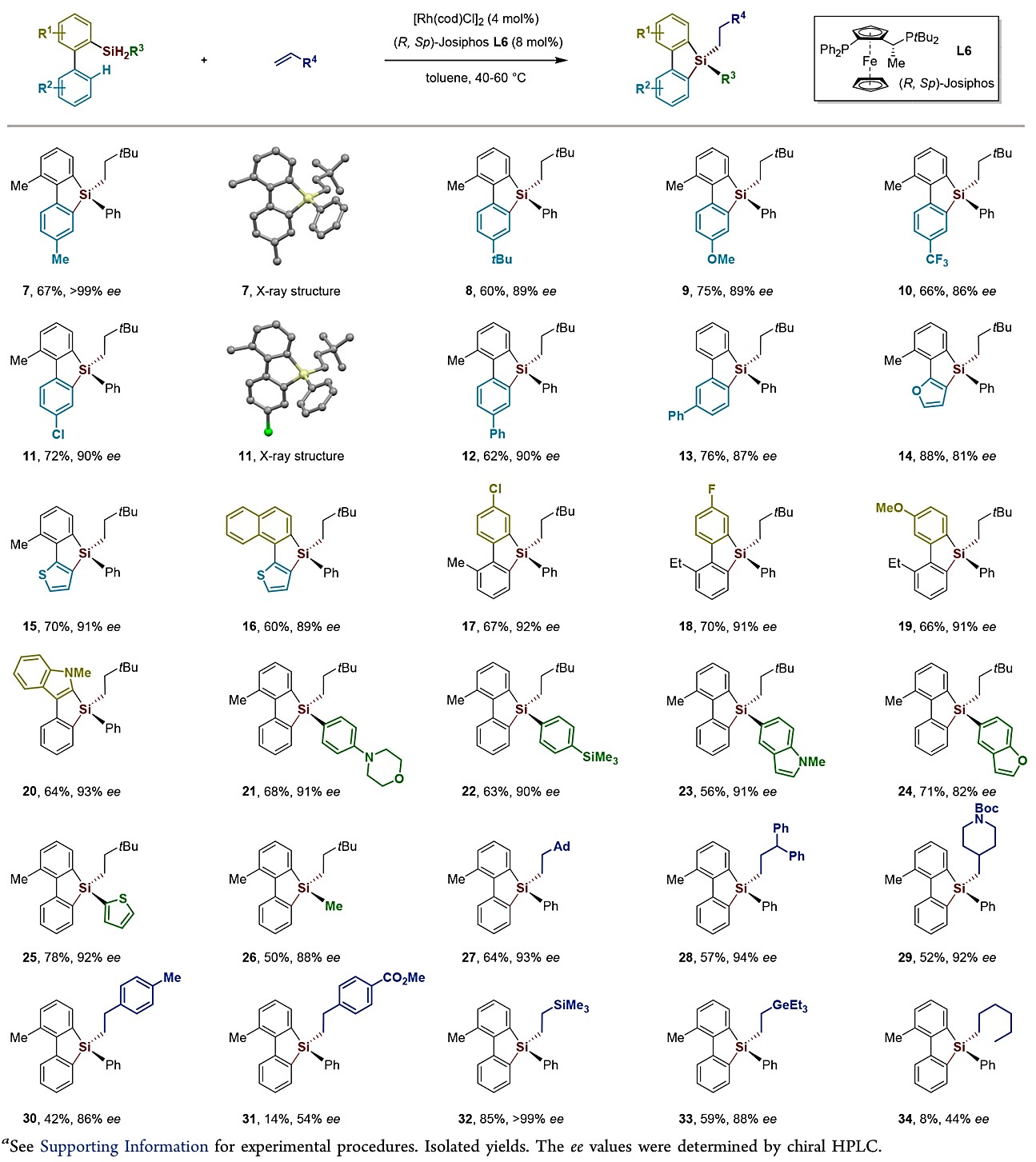
底物拓展: 在优化条件的基础上,作者接下来进行底物拓展研究,对四取代硅烷每部分取代均进行了评估(图4)。首先,联芳基二氢硅烷基具有较好的适应性。作者对联芳基的两个不同芳环均进行了探讨,与3,3-二甲基-1-丁烯均能很好的反应,以中等至优良的收率(55−88%)以及优异的对映选择性(81−99% ee)得到四取代硅烷。吸电子基团,如甲基、叔丁基、甲氧基(7−9)和吸电子基团,如三氟甲基(10)和卤素取代基(11,17,18)均具有良好的耐受性。此外,作者也对杂芳香环如呋喃、噻吩和吲哚(12−16,20)进行了研究,也可以成功转化为相应的目标产物。接下来,作者改变硅烷的第三个取代基,包括二氢硅烷底物的取代芳香环、杂芳环和脂肪甲基,也基本保持较高的对映选择性(21-26)。对于烯烃的范围,作者发现除3,3-二甲基-1-丁烯外,其他含金刚烷基、芳香环、氨基等取代基的各种烯烃均能很好地进行反应,得到高度功能化的取代硅烷,对应的产物均具有高的收率和对映选择性(27−30、32、33)。但是,羰基、酯或酮官能团在该反应中的效果不佳(31)。此外,线性脂肪族烯烃(34)的收率和对映选择性均较差。
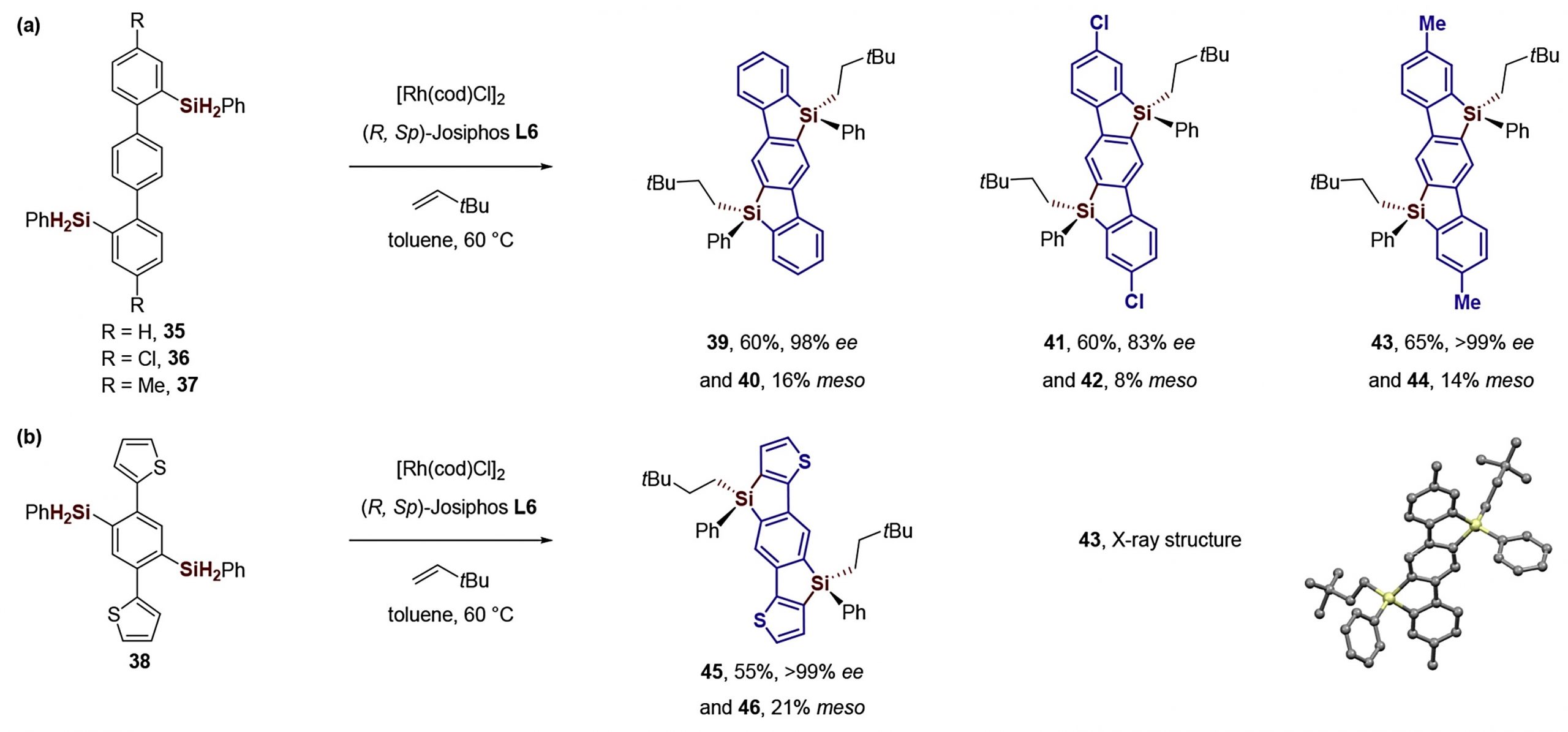
此外,作者考虑到硅桥梯形π共轭体系也是一类重要的有机支架,对映体纯的该类化合物可能在材料科学具有重要应用。作者选择四种双二氢硅烷底物(35−38)在标准条件下反应(图5),每个底物经历了的C−H硅烷化/烯烃硅氢化反应制备目标硅桥梯形π-共轭产物(39,41,43,45),均具有较高的收率和优异的ee值。
图4 部分9-硅芴底物拓展
图5 具有π共轭体系的底物拓展
图6 其他二茂金属类二氢硅烷底物拓展
作者利用SiH2控制的C−H硅烷基化/烯烃硅氢化反应,比较容易以高对映选择性获得硅立体9-硅芴衍生物,作者猜想能否利用茂金属体系,产生含硅立体中心的茂金属化合物。由于茂金属化合物在材料科学、生物有机金属化学中具有重要应用,且手性茂金属衍生物可作为催化剂和配体在不对称催化中发挥重要作用,作者认为将金属茂底物应用于该反应中是十分必要的。在现有的反应条件下,作者将Josiphos配体改为Segphos(L2)配体,不同的二茂铁二氢硅烷底物均显示良好的底物适应性(图6),得到的四取代硅烷同时含有硅中心手性和平面手性,且均作为单个非对映体并具有良好的对映选择性(90−99% ee)。首先,芳环上具有多个给电子、吸电子以及不同位置取代基的二茂铁二氢硅烷底物均展现了良好的底物适应性,如苯环上具有甲基、氟、氯、甲氧基、三氟甲基、OTBS和氨基官能团等,均以62−95%的收率和93−99%的ee(47−54,58−62)得到。此外,含萘环、苯并呋喃和二茂钌的二氢硅烷也具有可行性(55,56,63)。值得注意的是,一系列烯烃,包括脂肪族烯烃、乙烯基醚、乙烯基胺、苯乙烯、乙烯基二茂铁和乙烯基硅烷等均能以良好的反应结果得到目标产物(64−74)。此外,线性脂肪族烯烃与二茂铁二氢硅烷基体相容,可得产物66,表明SiH2转向茂金属的C−H活化/硅烷化比直接烯烃硅氢化反应更为有利。为了进一步说明该反应的转换效用,作者用几种生物活性分子、药物或材料构建底物,反映效果均非常优异,如(+)-α-生育酚(75)、D-呋喃糖苷(76)、β-雌二醇(77)、(-)-薄荷醇(78)、吩噻嗪(79)以及化合物80、81等,作者发现设计的这些底物均具有良好的底物适应性,展现了该反应的立体选择性好、官能团多样、分子结构复杂的优势。
论文总结评价
本文报导了基于各种二氢硅烷,通过对映选择性C−H硅烷化/烯烃硅氢化反应制备各种复杂和功能多样的四取代硅烷,反应底物适应性很好,均能以良好至优异的收率和对映选择性得到四取代硅烷,并通过控制实验以及机理研究提出了可能的催化循环。作者希望该方法能在合成化学、药物化学以及材料科学中发挥重要作用,并将在不对称催化中有进一步发展。
参考文献
- [1] E. Remond, C. Martin, J. Martinez, F. Cavelier, Chem. Rev. 2016, 116, 11654-11684. DOI: 10.1021/acs.chemrev.6b00122
- [2] L.-W. Xu, Angew. Chem. Int. Ed. 2012, 51, 12932-12934. DOI: 10.1002/anie.201207932
- [3] Y. Kuninobu, K. Yamauchi, N. Tamura, T. Seiki, K. Takai, Angew. Chem. Int. Ed. 2013, 52, 1520-1522. DOI: 10.1002/anie.201207723
- [4] M. Murai, Y. Takeuchi, K. Yamauchi, Y. Kuninobu, K. Takai, Chem. – Eur. J. 2016, 22, 6048-6058. DOI: 10.1002/chem.201504718
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.