作者:石油醚
导读:
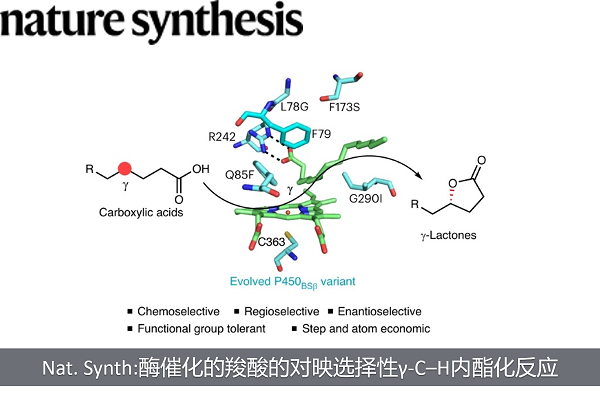
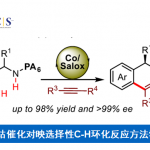
近日,扬州大学王喜庆教授团队通过定向进化改造P450酶(P450BSβ)解决了这一难题,实现了链状脂肪族羧酸未活化的C–H键的高度区域和对映选择性的γ-内酯化反应,从而将脂肪酸直接合成为相应的γ-内酯。安徽大学何超课题组解析了改造后的酶突变体与棕榈油酸复合物的晶体结构,并经中国科学技术大学廖结楼课题组分子动力学模拟和密度泛函计算,阐明了该酶反应选择性的结构基础。
“Biocatalytic enantioselective γ-C–H lactonization of aliphatic carboxylic acids
Qian Ma, Wenhao Shan, Xuan Chu, Haochen Xu, Ziyi Chen, Fudong Li, Jie-Lou Liao*, Chao He*, Wen-Ju Bai*, and Xiqing Wang*
Nat Synth. 2023 : doi:10.1038/s44160-023-00427-y.”
正文
γ-内酯存在于多种天然产物的结构中,且表现出优良的生物活性,被广泛应用于食品风味、药物开发、生物防治和保护以及生物相容性材料等多个领域。
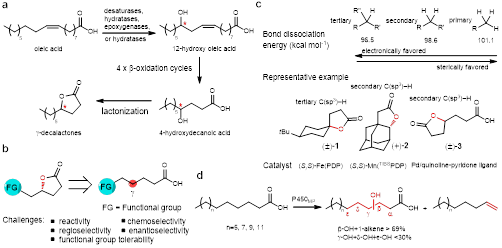
在生物代谢过程中,γ-内酯的合成与脂肪酸代谢相关。受自然合成策略的启发,王喜庆课题组和白文举博士(斯坦福大学,现艾伯维)设想通过亚甲基C–H键的羟基化和内酯化直接从自然界广泛存在、可再生的脂肪酸来高效、绿色合成γ–内酯。该想法存在着化学、区域、对映选择性以及官能团容忍性的多重挑战,所以,不论利用化学催化剂还是生物酶都难以实现。该课题组通过定向进化改造P450酶(P450BSβ)解决了这一难题,实现了链状脂肪族羧酸未活化的C–H键的高度区域和对映选择性的γ-内酯化反应,从而将脂肪酸直接合成为相应的γ-内酯。安徽大学何超课题组解析了改造后的酶突变体与棕榈油酸复合物的晶体结构,并经中国科学技术大学廖结楼课题组分子动力学模拟和密度泛函计算,阐明了该酶反应选择性的结构基础。该成果近期发表在Nature Synthesis上。
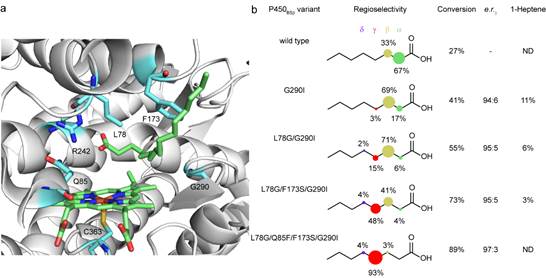
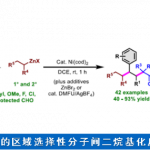
基于近年对P450BSβ的定向进化研究(Angew. Chem. Int. Ed. 2022;ACS Catal. 2021;ACS Catal. 2020),该合作团队赋予了原本无γ-内酯化活性的野生型P450BSβ新的γ-内酯化活性,得到了高转化率和高γ位选择性的P450BSβ-L78G/Q85F/F173S/G290I突变体。在定向进化过程中,底物转化率逐步从27%增加至89%,γ位羟基化选择性从0%提高至89%,且始终保持较高的对映选择性(>94:6 e.r.)。
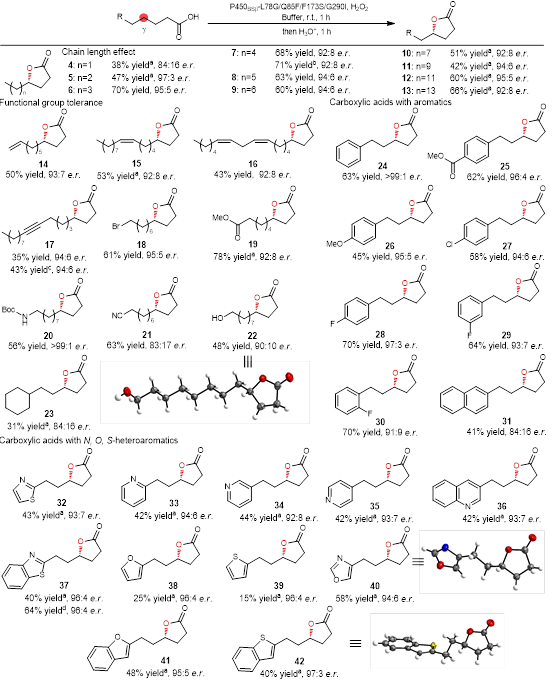
为探究该突变体酶的合成价值,作者对该酶进行了0.5 mmol制备级反应的底物研究,发现该酶摆脱了对烃链长度的依赖,能够催化C6–C20链长的脂肪酸(产物4-13),同时具有很好的官能团耐受性(产物14-23),展现了较好的反应活性以及高度的区域和对映选择性。值得一提的是,该反应也可适用于含各种芳环(产物24-31)和芳杂环的脂肪族羧酸(产物32-42),因此,在药物分子的合成与开发上有很好的应用。
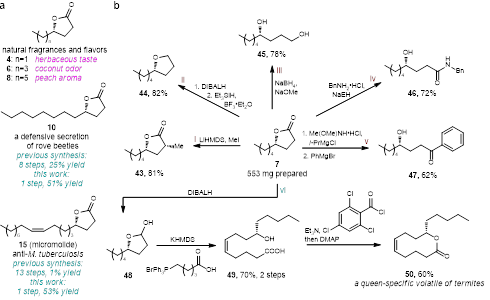
该酶反应的一些产物散发出香草、椰汁和桃子的香味而可作为食品口味添加剂(产物4,6,8)。这一催化反应也将一些天然产物的合成直接缩减到1步(天然产物10,15),大幅提到了合成效率。此外,所合成的γ-内酯可以搭配多样的后续化学转化,实现包括天然产物在内的一系列化合物的合成(产物43-50)。
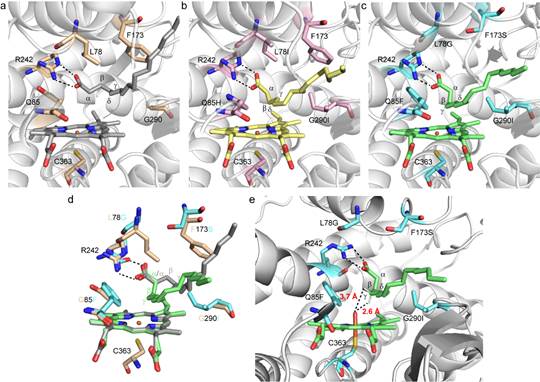
最后,对改造后的酶与棕榈酸复合物的晶体结构的解析以及分子动力学模拟和密度泛函计算揭示了该酶γ-内酯化反应的高区域和对映选择性的机理。该研究展现了定向进化可以赋予野生酶自然界未有的新功能,从而解决化学合成上具有挑战性的化学反应。
(王喜庆教授供稿)
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.















No comments yet.