作者:石油醚
导读:
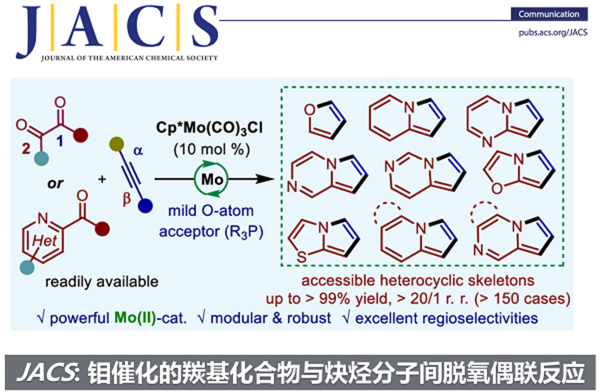
厦门大学卓春祥教授团队报道了一类稳定、易得的Cp*Mo(II)催化剂作为高效、新型的羰基脱氧催化剂,并用于催化羰基化合物和炔烃的分子间直接脱氧偶联反应。该反应能够以高化学选择性、高区域选择性、中等到优秀的收率得到一系列杂芳环化合物(十类不同杂环产物)。该策略为多种具有高价值的杂环化合物的快速构建提供了通用的催化平台。该成果近期发表于J. Am. Chem. Soc.上,博士生王佳乐和吴冠宇为论文的共同一作,硕士生罗建南(已毕业)、博士生刘俊龙参与了部分研究工作。
“Catalytic Intermolecular Deoxygenative Coupling of Carbonyl Compounds with Alkynes by a Cp*Mo(II)-Catalyst
Jia-Le Wang, Guan-Yu Wu, Jian-Nan Luo, Jun-Long Liu, and Chun-Xiang Zhuo* J. Am. Chem. Soc. 2024, ASAP doi: 10.1021/jacs.3c14195
正文:
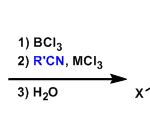
在有机合成中,羰基是一类重要的官能团且具有丰富的反应性。此外,羰基化合物具有廉价易得的特点,在自然界也广泛存在。然而,由于将C=O双键切断需要较高的活化能,直接将羰基化合物转化为金属卡宾物种具有较高的挑战性(图1 A)。尽管如此,该转化非常具吸引力因为这一转化能够将安全和易得的羰基化合物作为具有潜在爆炸风险的重氮化合物的替代物。目前实现这一转化的策略通常需要使用多步操作(图1 B)或当量金属试剂、低价金属络合物。通过催化方法一步实现羰基直接脱氧生成金属卡宾并发生后续官能团化仍然颇具挑战。
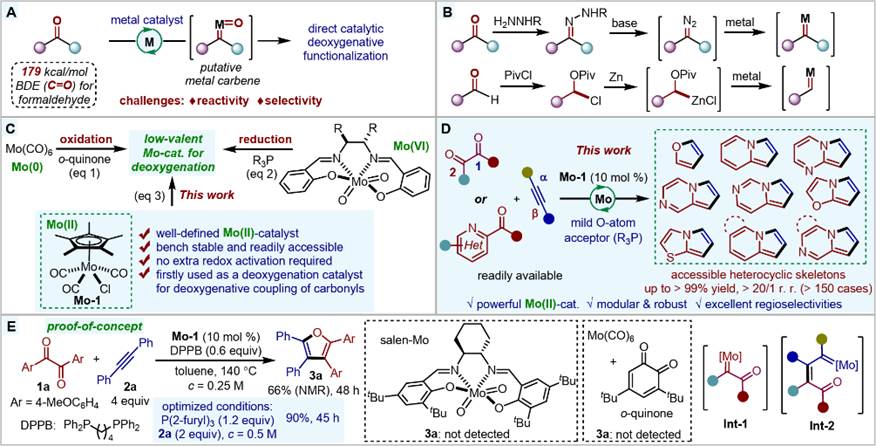
图1
厦门大学卓春祥课题组一直致力于发展新型钼催化的羰基直接脱氧官能团化反应(Angew. Chem. Int. Ed. 2021, 60, 15254; ACS Catal. 2022, 12, 11428; J. Am. Chem. Soc. 2023, 145, 2765; J. Am. Chem. Soc. 2023, 145, 8781; Org. Chem. Front. 2023, 10, 3544)。前期发展的羰基脱氧官能团化反应主要依赖于使用邻苯醌氧化零价Mo(CO)6(图1 C,eq 1)或者使用膦作为还原剂还原六价手性salen-Mo(图1 C,eq 2)的低价钼催化体系。由于这些催化体系均需经过氧化或还原的预活化才能生成活性低价钼物种,作者设想发展一类稳定、易于获取且能直接用于羰基脱氧官能团化反应的低价钼催化剂。作者注意到Cp*Mo(CO)3Cl是一种稳定的二价钼络合物,但却极少直接作为二价钼催化剂用于有机合成中。取而代之的是,该二价钼络合物经常作为六价钼的前体而用于一些氧化反应中。作者推测该Cp*Mo(II)络合物可能是催化羰基直接脱氧官能团化反应的理想催化剂候选者,因为富电子的Cp*配体不但能使得碳氧双键的断裂更容易,而且也能降低钼中心的Lewis酸性从而抑制酸促进的富电子芳环的分解或聚合(图1 C,eq 3)。
近日,卓春祥教授团队报道了一类稳定、易得的Cp*Mo(II)催化剂作为新型、高效的羰基脱氧催化剂,并用于催化羰基化合物和炔烃的分子间直接脱氧偶联反应(图1 D)。该反应能够以高化学选择性、高区域选择性、中等到优秀的收率得到一系列杂芳环化合物(十类不同杂环产物)(图2、4)。
通过使用1,2-二羰基底物和炔烃反应,该方法可用于至多含有四个不同取代基的呋喃产物的快速制备(图2)。
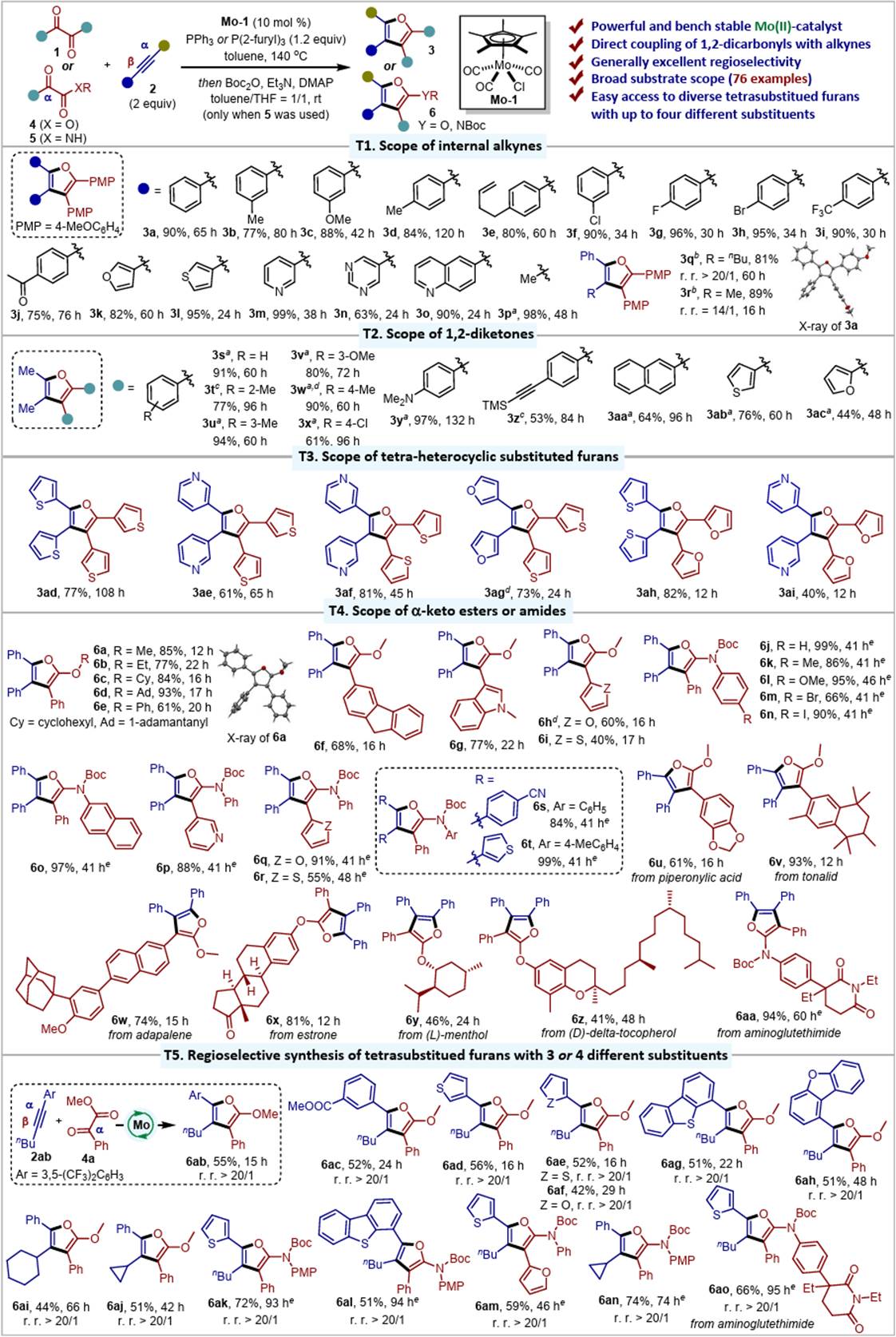
图2
作者进行了初步的机理研究(图3)。 首先,底物4a和2a在标准条件下反应能够分别以85%和106%的分离收率得到6a和三苯基氧膦,证明4a中羰基上的氧原子几乎完全转移至三苯基膦上(图3 A,eq 1)。随后,作者将两种可能的中间体在标准条件下进行反应,但几乎没有得到目标产物,这表明该反应的主要路径不是环丙烯化/重排路径或羰基-炔烃复分解/脱氧环化路径(图3 A,eq 2)。另外,当底物9在标准条件下反应时,可以以64%的分离收率得到脱氧环丙烷化产物10,表明1,2-二羰基化合物能够在标准条件下生成推测的钼卡宾中间体(图3 A,eq 3)。为了进一步验证可能的钼卡宾中间体的存在,作者使用底物1a和2a在当量Mo-1和18O标记的二苯基亚砜条件下进行反应,发现呋喃产物的生成被完全抑制,且分离到71%的18O-1a,这一结果表明原位生成的钼卡宾中间体I-2可能被18O标记的二苯基亚砜氧化(图3 A,eq 4)。基于此,作者提出了一个可能的催化循环(图3 B)。值得一提的是,这也是首个通过催化剂对非活化内炔的取代基的区分来实现分子间卡宾-炔烃复分解反应的高区域选择性的通用方法。
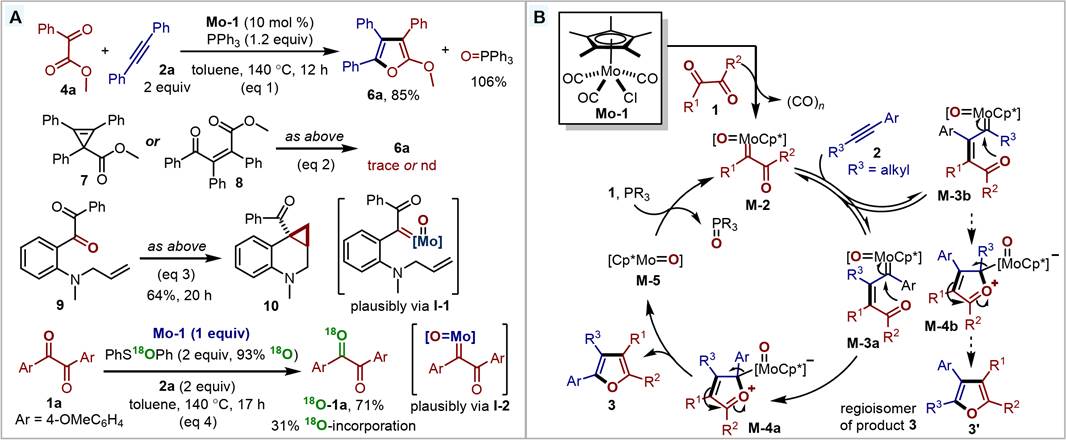
图3
此外,通过使用单羰基底物和炔烃反应,该方法也可用于多种含氮杂环产物的合成,在该体系中,端炔同样表现出优异的区域选择性(图4)。
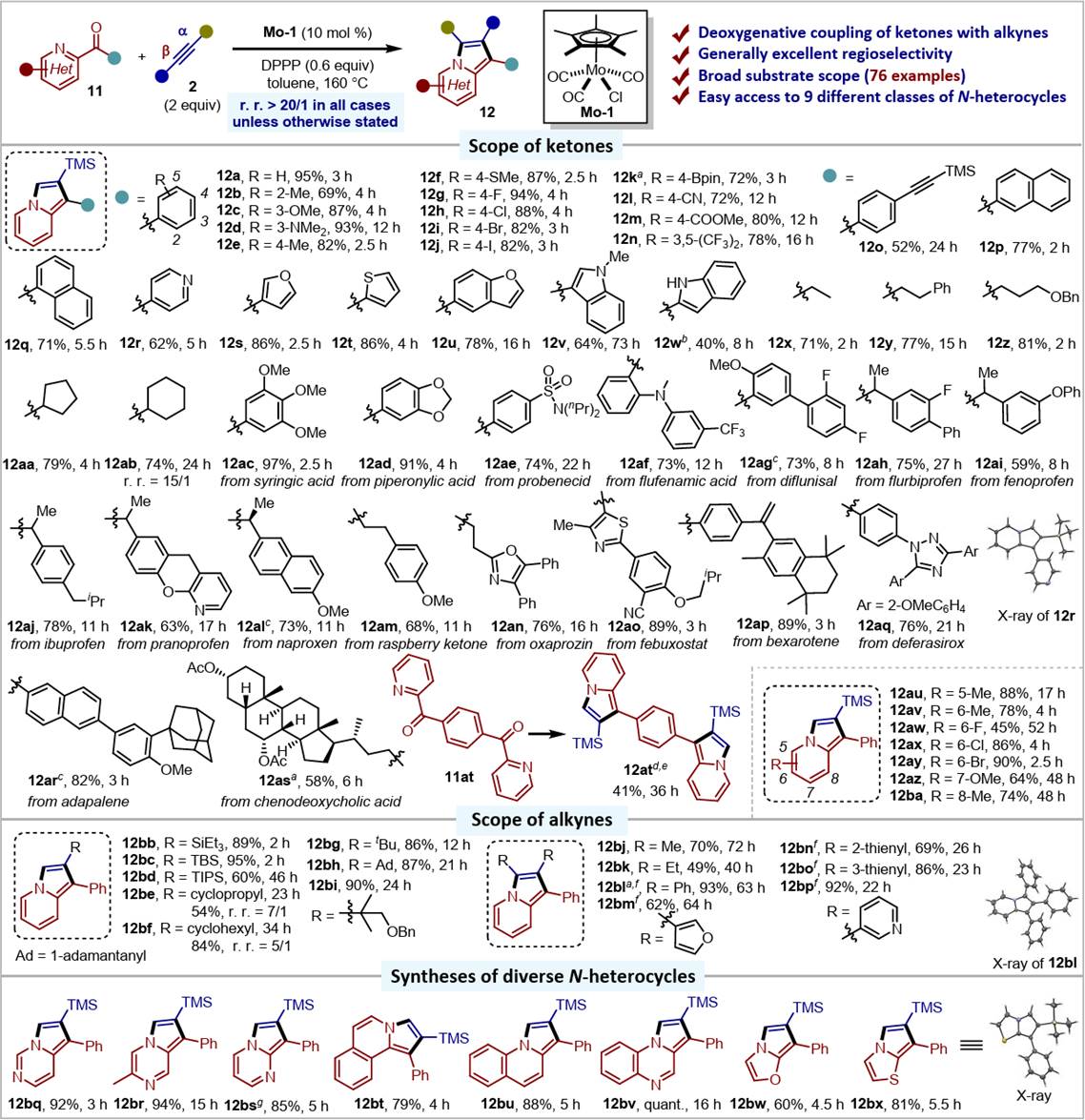
图4
随后,作者进行了克级反应和合成应用研究,以展示该方法的应用价值(图5)。在克级规模上,反应可以顺利进行。四取代呋喃产物可进一步发生Diels-Alder反应、氧化开环/环化、分子内重排等反应得到1,4-二羰基化合物、吡咯、五元内酯、六取代苯等多种合成砌块(图5 A-B)。四(2-噻吩)取代呋喃19可以通过该方法从商业化原料一步制备,相较于先前的合成方法更加便捷(图5 C)。通过该方法也能合成具有抗雌激素活性化合物的衍生物21(图 5 D),雌激素受体α配体23(图5 E),以及具有抗癌活性化合物的衍生物24(图5 F)。吲嗪产物可进一步发生酰基化/Hiyama偶联,吲嗪上的-TMS基团也可发生溴化或脱除,吲嗪环也可以和炔烃发生进一步环化(图5 G)。此外,通过该方法也可实现具有AIE活性的分子Aru68的形式合成(图5 H)和OLED材料分子的合成(图5 I)。
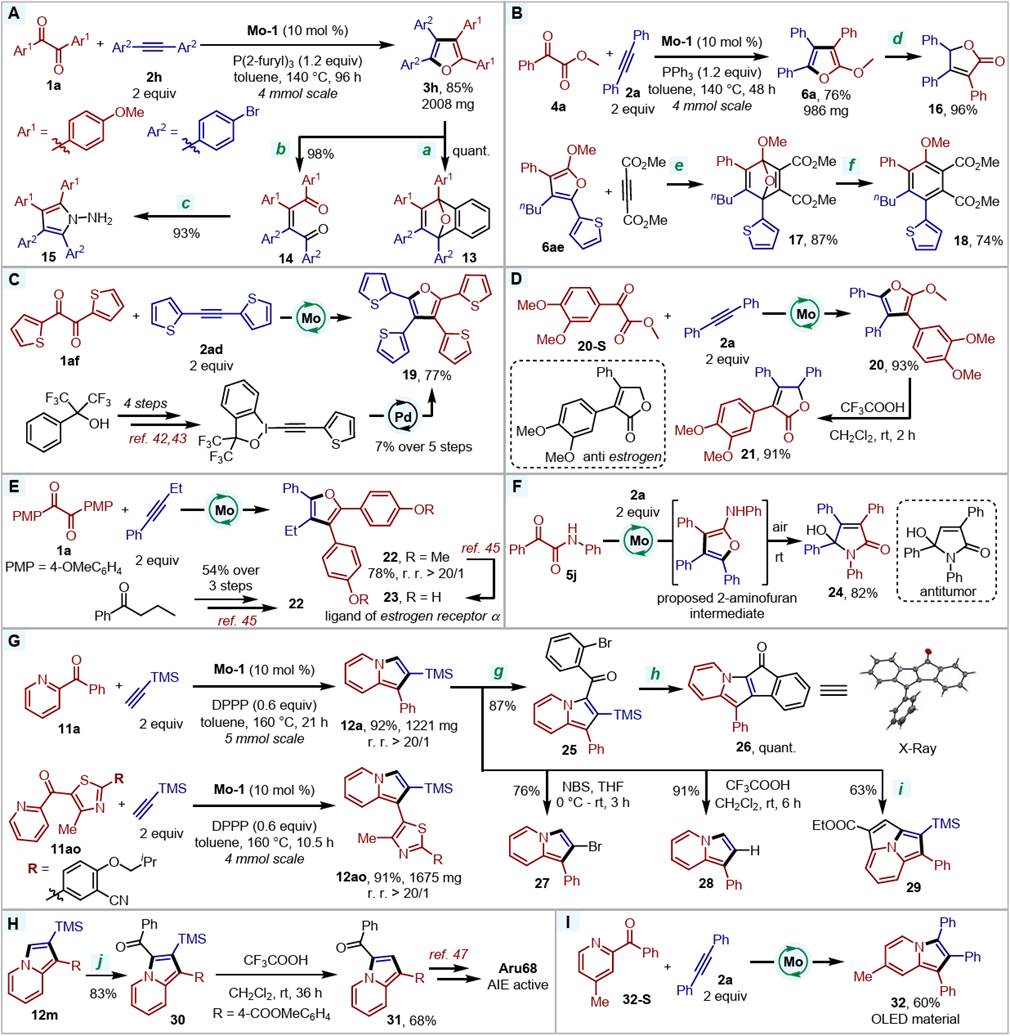
图5
在该工作中,卓春祥教授团队报道了一类稳定、易得的Cp*Mo(II)催化剂作为高效、新型的羰基脱氧催化剂,并用于催化羰基化合物和炔烃的分子间直接脱氧偶联反应。该反应能够以高化学选择性、高区域选择性、中等到优秀的收率得到一系列杂芳环化合物(十类不同杂环产物)。该策略为多种具有高价值的杂环化合物的快速构建提供了通用的催化平台。
课题组长简介
卓春祥,厦门大学教授,博士生导师,国家高层次青年人才,福建省“闽江学者”特聘教授,厦门市“双百计划”高层次创新人才,厦门大学化学化工学院有机化学研究所副所长。2009年本科毕业于湖南大学,2014年博士毕业于中国科学院上海有机化学研究所(导师:游书力 院士)。随后在德国马普煤炭所Alois Fürstner教授课题组进行博士后研究。2019年4月入职厦门大学开展独立研究工作,主要研究方向为新型有机合成方法学、不对称催化、活性天然产物及药物分子的合成。迄今发表论文33 篇,被引用3200余次。曾获得中美华人化学与化学生物学教授联合会青年教授奖(CAPA Junior Faculty Award,2024),德国Thieme Chemistry Journals Award (2022), Science of Synthesis首届国际青年咨委(2022),国家海外高层次青年人才(2019),国家自然科学二等奖(2017),中国科学院优秀博士论文(2015),德国洪堡学者(2015),中国科学院院长奖特别奖(2014)等荣誉与奖励。
欢迎有机化学方向的博士后加入本课题组,待遇详见: https://zhuolab.xmu.edu.cn/joinus.htm















No comments yet.