有机三氟硼酸盐(R-BF3–)对热・空气・湿度稳定,是取用十分简便的结晶性硼酸类化合物。
由于氟的取代后具有四配位型的硼酸构造,因此不显示路易斯酸性,从而对氧化条件稳定。另外可以看做是硼酸・硼酸酯的保护体,可以相互转化。
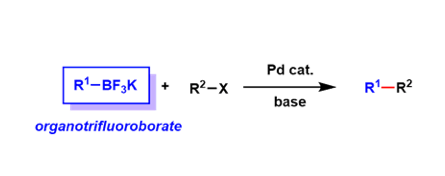
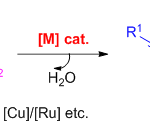
该化合物一般能够稳定存在于有机溶剂中,而在质子性溶剂下会分解,游离出三价的硼,因此可以直接作为铃木偶联的底物。三氟硼酸盐跟硼酸不同的是,它一定是以单体形式存在的,所以可以严密控制当量。
基本文献
- Chambers, R. D.; Clark, H. C.; Willis, C. J. J. Am. Chem. Soc. 1960, 82, 5298. DOI:10.1021/ja01505a007
- Vedejs, E.; Chapman, R. W.; Fields, S. C.; Lin, S.; Schrimpf, M. R. J. Org. Chem. 1995, 60, 3020. DOI: 10.1021/jo00115a016
- Vedejs, E.; Fields, S. C.; Hayashi, R.; Hitchcock, S. R.; Powell, D. R.; Schrimpf, M. R. J. Am. Chem. Soc. 1999, 121, 2460. DOI: 10.1021/ja983555r
- Darses, S.; Michaud, G.; Genet, J.-P. Eur. J. Org. Chem. 1999, 1875. [abstract]
- Churches, Q. I.; Hooper, J. F.; Hutton, C. A. J. Org. Chem. 2015, 80, 5428. DOI:10.1021/acs.joc.5b00182
<review>
- Darses, S.; Genet, J.-P. Eur. J. Org. Chem. 2003, 4313. DOI: 10.1002/ejoc.200300294
- Molander, G. A.; Figueroa, R. Aldrichimica Acta 2005, 38, 49. [website]
- Molander, G. A.; Ellis, N. Acc. Chem. Res. 2007, 40, 275. DOI: 10.1021/ar050199q
- Darses, S.; Genet, J.-P. Chem. Rev. 2008, 108, 288. DOI: 10.1021/cr0509758
- Oliveira, R. A. Synlett 2009, 505. DOI: 10.1055/s-0028-1083584
- Molander, G. A.; Canturk, B. Angew. Chem. Int. Ed. 2009, 48, 9240. DOI: 10.1002/anie.200904306
- Lennox, A. J. J.; Lloyd-Jones, G. C. Chem. Soc. Rev. 2014, 43, 412. DOI: 10.1039/c3cs60197h
反应机理
三氟硼酸盐具有4配位的阴离子结构,另外由于氟的吸电子效应使得其本身的亲核性很弱,从而trans-metal化比较慢。
对于铃木偶联反应来说,水解后生成的硼酸也是被认为是参与反应的。反应中的化学活性种具有slow-release的特性,所以自聚副反应比较少。(参考:Angew. Chem. Int. Ed. 2010, 49, 5156.)
反应实例
K离子变成四正丁基铵离子后可以提高化合物在非极性溶剂中的溶解性[1]。
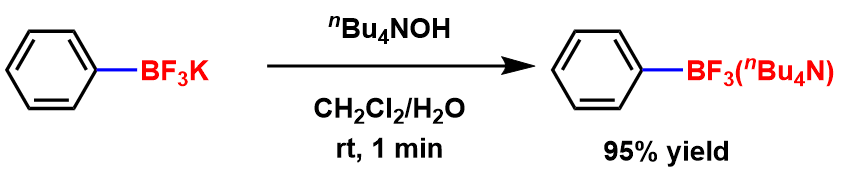
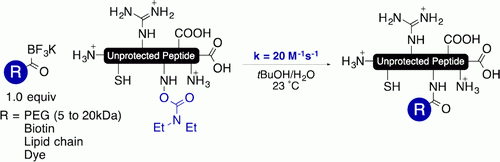
无保护多肽偶联的应用[2]
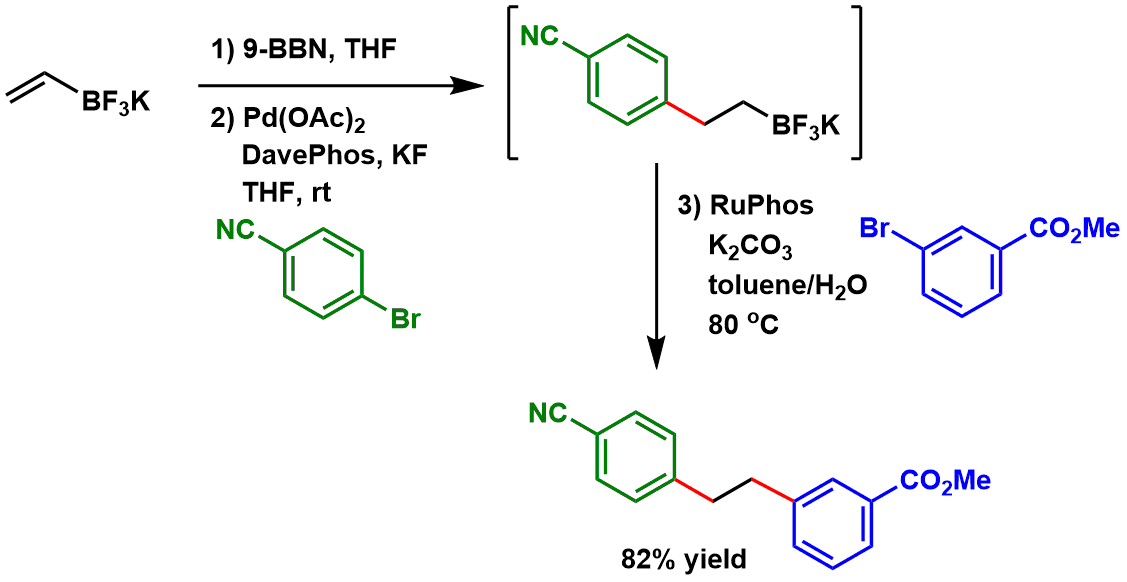
根据溶剂的不同化学选择性也有可能不同。[3]
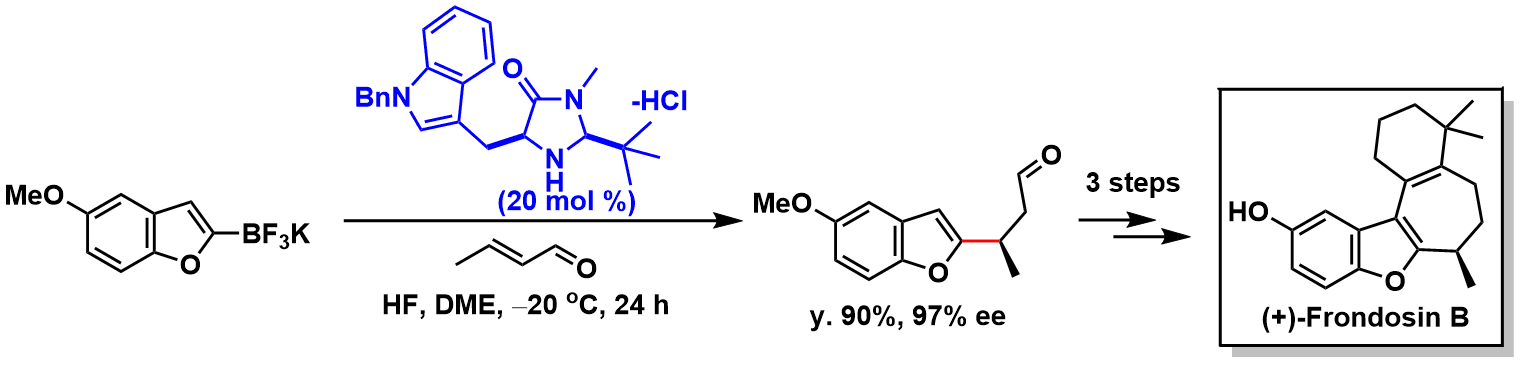
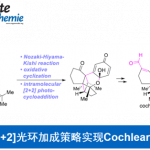
(+)-frondosin B的短步骤合成[4]: MacMillan催化剂催化的不对称共轭加成[5]是其中的关键步骤。
可见光氧化还原催化剂催化的三氟甲基化反应[6]
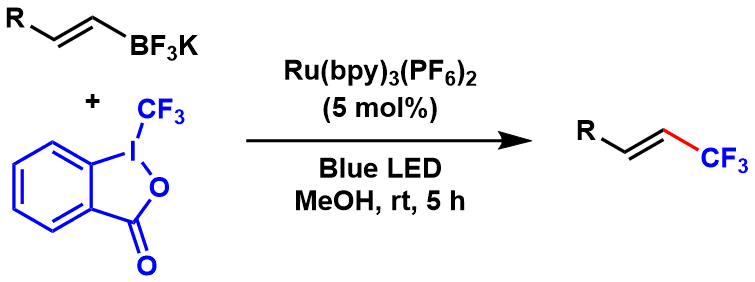
实验步骤
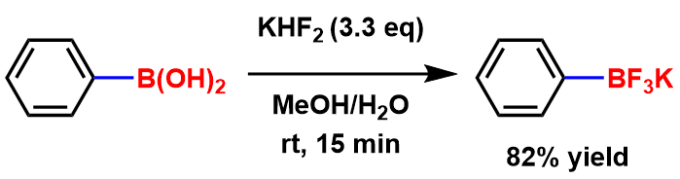
有机三氟硼酸盐的制备方法[7]:有机硼酸或者有机硼酸酯与KHF2反应即可。
苯基硼酸(ca. 169 mmol)溶解在甲醇中(50 mL)、一边搅拌一边缓慢加入过量的饱和KHF2水溶液(ca. 563 mmol)。十五分钟后,过滤收集反应产生的沉淀,再用冷的甲醇清洗。用最少量的乙腈重结晶得到纯的产物(25.5 g, 138 mmol, 82%)。
参考文献
- Batey, R. A.; Quach, T. D. Tetrahedron Lett. 2001, 42, 9099. doi:10.1016/S0040-4039(01)01983-9
- (a) Noda, H.; Eros, G.; Bode, J. W. J. Am. Chem. Soc. 2014, 136, 5611. DOI: 10.1021/ja5018442
- Molander, G.A.; Sandrock, D. L. Org. Lett. 2009, 11, 2369. DOI: 10.1021/ol900822j
- Reiter, M.; Torssell, S.; Lee, S.; MacMillan D. W. C. Chem. Sci. 2010, 1, 37. DOI: 10.1039/c0sc00204f
- Lee, S.; MacMillan, D. W. C. J. Am. Chem. Soc. 2007, 129, 15438. DOI: 10.1021/ja0767480
- Yasu, Y.; Koike, T.; Akita, M. Chem. Commun. 2013, 49, 2037. DOI: 10.1039/C3CC39235J
- Vedejs, E.; Chapman, R. W.; Fields, S. C.; Lin, S.; Schrimpf, M. R. J. Org. Chem. 1995, 60, 3020. DOI: 10.1021/jo00115a016
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.