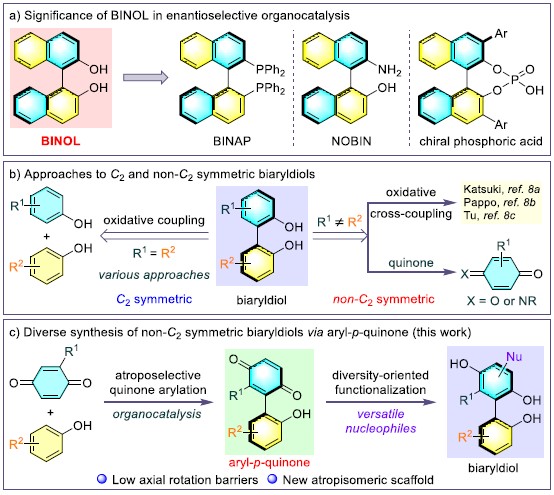
轴手性联芳基二醇骨架广泛存在于天然产物、生物活性分子、有用的手性配体以及催化剂中(Figure 1a),因此,轴手性联芳基二醇化合物的合成受到广泛关注且已经取得了不错的进展。过渡金属催化2-萘酚衍生物的氧化偶联反应是构建C2-对称轴手性联萘酚衍生物最直接有效的方法,但该策略不能有效的合成非C2-对称轴手性联萘酚衍生物。Katsuki课题组、Pappo课题组以及Tu课题组开发出了一些合成办法,但寻找新的合成非C2-对称轴手性联萘酚衍生物的方法仍然具有重要意义(Figure 1b)。最近,谭斌课题组[1]、Kurti课题组[2]和Bella课题组[3]成功实现了应用有机催化亲核加成、中心-轴向手性转换策略将醌或亚氨醌可作为苯酚的前体用于非C2-对称轴手性联萘酚衍生物的合成,但这些策略中醌及其衍生物的底物范围比较局限。在上述背景研究的基础上,南方科技大学谭斌团队和向少华团队共同报道了手性磷酸催化对醌与2-萘酚发生直接亲核加成反应,能以良好至优秀的收率得到一系列轴手性芳基醌化合物(Figure 1c)。同时,在手性磷酸催化作用下,2-氯-1,4-萘醌类似物还可与吲哚发生亲核加成反应,能以良好的收率和优秀的对映选择性得到一系列轴手性吲哚萘醌化合物。相关研究成果发表于
“Organocatalytic Enantioselective Synthesis of Atropisomeric Aryl-p-quinones: Platform Molecules for Diversity-oriented Synthesis of Biaryldiols”
Chen, Y.-H.; Li, H.-H.; Zhang, X.; Xiang, S.-H.; * Li, S.; Tan, B.* Angew. Chem. Int. Ed. 2020, Early View. DOI: 10.1002/anie.202004671
Figure 1 背景研究
论文概要
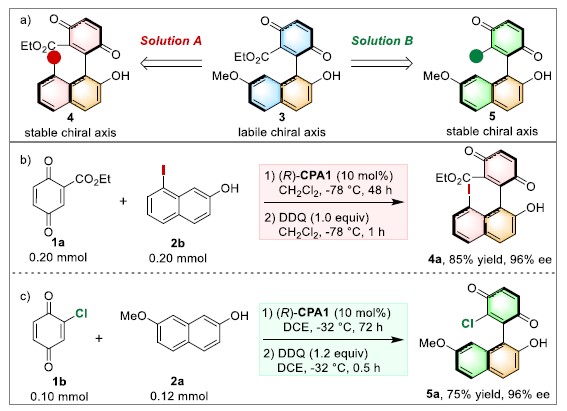
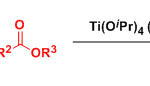
作者以1,4-苯醌1a和和2-萘酚2为模板底物,通过对催化剂、溶剂以及氧化剂等反应条件反复筛选,确定了两种最优条件(Figure 2):A)酯基取代的对醌与8-碘-2-萘酚为模板底物,(R)-CPA1为催化剂,CH2Cl2为溶剂,在-78℃条件下反应24小时后,再加入1.2 equiv 外源性氧化剂DDQ的CH2Cl2溶液,在-78℃条件下反应1小时,能以85%的收率和96%的对映选择性得到产物4a。B) 2-氯-对醌与7-甲氧基-2-萘酚为模板底物,(R)-CPA1为催化剂,DCE为溶剂,在-32℃条件下反应72小时后,再加入1.0 equiv 外源性氧化剂DDQ的DCE溶液,在-32℃条件下反应0.5小时,能以75%的收率和96%的对映选择性得到产物5a。
Figure 2 最优反应条件
在最优反应条件下,作者对反应的底物范围进行了考察。各种酯基取代的对醌、各种卤素取代的对醌以及各种给电子取代的萘酚均能较好的适应反应条件,能以良好至优秀的收率和优秀的对映选择性得到相应产物。
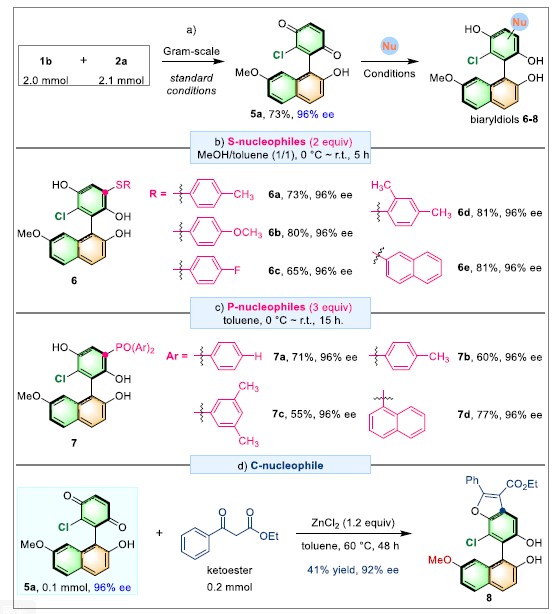
紧接着,为了证明反应的应用潜力,作者进行了一系列扩大化反应和衍生反应(Figure 3)。首先,作者对模板反应进行了扩大化反应,相应产物的收率和对映选择性能保持不变。然后,作者以5a为模板,在简单的反应条件下能分别与硫亲核试剂、磷亲核试剂以及碳亲核试剂发生亲核加成反应,能以良好的收率和优秀的对映选择性分别得到相应的化合物6,7,8。同时,在Sc(OTf)3作用下,5a还能与吲哚发生C-亲核加成反应,再经过简单的氧化过程即可得到具有重要作用的轴手性吲哚-芳基-对醌类化合物。
Figure 3 扩大化反应与衍生反应
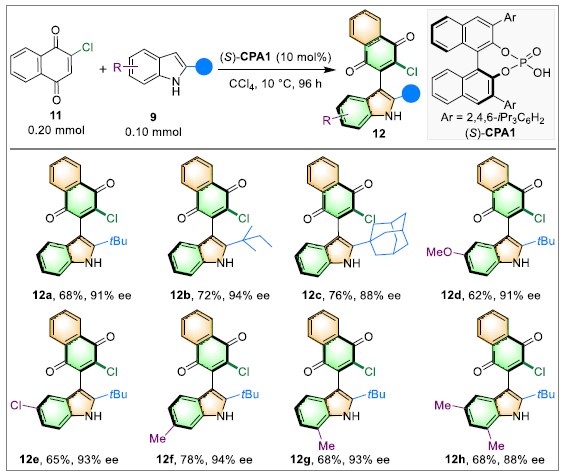
接着,通过优化上述最优条件,作者发现2-氯-1,4-萘醌可和2-叔丁基吲哚发生直接加成,能以良好的收率和优秀的对映选择性得到轴手性吲哚萘醌化合物。同时,作者考察了反应的底物范围。各种取代的2-叔丁基吲哚、2-叔戊基吲哚以及2-(1-金刚烷基)吲哚均能较好的适应反应条件,能以良好的收率和优秀的对映选择性得到相应产物(Figure 4)。
Figure 4 底物扩展
论文总结评价
南方科技大学谭斌团队和向少华团队共同报道了手性磷酸催化对醌与2-萘酚发生直接亲核加成反应,能以良好至优秀的收率得到一系列轴手性芳基醌化合物。得到的轴手性芳基醌化合物还可进一步与硫亲核试剂、磷亲核试剂以及碳亲核试剂发生亲核加成反应。同时,在手性磷酸催化作用下,2-氯-1,4-萘醌类似物还可与吲哚发生亲核加成反应,能以良好的收率和优秀的对映选择性得到一系列轴手性吲哚萘醌化合物。
参考文献
- [1] Chen, Y.-H.; Cheng, D.-J.; Zhang, J.; Wang, Y.; Liu, X.-Y.; Tan, B. Am. Chem. Soc. 2015, 137, 15062-15065. DOI: 10.1021/jacs.5b10152
- [2] Wang, J.-Z.; Zhou, J.; Xu, C.; Sun, H.; Kürti, L.; Xu, Q.-L. Am. Chem. Soc. 2016, 138, 5202-5205. DOI: 10.1021/jacs.6b01458
- [3] Moliterno, M.; Cari, R.; Puglisi, A.; Antenucci, A.; Sperandio, C.; Moretti, E. Di Sabato, A.; Salvio, R.; Bella, M. Chem. Int. Ed. 2016, 55, 6525-6529. DOI: 10.1002/anie.201601660
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!














No comments yet.