本文作者:杉杉
导读
近日,上海有机所汤文军教授课题组在美国化学学会杂志(Journal of the American Chemical Society)发表论文,报道了一种通用、实用且高效的手性邻二胺衍生物的合成方法,即通过手性联硼酸酯实现亚胺的不对称还原偶联反应。该方法具有高对映选择性、反应条件温和、操作简单、原料易得、底物范围广泛等优点。
Enantioselective Reductive Coupling of Imines Templated by ChiralDiboron
Mingkang Zhou, Kaidi Li, Dongping Chen, Ronghua Xu, Guangqing Xu, and Wenjun Tang
J. Am. Chem. Soc. 2020, 142, 10337–10342 DOI: 10.1021/jacs.0c04558
正文
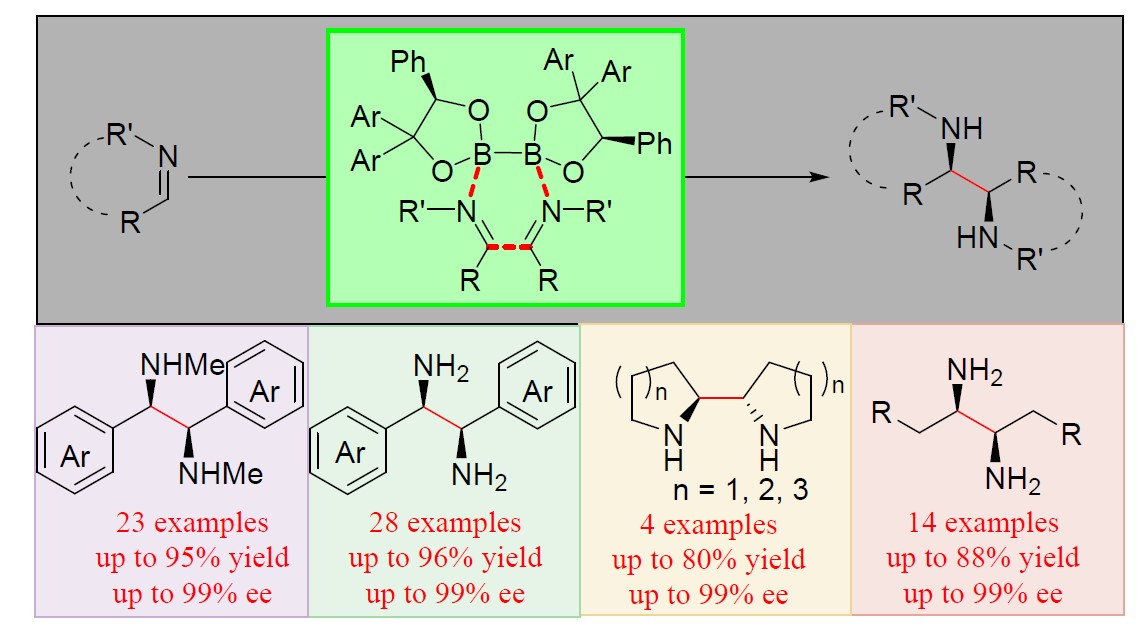
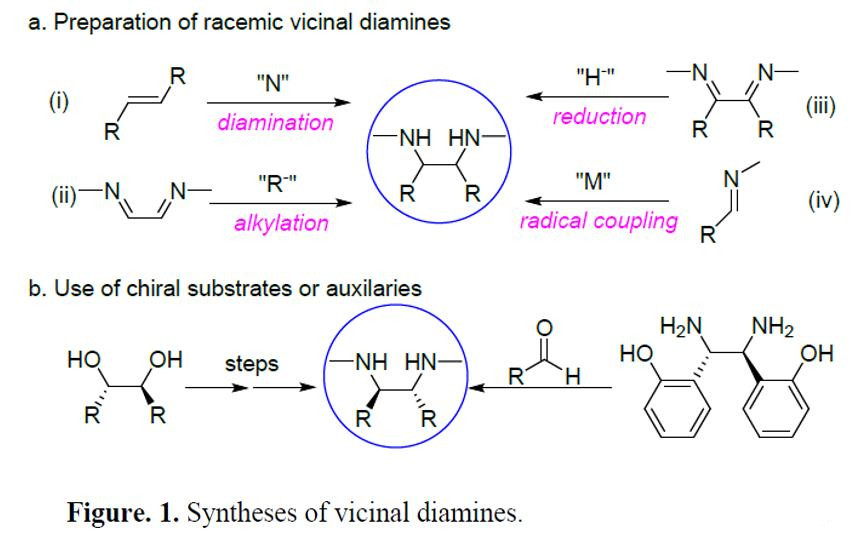
手性邻二胺化合物广泛存在药物分子、天然产物、农用化学品以及不对称催化领域中的配体或催化剂中。然而,大多数已知方法(Figure 1a)包括烯烃二氨化、二亚胺的亲核加成、二亚胺还原和亚胺的自由基偶联等,只会形成邻二胺的外消旋混合物,一半不是目标产物。此外,繁琐的纯化程序以及内消旋非对映异构体的存在,导致收率偏低。虽然,可以通过手性化合物合成目标产物(收率高),但需使用昂贵的手性原料(Figure 1b)。因此,高效且实用可合成具有优异收率和选择性的手性邻二胺化合物仍具有挑战。在此,上海有机所汤文军教授课题组报道了一种通用、简单且实用的手性邻二胺化合物的合成方法,即手性联硼酸酯促进亚胺的还原偶联反应。该反应具有高收率、优异的对映选择性、反应条件温和、操作简单、原料易获、底物范围广泛等特点。
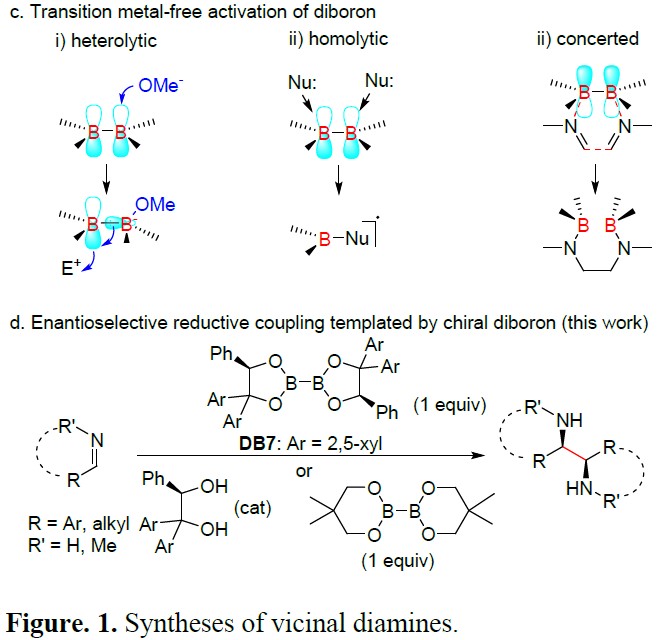
二硼化合物可在过渡金属催化下,构建碳-硼键。同时,也可在无过渡金属催化的条件下,通过简化活化过程,在碱性条件下与亲电试剂反应(Figure. 1c),或者通过均相裂解产生自由基发生反应。手性二醇合成的手性二硼化合物,可作为构建具有高立体特异性和对映选择性碳-碳键的高效“模板”。前期,本课题组通过使用手性二硼试剂实现异喹啉的还原,并以高产率、出色的对映选择性获得目标产物,涉及 [3,3]-σ重排。因此,作者设想,手性二硼化合物也可作为还原偶联的模板,可适用于各种亚胺底物的还原,从而合成手性邻二胺衍生物(Figure 1d)。
首先,作者使用苯甲胺2a(苯甲醛1a和氨反应生成)作为底物,对手性二硼化硼DB1–7进行还原偶联反应的研究(Figure. 2)。当使用DB1时,获得80%收率的3a,但ee仅为20%。当使用DB2和DB3时,ee均有所提高。此外,使用衍生自非C2对称手性二醇的DB4时,ee可达57%。而使用体积较大的DB5时,收率高达87%,但ee不佳。而使用位阻更高的DB6时,ee可提至80%。通过对乙硼烷结构的进一步优化,从而获得DB7,可将收率提至90%和ee高达95%。
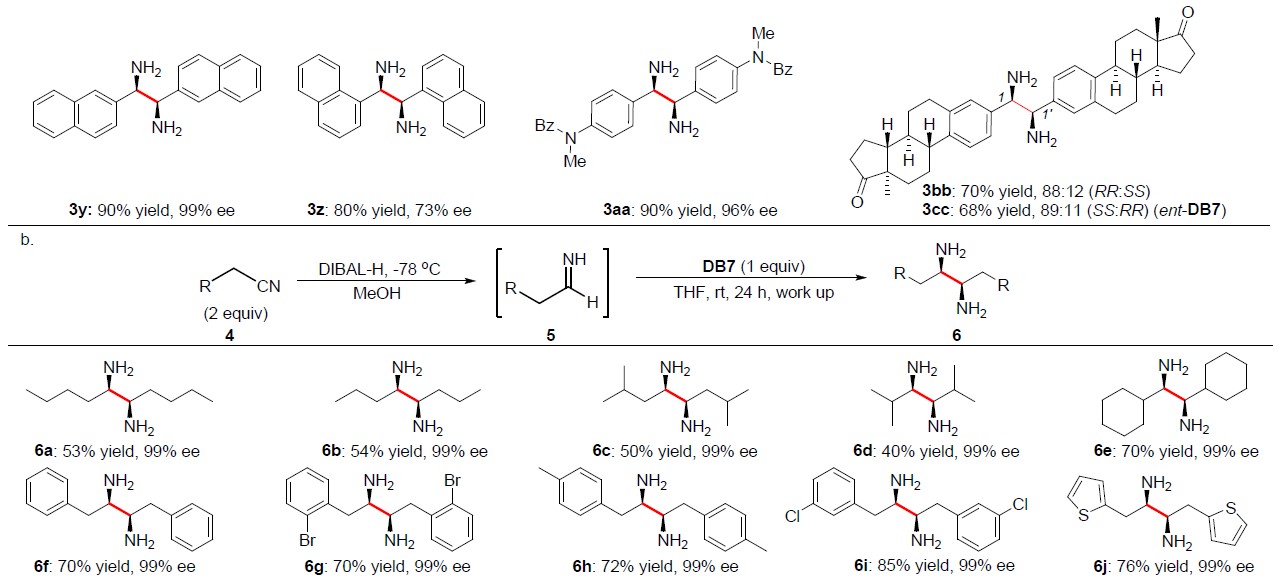
在获得上述最佳反应条件后,作者开始对亚胺底物进行了扩展(Figure. 3)。当使用芳基亚胺2作为底物时,反应不受电子效应和定位效应的影响,均与体系兼容,从而获得相应的产物3b–3t。同时,呋喃、噻吩的杂环以及萘环也适用于该体系,获得相应的产物3u–3z。此外,雌酚酮骨架也是相容的,而自偶联产物中二胺部分的手性取决于二硼的手性,从而获得3bb或3cc的非对映异构体混合物(9:1或1:9)。
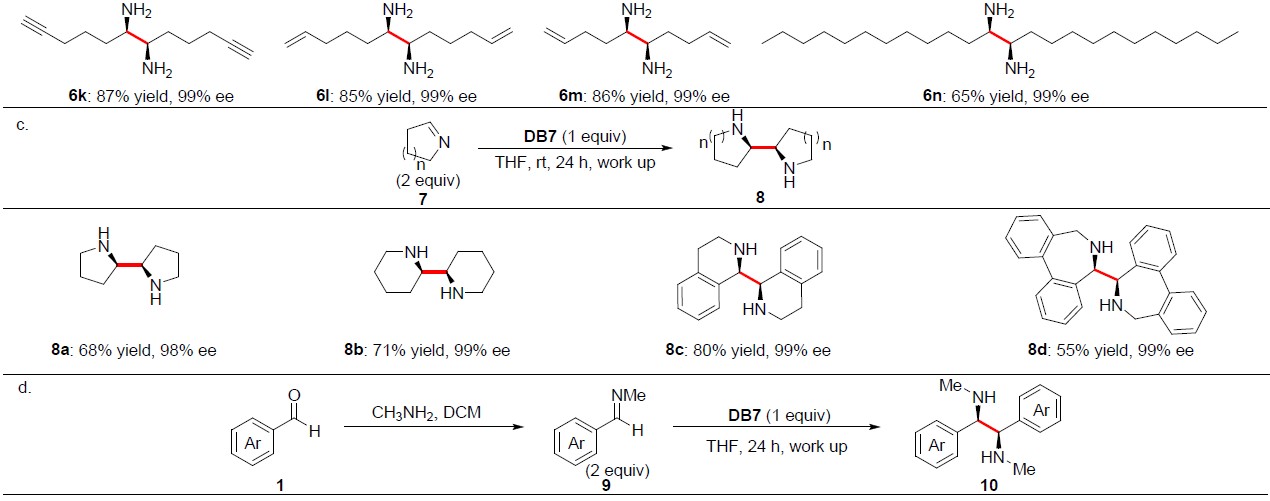
除芳基亚胺外,脂肪族亚胺5也可获得令人满意收率和对映选择性的1,1′-二烷基取代的邻二胺衍生物6。反应结果表明,具有伯烷基、仲烷基、苄基、噻吩基、烯烃、炔烃取代基均与体系相容,从而获得相应的产物6a–6n。同时,含有卤素、烯烃和炔烃官能团可为后期修饰提供多种可能。
同时,环亚胺7也适用于该还原偶联反应。如手性2,2′-联吡咯烷、2,2′-联哌啶、1,1′-八环双异喹啉和5,5′-四氢二苯并[c,e]氮杂,均可获得相应产物8a–8d。
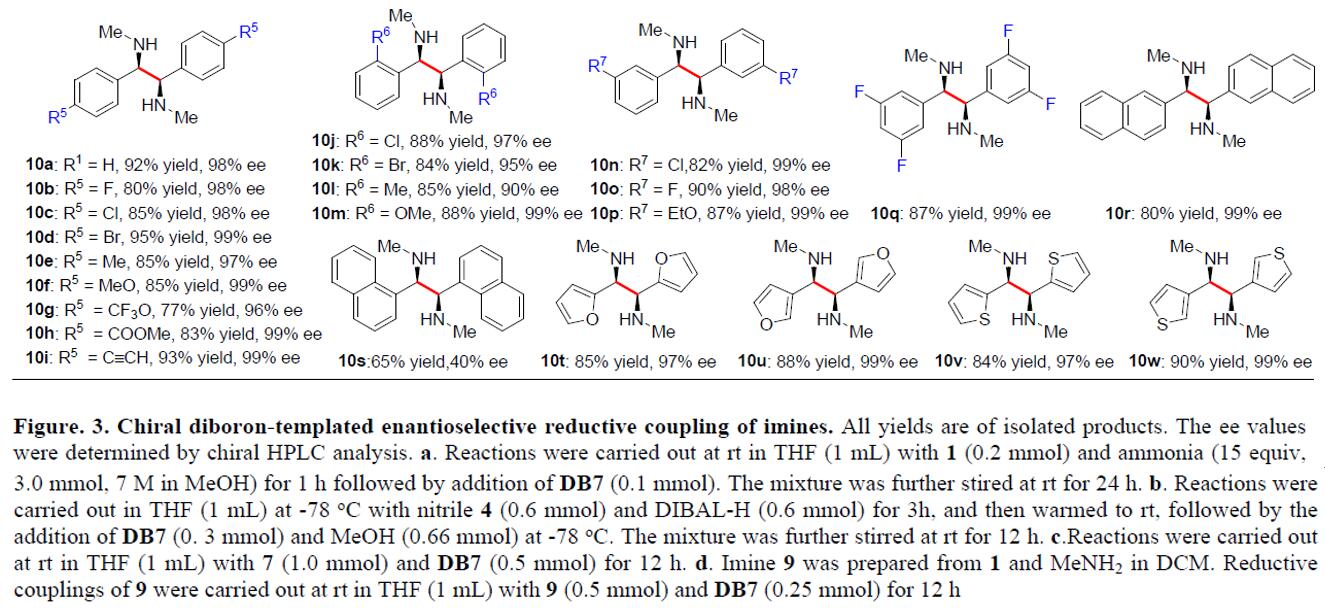
此外,N-甲基芳基亚胺9同样适用于该还原偶联反应,从而获得相应的产物10a–10w。然而,较大体积的N-烷基芳族醛亚胺(如N-乙基苯甲二胺)对于该反应是惰性的。
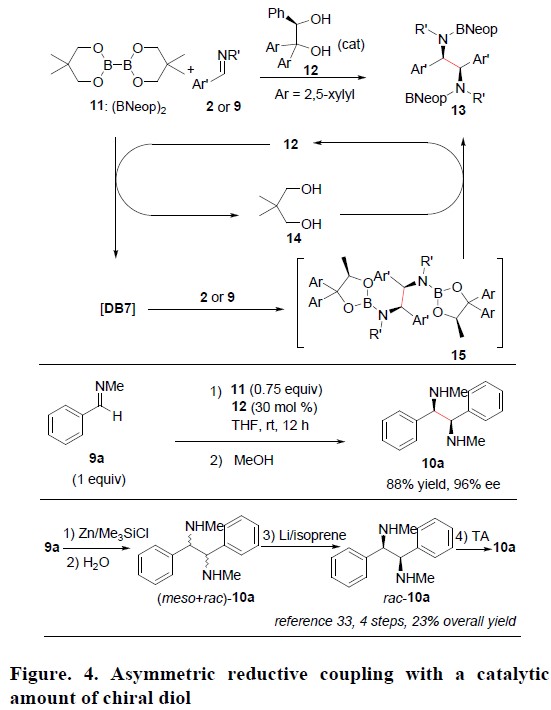
此外,该反应不限于手性联硼酸酯 DB7的化学计量使用,对于稳定的芳基亚胺2或9,使用化学计量的(BNeop)2(11)和催化量的手性二醇12同样可以实现不对称还原偶联反应(Figure. 4)。因此,通过使用双(新戊基乙二醇基)二硼作为非手性二硼源和30 mol%的手性二醇12作为催化剂,9a可顺利进行还原偶联获得10a,这是一种用于不对称氢化的有效手性配体,收率为88%和96% ee。当(BNeop)2与9a混合时,未观察到还原偶联产物。当添加12时,反应可在24h内完成,表明手性双硼DB7在促进对映选择性和反应性上至关重要。
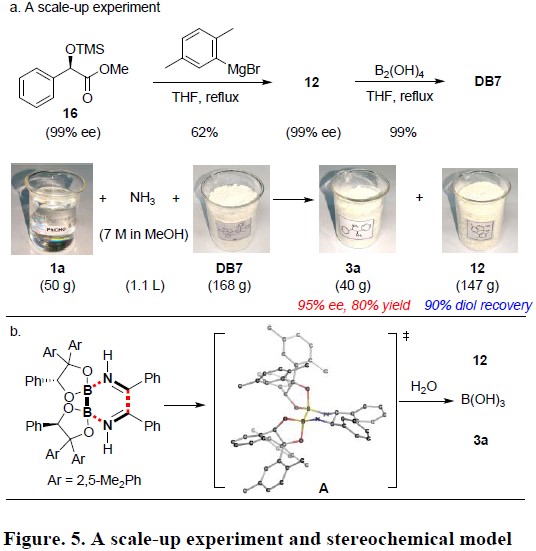
为了证明反应的实用性,作者进行可克级实验(Figure. 5a)。首先,使用2,5-二甲苯基格氏试剂与(R)-扁桃酸衍生物16反应,获得62%的收率的手性二醇12,12再与四羟基二硼在THF中反应,获得几乎定量收率的DB7。随后,向溶解在NH3/MeOH (7 M,1.1L)中的1a(50g)溶液中加入DB7(168g),并将混合物在室温搅拌24 h,再经酸/碱后处理后,获得80%收率和95% ee的产物3a(40g),同时手性二醇12(147 g)的回收率为90%。该方法作为合成手性邻二胺最有效方法之一。
该反应均获得高收率和对映选择性的手性邻二胺衍生物,同时均未观察到内消旋产物,从而说明二硼化合物可促进[3,3]-σ重排过程。此外,使用(BNeop)2作为二硼源和二醇12作为催化剂的成功方案,进一步证明了手性二硼结构在促进反应性和对映选择性方面的重要性。二硼的空间体积大且刚性的二氧杂硼烷对于提供有效的六元环过渡态A至关重要(Figure. 5b),从而允许进行高效的还原偶联。
总结
上海有机所汤文军教授课题组报道了一种简单、高效且实用的手性邻二胺衍生物的合成,即通过手性联硼酸酯实现亚胺的不对称还原偶联反应。该方法具有高对映选择性、反应条件温和、操作简单、原料易得、底物范围广泛(芳基亚胺、脂肪族亚胺、环亚胺、N-甲基芳基亚胺)等优点。同时,该反应涉及[3,3]-σ重排过程。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!



















No comments yet.