作者:杉杉
导读:
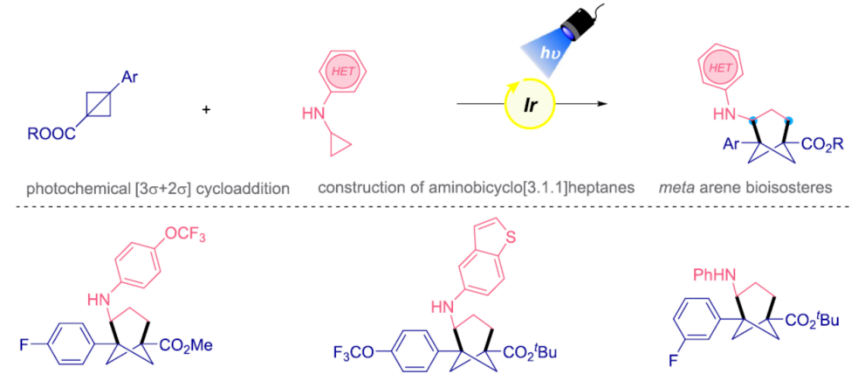
近日,美国Pennsylvania大学的G. A. Molander课题组在J. Am. Chem. Soc.中发表论文,报道首例光诱导的BCB (bicyclo[1.1.0]butane)与CPA (cyclopropylamine)之间的分子间 [3σ+2σ]环加成反应方法学,进而成功完成一系列三取代BCHep (bicyclo[3.1.1]heptane)分子的构建。
Photochemical Intermolecular [3σ + 2σ]-Cycloaddition for the Construction of Aminobicyclo[3.1.1]heptanes
Y.Zheng, W.Huang, R. Dhungana, A. Granados, S. Keess, M. Makvandi, G. A. Molander, J. J. Am. Chem. Soc.2022, 144, 23685. doi: 10.1021/jacs.2c11501.
正文:
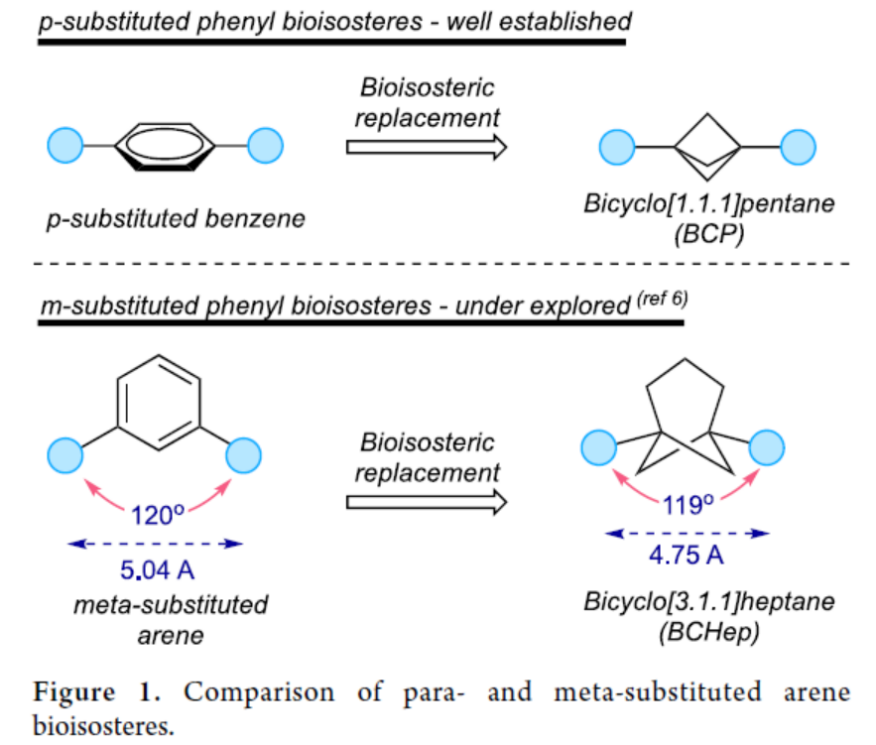
目前,构建BCP (bicyclo[1.1.1]pentane)分子的合成反应方法学研究,已经备受诸多研究团队的广泛关注[1]。然而,对于构建BCHep (bicyclo[3.1.1]heptane)分子的合成转化策略,目前却较少有相关的研究报道 (Figure 1) [2]。
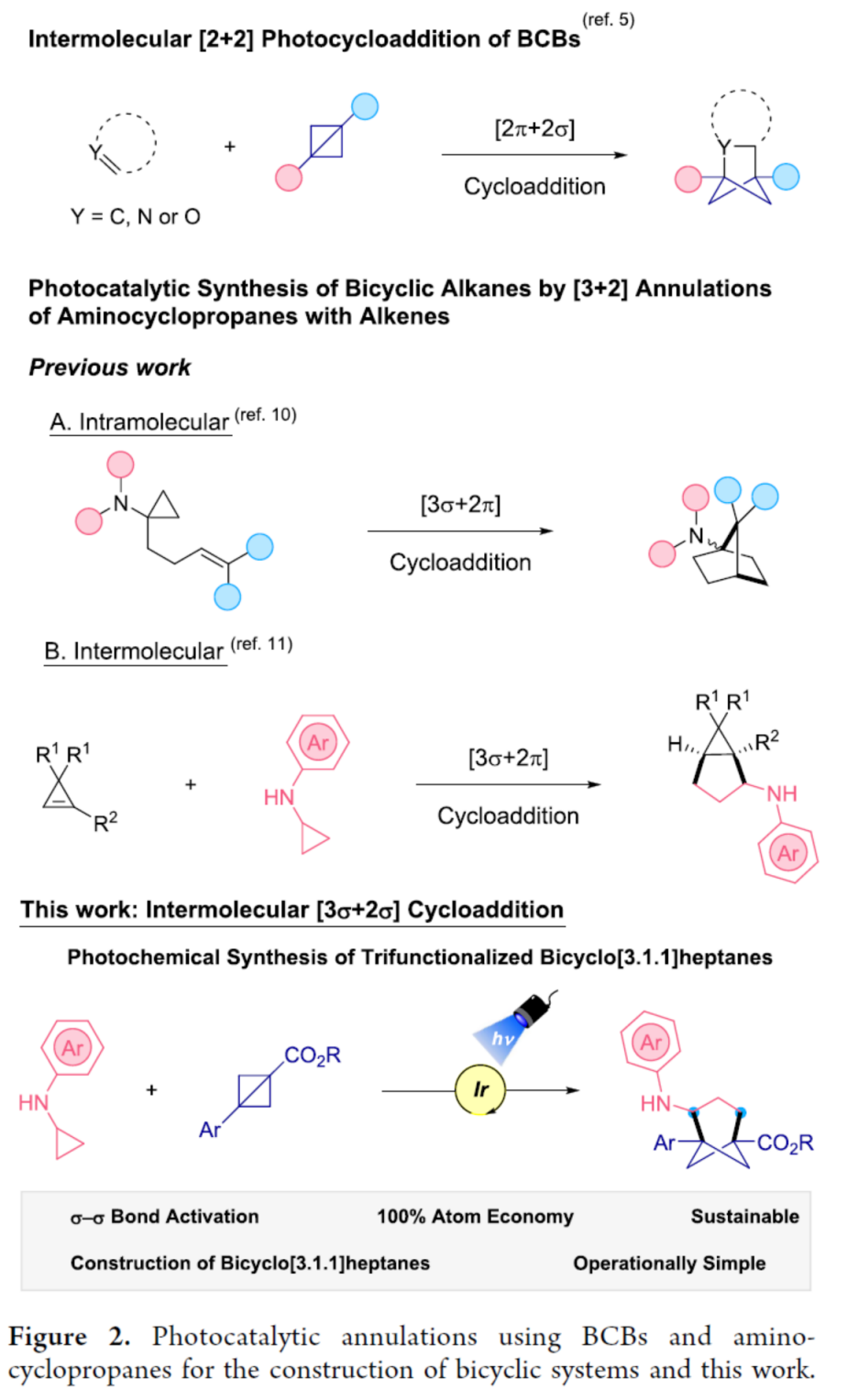
这里,受到近年来对于采用BCB分子参与分子间[2+2]光环加成[3]反应方法学、分子内[3σ+2π]环加成[4]反应方法学以及分子间[3σ+2π]环加成反应[5]方法学相关研究报道的启发,美国Pennsylvania大学的G. A. Molander课题组报道首例光诱导的BCB (bicyclo[1.1.0]butane)与CPA (cyclopropylamine)之间的分子间 [3σ+2σ]环加成反应方法学 (Figure 2)。
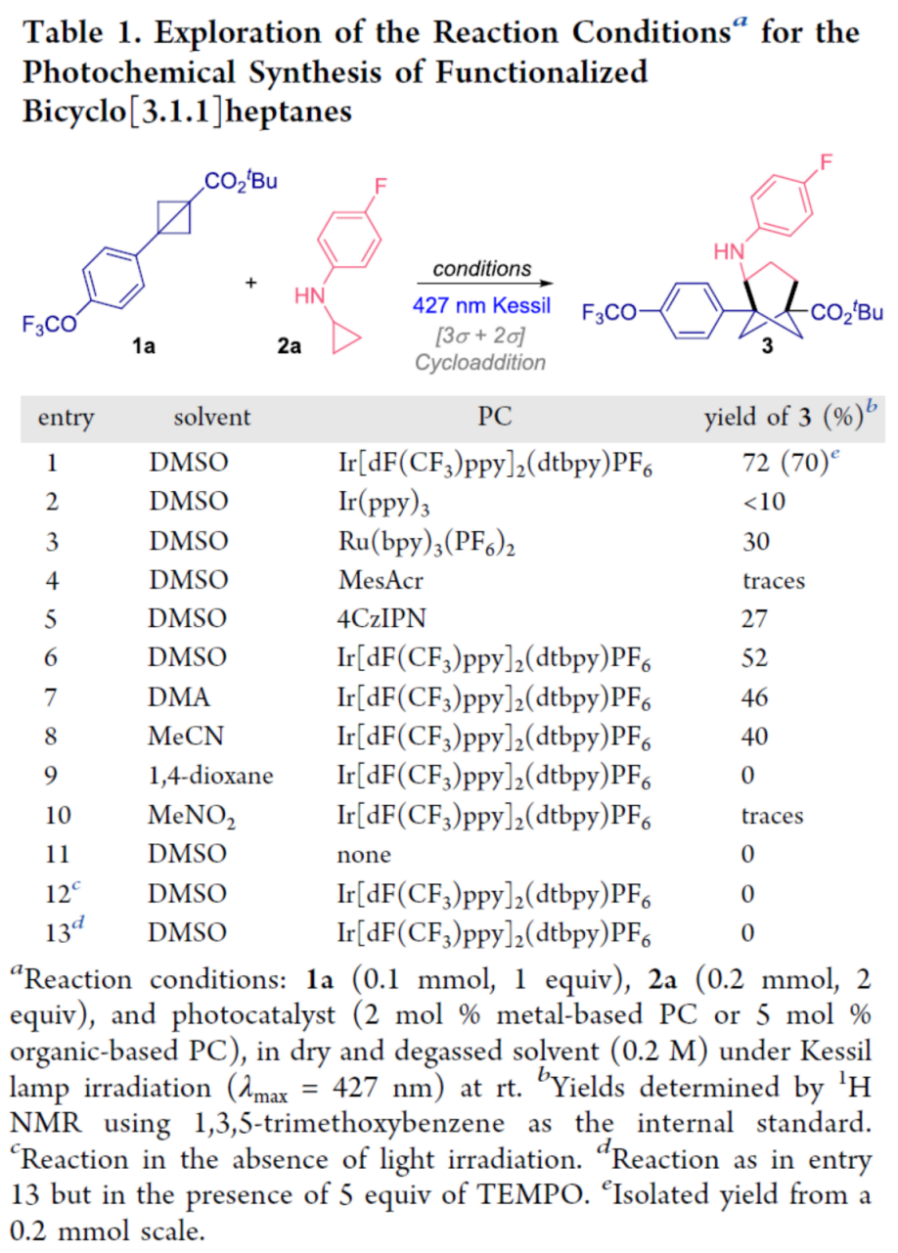
首先,作者采用BCB 1a与CPA 2a作为模型底物,进行相关反应条件的优化筛选 (Table 1)。进而确定最佳的反应条件为:采用Ir[dF(CF3)ppy]2(dtbpy)PF6作为光催化剂,427 nm 蓝光 (Kessil Lamp)辐射, DMSO作为反应溶剂,反应温度为室温,最终获得70%收率的BCHep产物3。
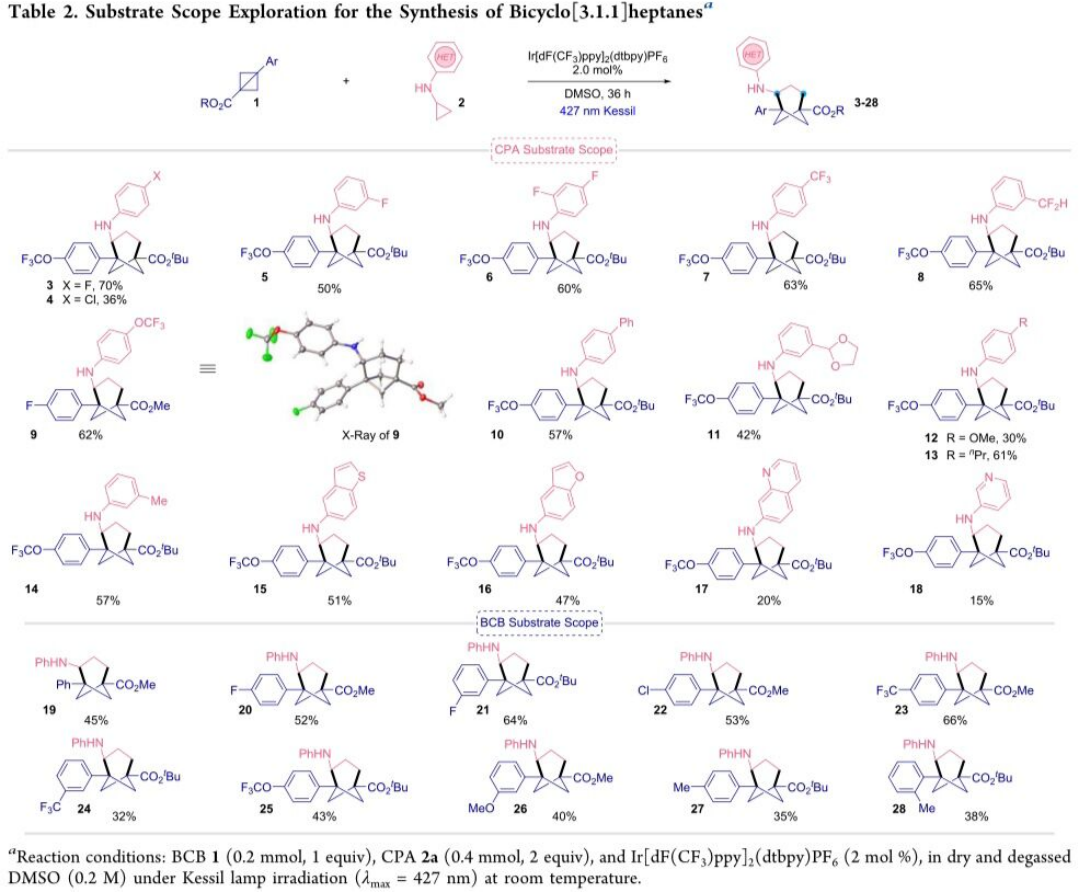
在上述的最佳反应条件下,作者分别对一系列CPA与BCB底物 (Table 2)的应用范围进行深入研究。

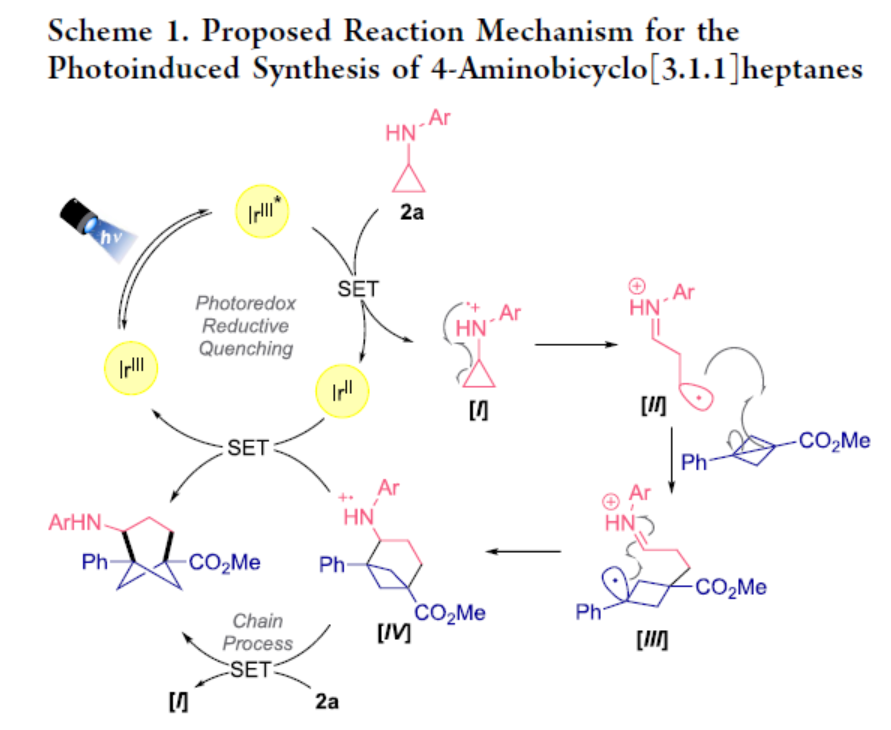
同时,基于前期相关的文献报道[4]-[6],作者提出如下合理的反应机理 (Scheme 1)。
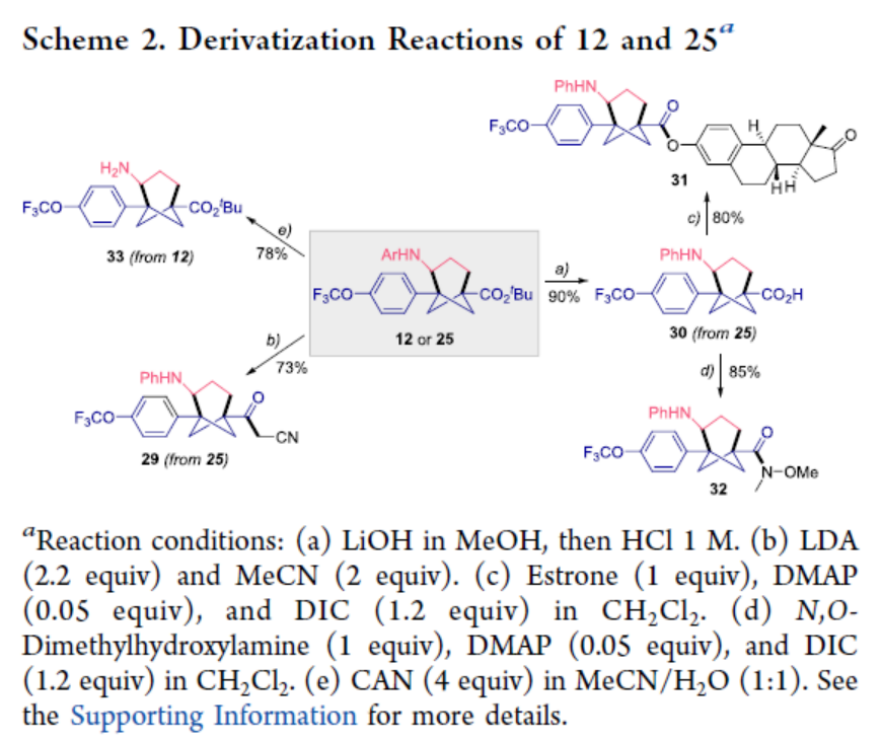
之后,该小组通过如下的一系列研究进一步表明,这一全新的分子间[3σ+2σ]-环加成策略具有潜在的合成应用价值 (Scheme 2)。
总结:美国Pennsylvania大学的G. A. Molander团队成功设计出首例光诱导的BCB (bicyclo[1.1.0]butane)与CPA (cyclopropylamine)之间的分子间 [3σ+2σ]环加成反应方法学,进而成功完成一系列三取代BCHep分子的构建。这一全新的[3σ+2σ]环加成策略具有温和的反应条件、广泛的底物范围以及优良的官能团兼容性等优势。
参考文献:
- [1] J. Kanazawa, M. Uchiyama, Synlett 2019, 30, 1. doi: 10.1055/s-0037-1610314.
- [2] T. Iida, J. Kanazawa, T. Matsunaga, K. Miyamoto, K. Hirano, M. Uchiyama, J. Am. Chem. Soc. 2022, 21848. doi: 10.1021/jacs.2c09733.
- [3] Y. Liang, R. Kleinmans, C. G. Daniliuc, F. Glorius, J. Am. Chem. Soc. 2022,
- 144, 20207. doi: 10.1021/jacs.2c09248.
- [4] D. Staveness, J. L. Collins, R. C. McAtee, C. R. J. Stephenson, Angew. Chem., Int. Ed. 2019, 58, 19000. doi: 10.1002/anie.201909492.
- [5] B. Muriel, A. Gagnebin, J. Waser, Chem. Sci. 2019, 10, 10716. doi: 10.1039/C9SC03790J.
- [6] Y. Cai, J. Wang, Y. Zhang, Z. Li, D. Hu, N. Zheng, H. Chen, J. Am. Chem. Soc. 2017, 139, 12259. doi:10.1021/jacs.7b06319.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载



















No comments yet.