作者:石油醚
导读:
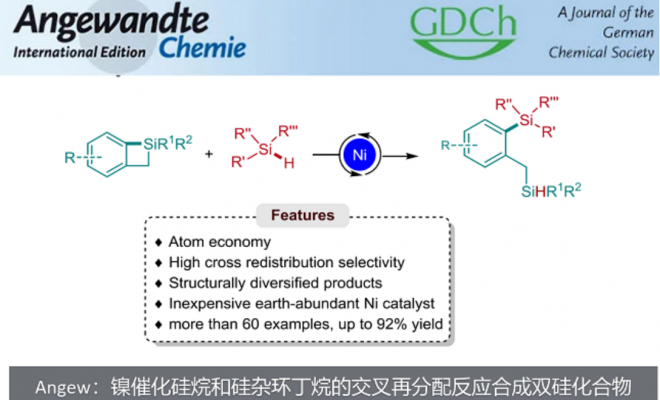
近日,武汉大学高等研究院的沈晓课题组首次报道了镍催化硅烷和苯并硅杂环丁烷的交叉再分配反应合成双硅化合物, 利用焓驱动的策略实现了高选择性的交叉再分配反应。相关成果发表于Angew. Chem. Int. Ed上。
“Nickel-Catalyzed Cross-Redistribution between Hydrosilanes and Silacyclobutanes Kezhuo Zhang, Chenchen Li, Yining Jia, Wanxiang Zhao*
Angew. Chem. Int. Ed. 2022, ASAP. doi: 10.1002/anie.202213431”
正文:
有机硅化合物在化学工业和材料科学中具有重要的价值。具有Si-H键的有机硅烷在各种转化中作为氢原子或者氢化物给体尤其重要。就像强大的烯烃复分解反应可以从廉价的烯烃获得高附加值的烯烃一样,选择性的硅烷再分配反应(即硅氢键和硅碳键的交换)也可能具备从两个简单硅烷制备高级硅烷的潜力。尽管HSiCl3的自身再分配反应已经是制备SiH4的工业手段,但是选择性交叉再分配反应仍是一个巨大的挑战。要获得高的交叉再分配选择性,需要克服以下几个困难(图1):(1)如何抑制自身再分配反应;(2)如何抑制硅烷脱氢偶联的副反应;(3)如何避免新形成的硅氢键的过度反应?以往的工作大多是通过生成硅烷气体来促进反应,是一种熵驱动的策略。最近,武汉大学高等研究院的沈晓课题组首次报道了镍催化硅烷和苯并硅杂环丁烷的交叉再分配反应合成双硅化合物, 利用焓驱动的策略实现了高选择性的交叉再分配反应。

图1: 硅烷再分配反应研究背景和本文的策略
经过一系列条件筛选,作者确定了最优条件为:当Ni(COD)2的摩尔分数为10 mol%,(p-MeC6H4)3P的摩尔分数为20 mol%时,反应在40 oC下3 h内完成,以90%的产率得到所需的交叉再分配产物3a,并在此条件下对底物进行拓展。该反应具有广泛的底物范围,对于二芳基硅烷、一芳基一烷基硅烷、两烷基硅烷、三芳基硅烷、三烷基硅烷以及烷基芳基的三取代硅烷均能取得中等到良好的收率。其中包括含有供电子取代基、吸电子取代基和杂原子取代的硅烷底物。值得提出的是,对于工业上常用的硅氧烷和氯硅烷底物,也能在该条件下顺利反应得到双硅化合物。对于天然氨基酸衍生的复杂硅烷底物也能参与到反应中以中等收率得到相应的双硅产物(图2)。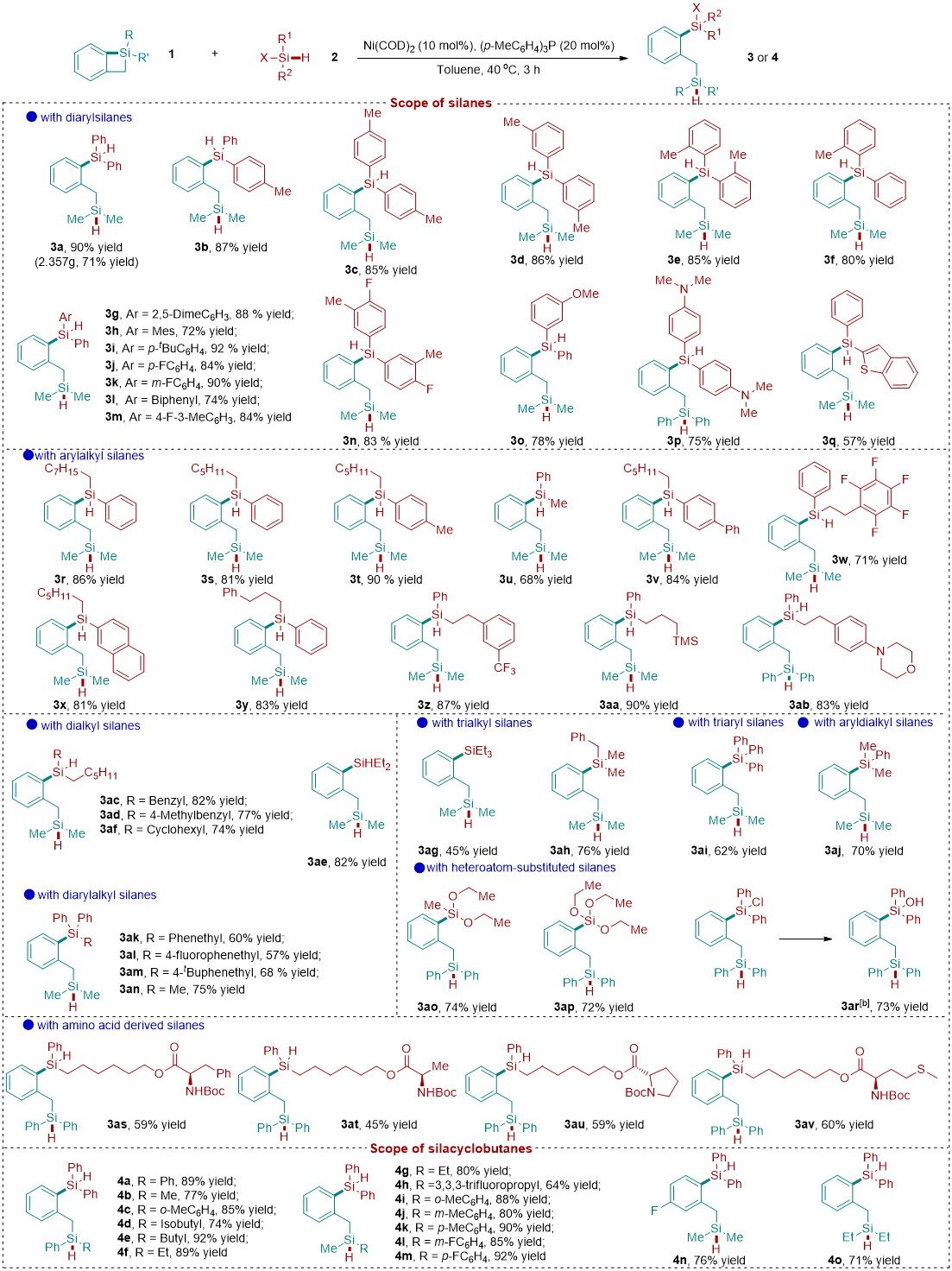
图2: 底物拓展
随后作者尝试对含有硅氢的双硅化合物进行转化。通过Rh催化的分子内脱氢反应,3a以81%的产率转化为环双硅化合物5。除了过渡金属催化剂外,B(C6F5)3在硅氢化反应中也表现出良好的性能。作者以5%的B(C6F5)3为催化剂,实现了丙酮的硅氢化反应,合成了六元环硅氧烷6,产率84%。在类似条件下,苯甲腈经历可能的中间体7经水解后,以84%的产率得到苯甲胺8。当硅上取代基的电性不同时,硅氢的反应活性是不同的,作者利用这一特性实现了在同一个分子中有两个硅氢键的选择性硅氢化,在B(C6F5)3的催化下4b能与苯乙烯反应,选择性的在烷基取代的硅氢键上发生硅氢化以78%的收率得到化合物9。剩余的一个硅氢也可以在碱性条件下高效的被转化为硅羟基,以81%的收率得到化合物10。通过C-H硅烷化反应合成六元硅杂环化合物更具挑战性,因为需要生成高能量的七元环金属中间体。作者发现了一种Rh催化分子内碳氢键硅基化反应,以硅烷再分配产物为底物来实现此类分子的构建。结果表明,以[Rh(COD)Cl]2为催化剂,Xantphos为配体,在甲苯中反应效果较好,以60%~80%的产率合成了11a到11h的二硅苯并环己烷(图3)。这些后续化学转化都展示了作者开发的方法学的合成应用价值。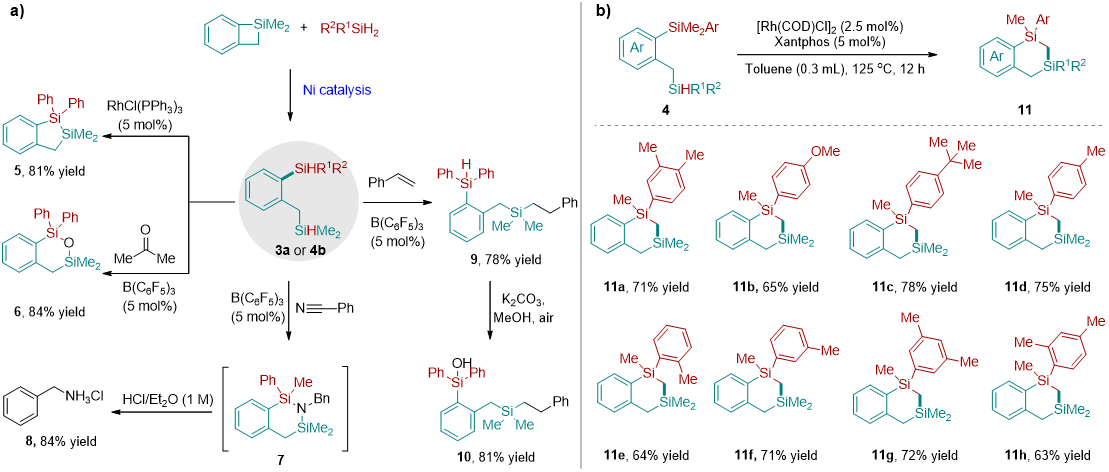
图3: 双硅产物的转化与应用
为了更加深入的了解硅烷与环硅化合物的再分配反应的机理,作者进行了一系列的机理验证实验,并结合DFT计算,对这个反应的机理进行研究。首先,为了探究反应是否经历自由基的历程,作者在标准模板反应中加入自由基抑制剂TEMPO,反应可以进行,这表明产物的形成不太可能涉及自由基机制(图4-a)。在模板反应中,作者将Ph2SiH2替换为Ph2SiD2,发现产物中的硅氢均是氘代的硅氢,说明产物中的氢来源于硅烷(图4-b)。当将Ph2SiH2/Ph2SiD2(1:1)混合加入到模板反应中时,KIE只有1.08左右,并没有发现大的KIE效应(图4-c)。为了更清楚的了解硅氢键的断裂过程,作者还进行了平行实验进行KIE的探究,得到KIE的数值为1(图4-d),说明在这个反应中硅氢键的断裂在动力学上并不显著,也就是说硅氢键的断裂并没有参与到决速步中。作者对反应组分的动力学进行了研究(图4-e)。作者首先研究了Ph2SiH2不同浓度下的初始速率,发现该速率对Ph2SiH2的浓度呈现零级动力学效应,这与KIE结果一致,表明Ph2SiH2的Si-H键的断裂不参与到决速步中。然后作者接着研究了催化剂和1a不同浓度下的初始速率,发现反应速率与催化剂(Ni(COD)2+2(p-MeC6H4)3P)和1a的浓度呈一级动力学效应,表明1a在催化剂作用下C-Si键的断裂可能是反应的决速步骤。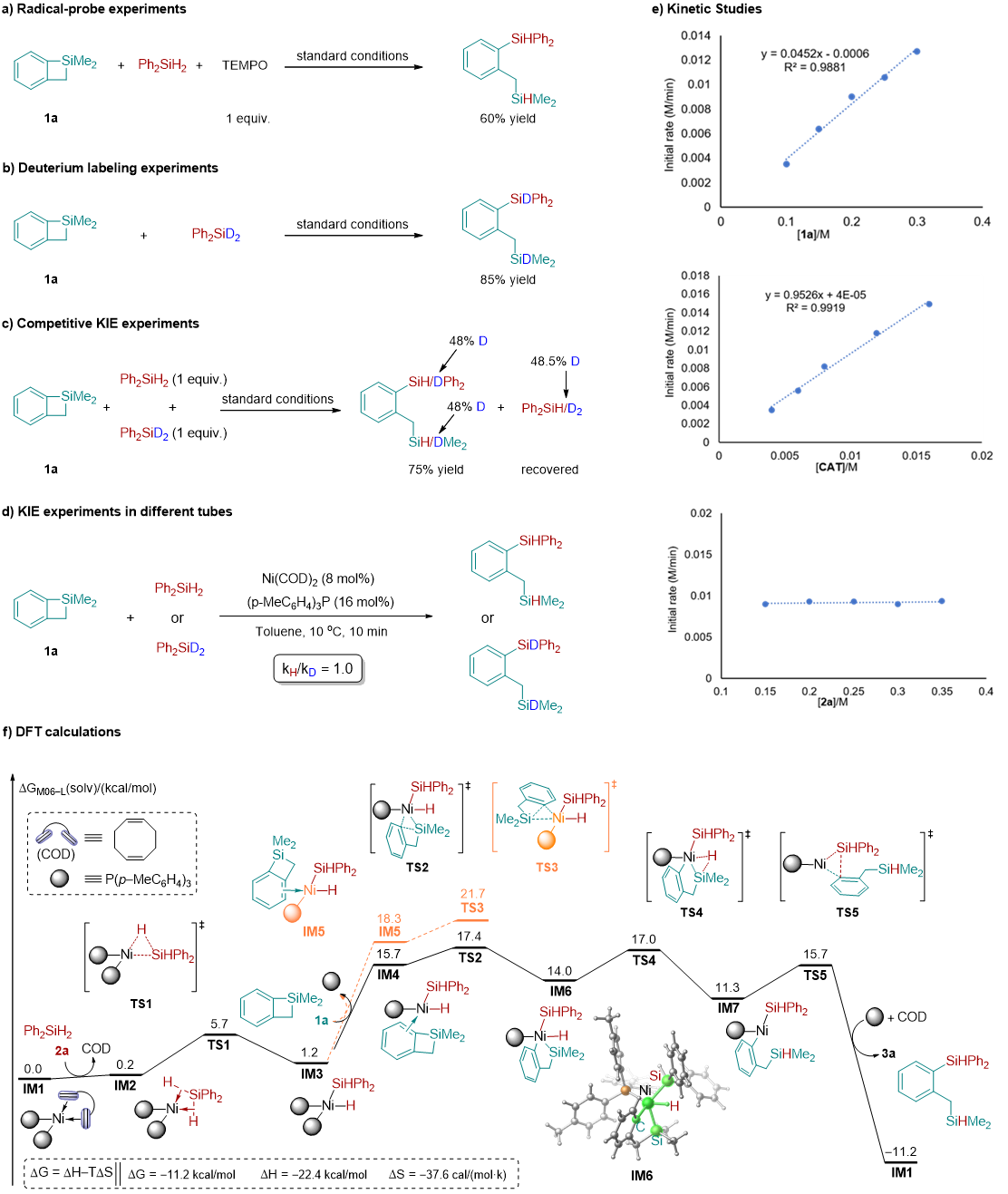
图4: 机理研究与DFT计算
基于这些实验结果和有关镍催化反应的相关报道,作者提出了一个可能的镍催化二苯基硅烷和苯并四元环硅的交叉再分配反应的催化循环机理。如图5所示,首先Ni(COD)2和2(p-MeC6H4)3P络合配位生成零价镍物种I与Ph2SiH2发生配体交换得到中间体II, 然后Ni(0)与二苯基硅烷的硅氢键发生氧化加成生成二价镍中间体III.随后苯并环硅的硅碳键与二价镍中间体III发生氧化加成得到四价镍中间体IV。最后,硅氢键与硅碳键分别发生还原消除得到目标产物3a并重生了催化剂活性物种I。DFT计算的结果进一步支持了作者提出催化循环机理,反应整个历程的吉布斯自由势能如图4-f所示。Ni(0)中间体IM1与二苯基硅烷2a发生配体交换生成中间体IM2所需要的能量仅为0.2 kcal/mol。随后硅氢键的氧化加成经过过渡态TS1生成Ni(II)-中间体IM3所需要的的能量为5.5 kcal/mol。这个计算结果表明零价镍可以很容易的被二苯基硅烷氧化为二价镍。另一种硅烷底物苯并四元环硅1a可以通过配体交换与Ni(II)中心配位,后续发生的配体交换如果发生在镍上氢原子的反式会生成中间体IM5,相应的通过过渡态TS3的Si-C键氧化加成反应需要21.7 kcal/mol的活化自由能。当配体交换发生在镍上硅原子的反式会形成中间体IM4,相应的通过过渡态TS2的Si-C键氧化加成反应生成Ni(IV)中间体IM6需要17.4 kcal/mol的活化自由能,比经历TS3所需要的能量低4.3 kcal/mol。随后的Si-H还原消除通过过渡态TS4生成Ni(II)中间体IM7,势垒为2.7 kcal/mol。最后,通过过渡态TS5的Si-C键还原消除得到产物3a并再生Ni(0)物种IM1。该步骤的势能垒为4.4 kcal/mol,自由能降低为22.5 kcal/mol。计算结果表明,通过Si-C键氧化加成生成的Ni(IV)络合物具有最高的活化自由能,可能是决速步。计算的结果与动力学结果是一致的。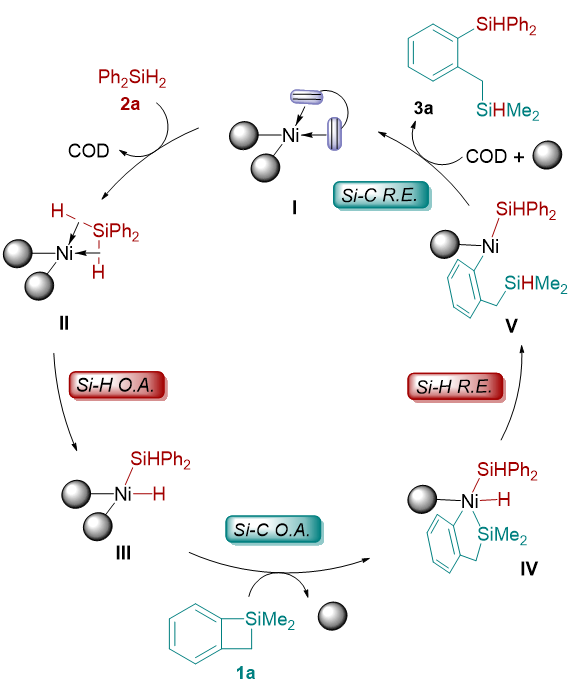
图5: 机理预测
总结:
在该工作中,沈晓课题组报道了一种硅烷和苯并硅杂环丁烷在镍催化下的选择性交叉再分配反应。该反应能够成功的关键是由于在熵驱动下苯并四元环硅环张力的释放。这与之前的通过生成硅烷气体的焓驱动的硅烷再分配反应在反应模式上是不一样的。该反应具有广泛的底物范围。实验和计算相结合的机理研究支持反应是通过Ni(0)-Ni(II)-Ni(IV)催化循环进行的。其中环硅通过环张力释放的氧化加成步骤是整个再分配反应能够成功的关键。高等研究院博士研究生陈绍维为第一作者。计算部分的工作由重庆大学博士研究生何晓倩完成。沈晓教授、蓝宇教授和加州大学洛杉矶分校Houk教授为通讯作者。
该研究得到了中国国家自然科学基金委、中国中央高校基本科研业务费、武汉大学人才启动经费和美国国家自然科学基金委的支持。
(沈晓教授供稿)
相关链接
沈晓课题组常年招收博士后,研究生,感兴趣的同学请直接联系沈晓老师(xiaoshen@whu.edu)课题组链接:http://xiaoshen.whu.edu.cn/index.php
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载

















No comments yet.