本文作者:自由基先生
导读
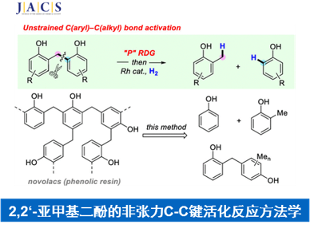
近日,美国Chicago大学的董广斌课题组在J. Am. Chem. Soc.中发表论文,报道一种全新的采用铑催化剂参与的通过RDG (removable directing group)策略进行的2,2′-亚甲基二酚化合物的氢解反应方法学,进而顺利实现一系列单酚类化合物的构建。这一全新的C-C键活化策略表现出良好的官能团兼容性与广阔的合成应用前景。
Catalytic Activation of Unstrained C(Aryl)−C(Alkyl) Bonds in 2,2′-Methylenediphenols, J. Zhu, Y. Xue, R. Zhang, B. L. Ratchford, G. Dong, J. Am. Chem. Soc. 2022, ASAP. doi: 10.1021/jacs.1c13342.
正文
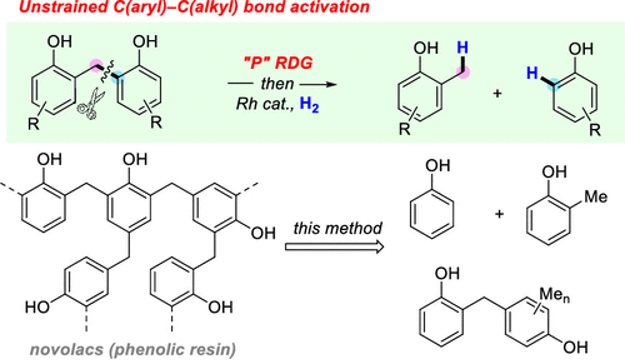
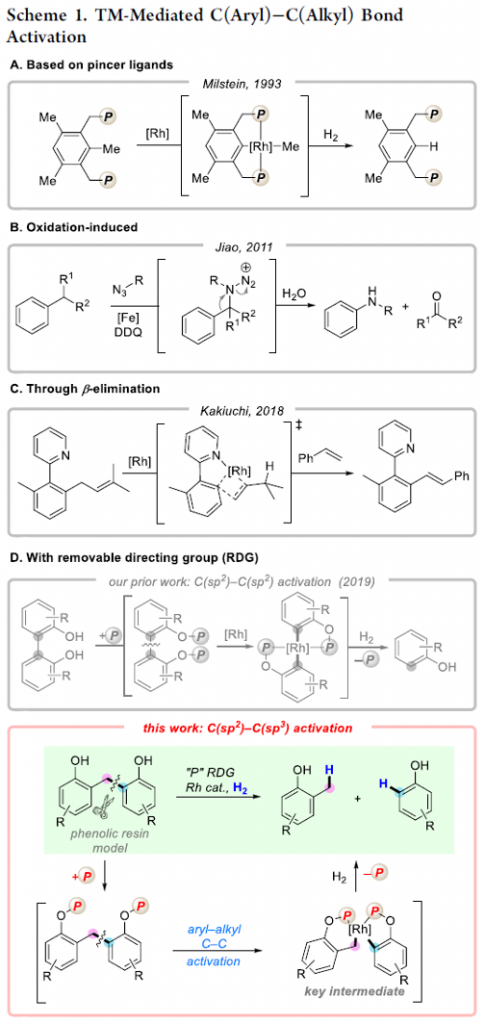
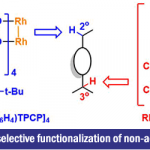
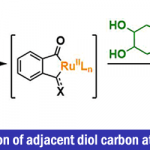
通过过渡金属催化的C-C键活化反应方法学研究,目前已经备受有机合成化学家的广泛关注[1]-[6]。然而,对于非张力与非极性的C-C键断裂反应的研究,则较少有相关的文献报道 (Scheme 1A-1C) [7]-[10]。这里,受到本课题组前期对于非张力联芳化合物中C(aryl)-C(aryl)键的断裂反应[11] (Scheme 1D)方法学相关研究报道的启发,董广斌研究团队成功设计出一种全新的采用铑催化剂参与的通过RDG (removable directing group)策略进行的2,2′-亚甲基二酚化合物的氢解反应方法学,进而顺利实现一系列单酚类分子的构建。同时,该小组进一步发现,反应过程中的关键中间体主要涉及5/6螺-环金属配合物。
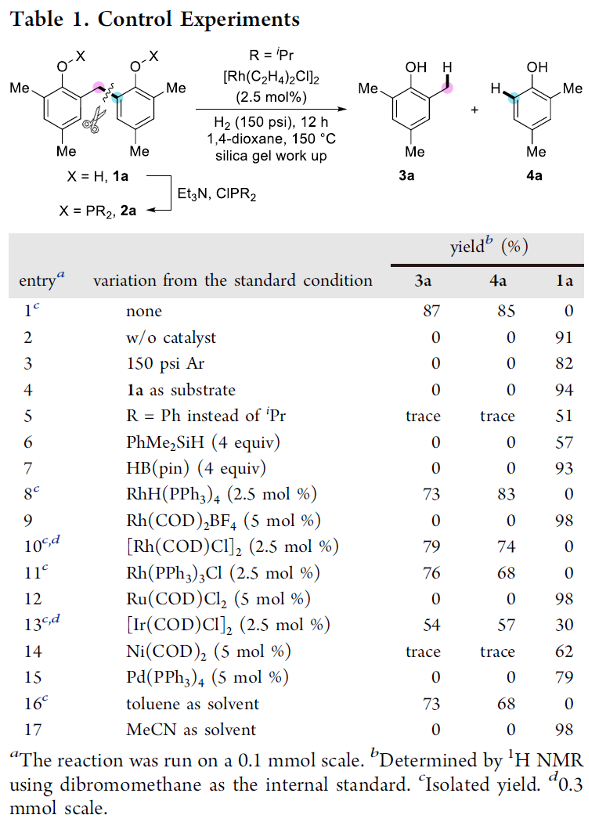
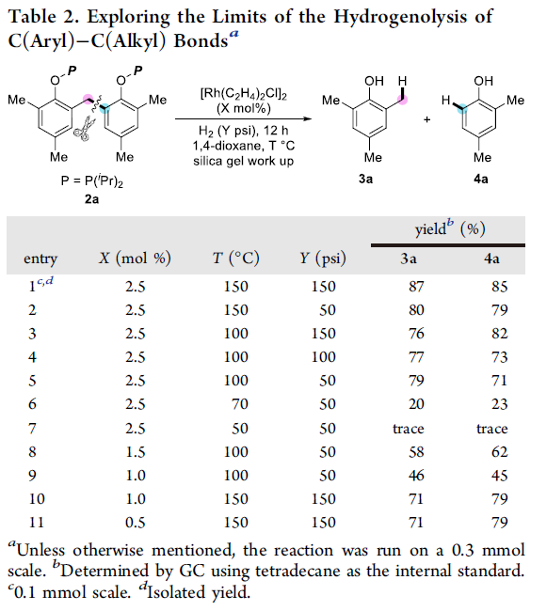
首先,作者采用原位形成的双酚phosphinite 2a作为模型底物,进行相关反应条件的优化筛选 (Table 1-2),进而确定最佳的反应条件为:采用[Rh(C2H4)2Cl]2作为催化剂,phosphinite作为RDG,150 psi的H2压力,1,4-二氧六环作为反应溶剂,反应温度为150 oC,反应进行12 h,之后,通过硅胶进行处理与纯化,去除分子中的RDG,最终分别以87%与85%的分离收率,获得相应的氢解产物3a与4a。
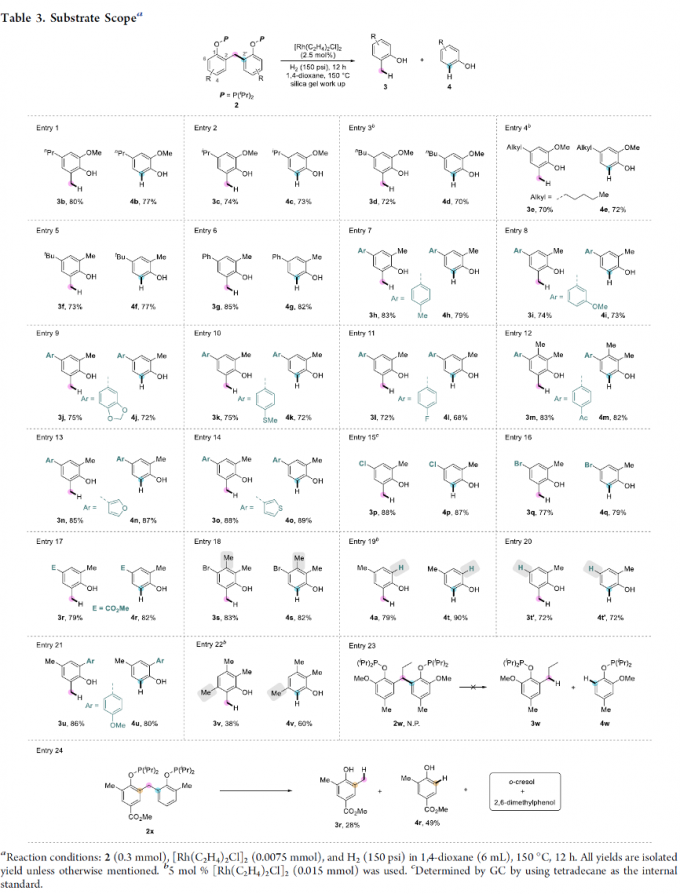
在上述的最佳反应条件下,作者对一系列2,2′-亚甲基二酚phosphinite底物的应用范围进行考察 (Table 3)。研究表明,各类苯环4,4′-位具有烷基、芳基、杂芳基、卤素基团、酯与硫代酯、醚、缩醛、羰基以及富电子杂环基团取代的2,2′-亚甲基二酚phosphinite底物,均能够较好地与上述的标准反应条件兼容,并以中等至良好的反应收率,获得相应的单酚产物 (Entry 1-17, 20)。同时,作者进一步发现,在苯环5,5′-位与6,6′-位具有不同基团取代的2,2′-二酚phosphinite底物,同样能够有效地参与上述的合成转化过程,进而以中等至良好的反应收率,获得相应的单酚产物 (Entry 12, 18-19, 21)。然而,上述的标准反应条件对于3,3′-位取代的2,2′-亚甲基二酚phosphinite,则仅能够获得中等收率的单酚产物 (Entry 22)。之后,该小组发现,在2,2′-亚甲基二酚phosphinite底物的亚甲基中具有取代基团存在时,能够有效地抑制金属中心对于分子中相应C(aryl)-C(alkyl)键的配位,进而无法获得预期的目标产物 (Entry 23)。并且,作者进一步观察到,采用非对称的底物2x,则Csp2-Csp3键的断裂优先选择在更加缺电子的芳环中进行 (Entry 24)。
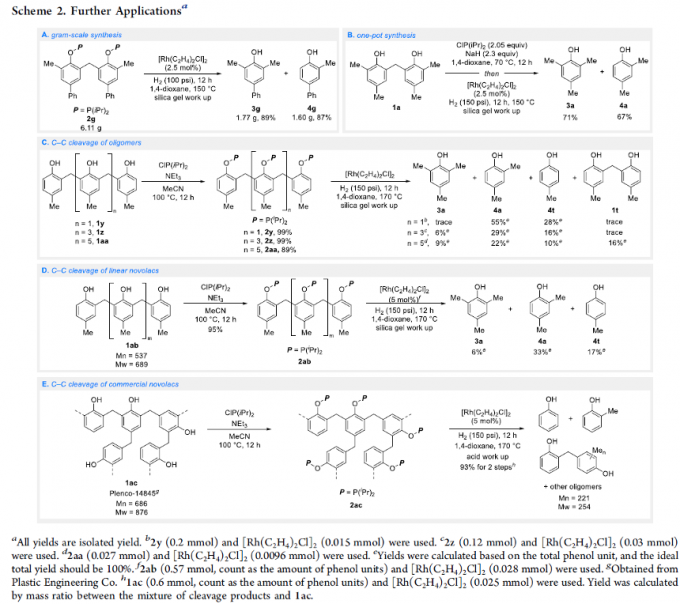
之后,该小组通过如下的一系列研究进一步表明,这一全新的氢解策略具有良好的合成应用前景 (Scheme 2)。
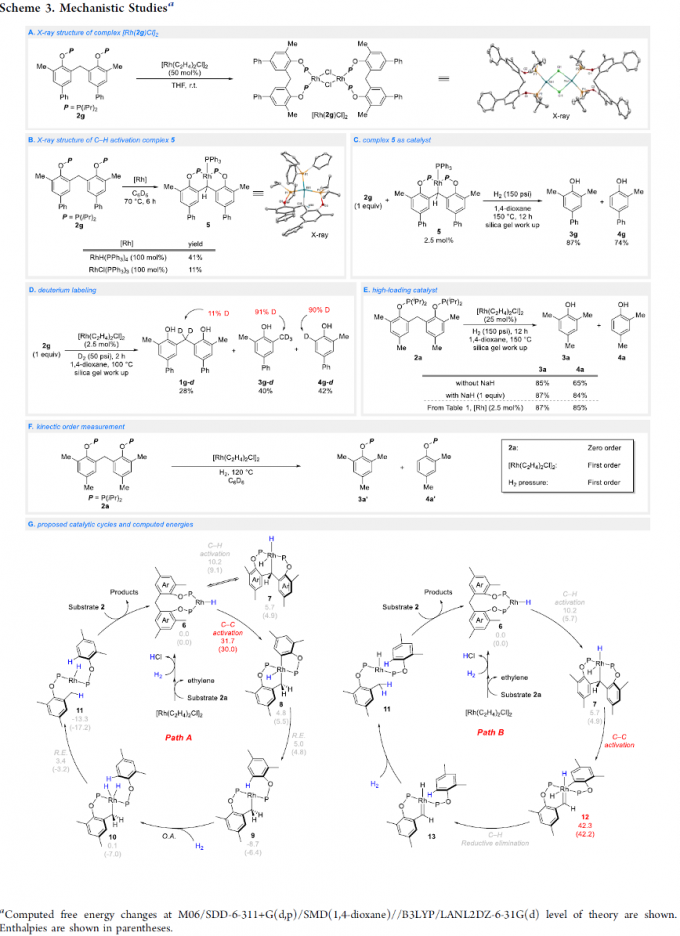
接下来,作者通过X射线晶体学研究表明,在铑催化剂与2,2′-亚甲基二酚phosphinite之间的配位过程中,更加有利于形成双齿配位的配合物[Rh(2g)Cl]2,进而促进后续配体取代过程的有效进行 (Scheme 3A)。之后,作者进一步通过对于铑配合物5的X射线晶体学研究表明,亚甲基位置的C-H活化过程为快速反应步骤 (Scheme 3B)。同时,作者进一步发现,通过C-H铑化 (C-H rhodation)步骤形成的配合物5可能作为反应过程中的关键中间体(Scheme 3C)。并且,C−H活化为可逆的非循环过程 (off-cycle process)。之后,该小组通过氘标记实验的相关研究 (Scheme 3D)发现,底物中亚甲基基团H/D交换过程的反应速率高于相应的C-C活化步骤;同时,monophosphinite基团导向的C-H活化过程的反应速率较为缓慢,难以与相应的C-C活化步骤进行有效的竞争;而且,底物之间的配体交换速率同样较为缓慢。同时,该小组通过对催化剂负载量的相关实验研究 (Scheme 3E)进一步表明,反应过程中,可能通过氢分子对催化剂进行活化[11]。接下来,作者通过动力学级数的测定进一步表明,底物与催化剂之间能够快速地形成较为稳定的配合物中间体。同时,该小组通过Hammett分析表明,苯酚片段中吸电子基团的存在,能够促进反应过程的有效进行。通过上述研究,作者提出两种可能的反应路径 (Scheme 3G),并进一步通过DFT计算表明,path A过程更为有利。
总结
董广斌教授团队成功设计出一种全新的采用铑催化剂促进的通过RDG (removable directing group)策略进行的2,2′-亚甲基二酚化合物的氢解反应方法学,进而顺利实现各类单酚类分子的构建。这一全新的氢解策略具有良好的官能团兼容性以及广阔的合成应用前景。
参考文献
- [1] M. E. van der Boom, D. Milstein, Chem. Rev. 2003, 103, 1759. doi: 10.1021/cr960118r.
- [2] G. Fumagalli, S. Stanton, J. F. Bower, Chem. Rev. 2017, 117, 9404. doi: 10.1021/acs.chemrev.6b00599.
- [3] L. Deng, G. Dong, Trends Chem. 2020, 2, 183. doi: 10.1016/j.trechm.2019.12.002.
- [4] M. Tobisu, N. Chatani, Chem. Soc. Rev. 2008, 37, 300. doi: 10.1039/B702940N.
- [5] C. Jun, Chem. Soc. Rev. 2004, 33, 610. doi: 10.1039/B308864M.
- [6] M. D. R. Lutz, B. Morandi, Chem. Rev. 2021, 121, 300. doi: 10.1021/acs.chemrev.0c00154.
- [7] M. Gozin, A. Weisman, Y. Ben-David, D. Milstein, Nature 1993, 364, 699. doi: 10.1038/364699a0.
- [8] C. Qin, W. Zhou, F. Chen, Y. Ou, N. Jiao, Angew. Chem. Int. Ed. 2011, 50, 12595. doi: 10.1002/anie.201106112.
- [9] S. Onodera, S. Ishikawa, T. Kochi, F. Kakiuchi, J. Am. Chem. Soc. 2018, 140, 9788. doi:10.1021/jacs.8b03718.
- [10] J. Zhu, P. Chen, G. Lu, P. Liu, G. Dong, J. Am. Chem. Soc. 2019, 141, 18630. doi: 10.1021/jacs.9b11605.
- [11] J. Zhu, J. Wang, G. Dong, Nat. Chem. 2019, 11, 45. doi: 10.1038/s41557-018-0157-x.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载























No comments yet.