摘要
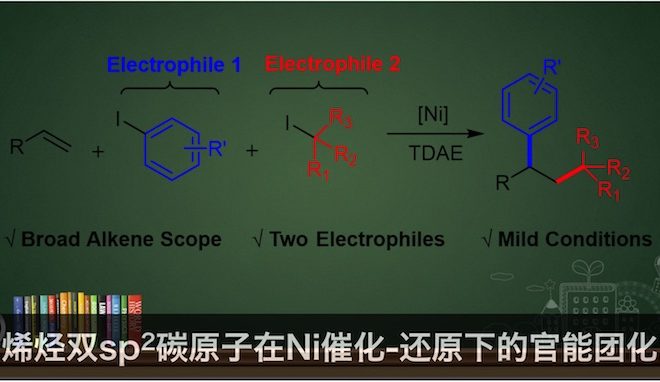
瑞士苏黎世大学的Cristina Nevado课题组近日报道了首例在Ni和TDAE [tetrakis(dimethylamino)ethylene]催化下,利用两种亲电试剂对烯键加成,可在温和条件下使烯烃的两个sp2碳原子官能团化的反应。该反应具有底物范围广、条件温和、操作简单等特点。
Nickel-Catalyzed Reductive Dicarbofunctionalization of Alkenes Andrés García-Domínguez, Zhaodong Li, and Cristina Nevado J. Am. Chem. Soc., 2017, 139, 6835–6838. DOI:10.1021/jacs.7b03195
研究背景
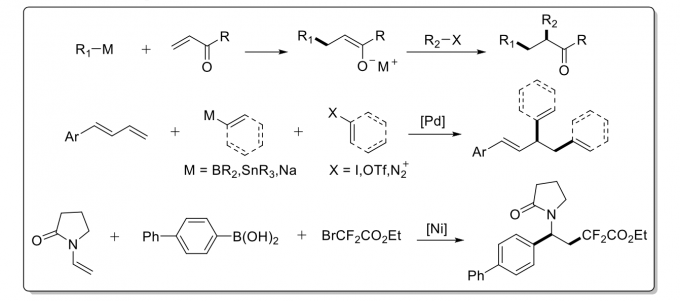
对烯烃的两个sp2碳原子进行官能团化近年来吸引了很多研究者的兴趣,原因是烯烃来源广以及官能团化的产物具有较高的价值。传统的方法是利用有机金属化合物的Michael加成反应1,近年利用过渡金属尤其是Pd和Ni催化的方法也有报道2(见图1)。然而这些反应都具有一定局限性,就过渡金属催化而言,Csp3金属试剂或中间体会发生-H消除、自偶联、异构化等多种副反应,仅有少数利用Csp3金属试剂的反应得到报道3。借鉴众多已发表的成果,基于Csp3试剂的这类反应可通过还原偶联这一独特方法实现。最终,课题组人员在Ni催化下,首次利用两种亲电试剂(区别于之前一种亲电试剂和一种亲核试剂)对烯键加成,实现了sp2碳原子的双官能团化。
条件优化
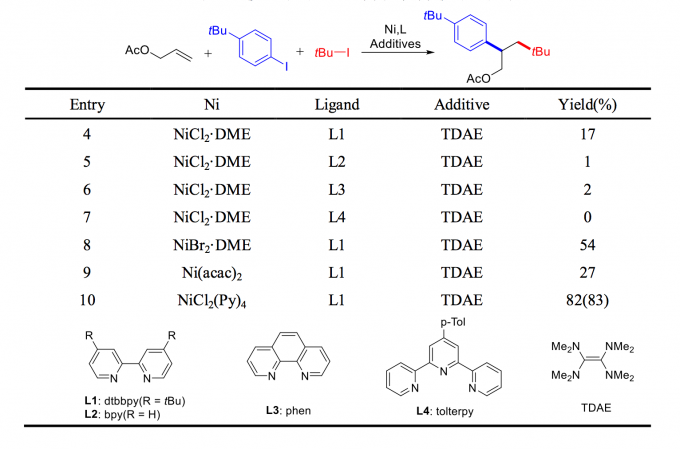
课题组人员首先建立了一个模型反应,然后对催化剂Ni、配体和添加物进行了筛选优化。部分筛选结果如表1所示。研究人员首先对添加物进行了筛选,以NiCl2·DME为Ni的来源,L1为配体,加入Zn、Mn和B2pin2/tBuOK后反应均不进行,加入TDAE可得到17%的产率(Entry 4)。随后对不同配体进行筛选,由L1换成其余配体后产率未得到提高反而降低较多(Entry 5-7)。最后进行的是催化剂Ni的筛选,NiBr2·DME较NiCl2·DME和Ni(acac)2效果更佳(Entry 8-9),但NiCl2(Py)4可得到最高83%的可观产率(Entry 10)。缺少某种原料对反应影响的实验表明,Ni络合物以及配体对反应至关重要,不可或缺。
表 1模型反应的部分条件优化结果
底物拓展
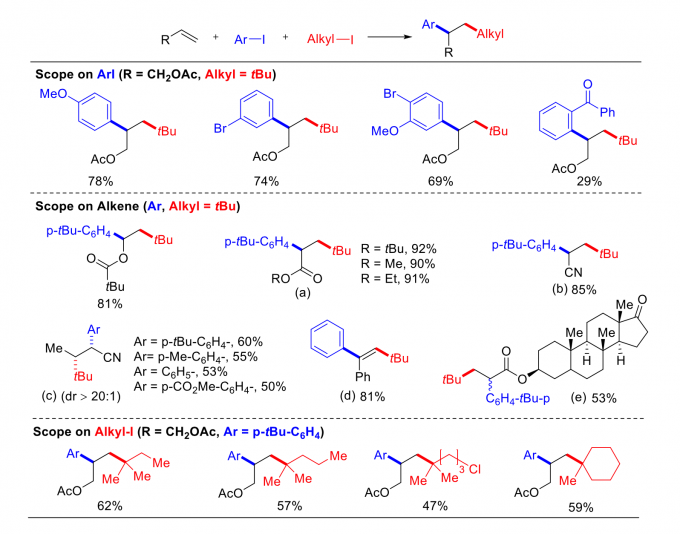
建立最优的反应条件(表1,Entry 10)后,研究人员对反应底物的范围进行了探究。部分结果如图2所示,首先是芳基碘化物,当对位和间位分别是甲氧基和溴原子时产率最高,换成其他吸电子或给电子取代基时也可达到中等及以上的收率;间位和对位被甲氧基和溴原子取代时产率为69%,然而邻位取代的底物由于位阻的存在,仅有29%的较低收率。随后探究的是烯烃的种类,烯醇酯产率81%,特别地是,对于可发生Michael加成的底物,产率较高的到达85%(b),更高可到90-92%(a)。在立体化学方面,丁烯腈(E:Z = 4:1)参与反应除了具有可观的收率外,还表现出较高的非对映选择性(dr > 20:1);对于更复杂的甾类底物(e),反应仍然奏效。最令人欣喜的是,炔类化合物也能顺利进行反应(产率81%,d),并且仅得到单一的反式加成产物。最后是烯烃的种类,不同类型的不活泼的3°碘代烷,包括那些含有Csp3-Cl的都可以顺利反应。对于那些不含官能团的双键,反应往往不能进行,说明官能团的存在对于反应具有一定的协同/导向作用。总之,这个反应具有很好的底物兼容性,可在多种底物上成功应用。
对照实验与反应机理
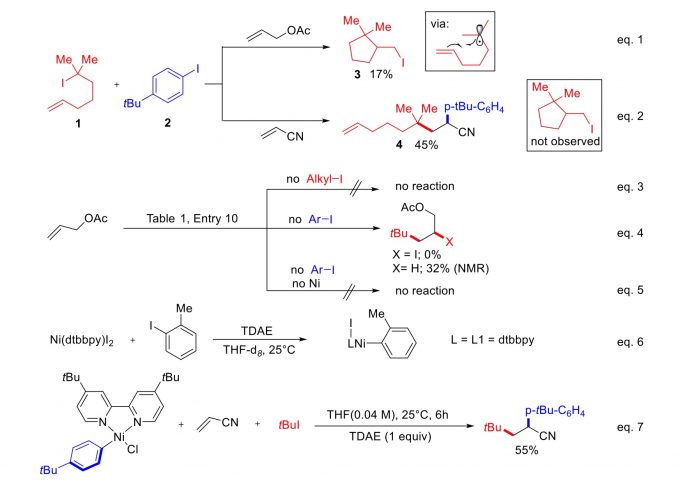
为了揭示反应进行的机理,研究人员进行了一系列对比实验(图3)。首先进行的是自由基抑制实验,当体系中加入BHT、1,1-二苯乙烯和1,4-环己二烯后,反应受到较大抑制,产率为0或者仅有23%,说明反应可能经历自由基中间体。进一步实验,不活泼的乙酸烯丙酯作为烯烃部分参与反应时,化合物1分子内关环得到产物3这一途径要优于分子间反应4;当丙烯腈参与反应时,分子间反应优势则更明显,没有化合物3生成。这些结果与之前所报道的两个过程(分子内自由基中间体关环和分子间反应)竞争的动力学数据相吻合5,同时也可证明自由基中间体的存在。底物拓展时,叔碘代烷可以顺利进行反应,并未进行仲碘代烷的实验,为了探究反应过程中是否出现由叔碘代烷到仲碘代烷这一可能过程,单独利用仲碘代烷进行实验的结果是反应不能进行,没有得到预期产物。有趣的是,当缺少碘代烷时,反应不能进行(eq. 3),证明该条件下反应不会生成Heck类型的偶联产物。然而缺少芳基碘代物时的碘代叔丁烷却可以发生反应,虽然产率较低(eq. 4),另外Ni的存在对于反应至关重要(eq. 5),最后探究的是还原剂的作用,实验表明Ni(dtbpy)I2和TDAE在邻碘甲苯存在时可以形成ArNi(II)络合物,表明TDAE还原Ni(II)后体系还进行了一个氧化加成过程(eq. 6)。经对氯叔丁基苯制备的ArNi(II)2络合物和丙烯腈、碘代叔丁烷在TDAE存在下的反应可得到55%产率的预期产物(eq. 7),这更说明了ArNi(II)络合物是反应的重要中间体。
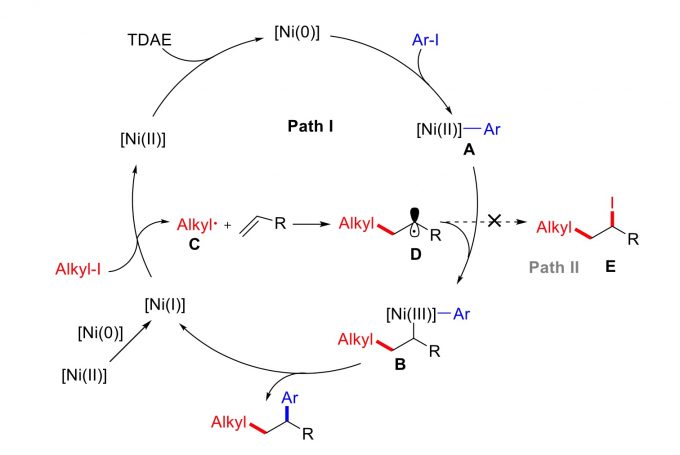
基于上述对照实验,研究人员提出了可能的反应机理(图4),大致过程可以描述为:由TDAE还原Ni(II)原位生成的[Ni(0)]与ArI通过氧化加成得到ArNi(II)中间体A,同时[Ni(I)]活化碘代烷产生碳自由基中间体C,紧接着自由基加成到双键上得到自由基中间体D,A与D最终都会转化为关键中间体Ni(III)络合物B(途径I)。络合物B经历一个还原消除过程得到目标产物和Ni(I),Ni(I)可被氧化到Ni(II),也可由Ni(II)和Ni(0)生成,从而形成形成一个循环。对照实验已经证实,途径II生成产物E是不能进行的。不难发现,对照实验eq. 4正是通过自由基中间体D进行的。
结论
首例分子间的三组分偶联反应对烯烃双键进行官能团化的方法得到报道。利用TDAE对Ni再生,避免了浪费并且操作简单。除此之外,反应的条件温和,官能团兼容性强,反应机理也比较新颖。
参考文献
- (1) Chapdelaine, M. J.; Hulce, M. Org. React. 1990, 38, 225.
- (2) (a) Urkalan, K. B.; Sigman, M. S. Angew. Chem., Int. Ed. 2009, 48, 3146. DOI: 10.1002/ange.200900218 (b) Liao, L.; Jana, R.; Urkalan, K. B.; Sigman, M. S. J. Am. Chem. Soc. 2011, 133, 5784. DOI: 10.1021/ja201358b
- (3) (a) Wang, F.; Wang, D.; Mu, X.; Chen, P.; Liu, G. J. Am. Chem. Soc. 2014, 136, 10202. DOI: 10.1021/ja504458j (b) Ouyang, X.-H.; Song, R.-J.; Hu, M.; Yang, Y.; Li, J.-H. Angew.Chem., Int. Ed. 2016,55, 3187. DOI: 10.1002/anie.201511624
- (4) Newcomb, M.; Filipkowski, M. A.; Johnson, C. C. TetrahedronLett. 1995, 36, 3643. DOI: 10.1016/0040-4039(95)00595-4
- (5) Fischer, H.; Radom, L. Angew. Chem., Int. Ed. 2001, 40, 1340. DOI: 10.1002/1521-3773(20010417)40:8<1340::AID-ANIE1340>3.0.CO;2-#
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!














No comments yet.