作者:石油醚
本期热点研究,我们邀请到了本文第一作者,来自UCLA的和志奇博士为我们分享。
2023年08月24日,Sciecne在线发表了来自UCLA的Ohyun Kwon教授团队题为「Aminodealkenylation: Ozonolysis and copper catalysis convert C(sp3)–C(sp2) bonds to C(sp3)–N bonds」的研究论文。作者利用与π-键相邻的C(sp2)–C(sp3) σ-键,在温和的条件下,通过臭氧化反应和铜催化,使烯烃的C(sp3)–C(sp2) σ-键断裂并重新构建C(sp3)–N 键,得到了分子骨架解构重组的脱烯胺化产物。通过这样的非传统转化,利用自然界丰富的萜类天然产物中的烯烃官能团,可以合成具有高潜在生物活性的非天然萜类生物碱和复杂的手性胺化合物。并且工业上廉价的cumene process副产物,α-甲基苯乙烯,发展为甲基化试剂,一步直接与核苷反应生成表观遗传学中重要的甲基化核苷原料。这样的方法也被用于激素、药物中间体、多肽和核苷的后期修饰或合成。通过动力学研究,揭示了一种一直被忽略的铜离子对协同催化机理。
“Aminodealkenylation: Ozonolysis and copper catalysis convert C(sp3)–C(sp2) bonds to C(sp3)–N bonds
Zhiqi He, Jose Antonio Moreno, Manisha Swain, Jason Wu, Ohyun Kwon*
Science, 2023, 381, 877-886. DOI: 10.1126/science.adi4758”
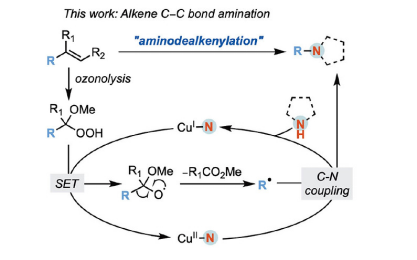
Q1. 请对“Aminodealkenylation: Ozonolysis and copper catalysis convert C(sp3)–C(sp2) bonds to C(sp3)–N bonds”作一个简单介绍。
从易得的起始原料出发,发展高效合成策略,制备重要的有机化合物一直是合成化学的研究重点。相较于从简单原料出发的通过官能团转化/偶联的汇聚式合成构建复杂产物策略,直接从复杂化合物出发,针对分子骨架进行解构重组(deconstructive construction/synthesis)构建目标产物有时会更为高效。脂肪胺和含氮杂环在天然产物、药品、农药以及其他生物活性化合物中广泛存在。当前的新药研发对合成更为复杂的三维结构手性胺的需求逐渐增加,这也促使着各种高效构建C(sp3)–N键方法的发展。
烯烃广泛存在于石油化工和天然产物中,通过烯烃来制备脂肪胺一直以来都是研究热点,而烯烃中的π-键作为活泼官能团通常是构建新的C(sp3)–N键的反应位点。本工作基于2019年课题组发展的脱烯氢化反应(Science 2019, 364, 681–685)发展了全新的烯烃胺化策略。我们的策略是通过烯烃在醇溶剂中的臭氧化反应,生成过氧中间体。其中较为活泼的O–O键(BDE ~ 45 kcal/mol)可以提供驱动力在被单电子还原的情况下变成烷基氧自由基。随后烷氧自由基触发C–C键裂解,将原本的烯烃解构成活泼并且多用途的烷基自由基中间体。一价铜催化剂可在这个过程中充当单电子供体生成二价铜,而二价铜可以捕获烷基自由基进而促进C(sp3)–N键偶联,从而得到了分子骨架解构重组的脱烯胺化产物。这样的方法也被用于激素、药物中间体、多肽和核苷的后期修饰或合成。并且通过这样的非传统转化,利用自然界丰富的萜类天然产物中的烯烃官能团,可以合成具有高潜在生物活性的非天然萜类生物碱和复杂的手性胺化合物。尤其是一些较为昂贵的手性胺生物活性中间体,传统合成路径较为繁琐。而使用脱烯胺化方法,直接使用大量易得且具有一定复杂度的天然萜类衍生物进行解构胺化,可将合成路线简化,这也为合成化学提供了新的手段和思路。同时,工业上廉价易得的烯烃,比如说cumene process副产物,α-甲基苯乙烯,在脱烯胺化反应中可以作为良好的甲基化试剂,一步直接与核苷反应生成表观遗传学中重要的甲基化核苷原料,例如m6A。最后,在机理研究中,人们总是认为中性的[(Phen)CuL]是铜和1,10-菲啰啉的组合的催化活性物种,其离子对形式[(Phen)2Cu]+ [CuCl2]–通常被人们所忽视。本工作中,通过研究不同的铜化合物,还有[(Phen)2Cu]+和[CuCl2]–分别对C–C键断裂和C–N键生成的的影响,证实了铜离子对协同催化机理是存在并且可行的。这一结论可以让人们重新思考,相关铜催化过程中的机理,并且为已发表相关论文中提出的催化机理,尤其是没有经过实验正式仅简单推测的催化循环,提供了重新审视的理论基础。
Q2.在研究的时候遇到过怎样的困难呢?又是怎样克服的呢?
我感觉一开始做动力学实验时是最困难的。这个反应速度快,通常10分钟内就反应完了,所以不方便取样测量,因为操作不过来,样品点太少。又由于体系里面有含有铜离子,所以不能用原位核磁实时监测反应。我们的产物分子量大,气相色谱又出不来。所以我一开始只能用最笨的方法,将反应极度稀释来降低反应速率,达到可以取样测量的程度,然后过滤硅胶柱除掉铜盐,再用核磁测产率。最后大概稀释了25倍,才是一个可以操作的反应速率。但是这个时候铜非常稀,3毫克的CuCl溶在75 mL的乙腈里面,浓度是400 ppm。这就导致溶剂里面微量的氧气都有可能氧化一价铜物种,所以我每次做这个实验前都是新鲜蒸馏,然后再做冻抽,即使是这样也时常发现结果不重现。如果CuCl+Phen被氧化,最终结果将使得速率变慢,或者开始慢后来快的S形曲线,甚至出现induction period。而且由于反应浓度稀,每次取样3 mL才能用装备有冷冻探头的核磁扫描64次拿到信号强度足够的氢谱。而且内标也是个问题,我试过将内标提前加入到反应中,发现要不内标对反应有影响,要不反应对内标有影响,总共试过四五种内标都不太好,最终只能配好的内标溶液,在快速的取样过滤之后加入相同体积的内标溶液,这里还必须保证样品体积和内标溶液体积一样,也就是那3 mL反应液要快速准确的取出。感觉操作非常繁琐,而且经常遇到数据不好的情况。这个用核磁方法研究动力学足足做了7个多月,实验强度大,数据到最后也不是很满意。所以我也是一直想找其他方法来分析反应。
后来也是一个契机,Mettler Toledo来UCLA,我们跟他们表明需要他们的技术支持,于是他们在去年10月底给我们寄过来一台ReactIR。由于之前7个月把做这个动力学实验中需要注意的细节都摸清楚了,第一次用,只一周时间就把原来7个月都没做好的实验做完了,而且数据质量显著提高,重现性好。但是这次demo test只有一周时间,于是我们再次跟他们联系,他们表示12月有大量空闲机时,我们就趁着这一个月,拿到了现在文章上的所有数据。而且用ReactIR监测反应的时候,MeOAc的峰很明显,这也给我一个同时研究C–C断裂和C–N生成的手段。而且一个月时间相对宽裕,我才能深入的探索铜离子对中正负离子的功能以及对反应的影响。
Q3. 本次研究主体,有没有什么让您感觉特别辛苦和烧脑呢?
就是在用ReactIR得到靠谱数据后发现这些数据又很离谱。我们用VTNA方法分析了反应底物以及催化剂的反应级数(在文章中有部分总结, SI-section8中可以看到更全的底物和催化剂的具体反应级数)发现都是一些非常规的反应级数,比如(CuCl+Phen)对C–C键断裂和C–N生成均是1.3级。当保持CuCl为4 mol%时,Phen从2 mol% – 4mol%是0级,但是Phen从4 mol% – 8mol%时表现为–5级。然后 [(Phen)2Cu]+和[CuCl2]–在不同浓度下有不同动力学级数,并且对C–C键断裂和C–N生成也有不同的动力学级数,比如说,固定[(Phen)2Cu]+用量为0.5 mol%的时候,[CuCl2]–对C–C键断裂和C–N生成表现为2级反应,但是当[(Phen)2Cu]+用量为2 mol%时,[CuCl2]–对C–C键断裂和C–N生成表现为1.3级反应;固定使用2 mol% [CuCl2]–时,[(Phen)2Cu]+使用量为0.1 mol%到0.5 mol%时对C–C键断裂表现为0级对C–N生成表现为1级,但是[(Phen)2Cu]+使用量为0.5 mol%到2.0 mol%时对C–C键断裂表现为–0.3级对C–N生成表现为0级。所以当时如何将这些动力学级数合理化并且推导出反应速率方程的过程确实非常烧脑。今年1月初归还了ReactIR之后一直没做实验,天天在构建反应模型,然后推导动力学公式,用了一个半月才建立了一个粗糙的模型,详细分析过程以及推导过程都写在了SI的10.1 和10.2章,也希望大家能多交流指正。
Q4. 将来想继续研究化学的哪个方向呢?
其实有机化学的相关方向我都想学习,想学一些交叉学课,比如化学生物学,有机材料,机器学习啥的,但是申请这些方向课题组时人家都不理我。目前在搞塑料降解相关的研究,以后大概率还要回到有机方法学及其延申的方向。
Q5. 最后,有什么想对各位读者说的吗?
我想鼓励年轻的研究生和博士后们在科研生活中坚持追求自己的兴趣,保持对科学的热情和好奇心,勇敢面对挑战,因为探索的道路充满了发现和惊喜。
作者教育背景简介

教育背景:
2007-2011年:中国农业大学,本科
2011-2016年:北京大学,博士,导师:黄湧教授
2016-2019年:北京大学,研究助理,导师:黄湧教授
2019-2023年:UCLA,博士后,导师:Ohyun Kwon
2023-:UW-Madison,博士后,导师:Shannon S. Stahl
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.



















No comments yet.