作者:石油醚
本期热点研究,我们邀请到了本文第一作者,来自西安交通大学的博士生高原为我们分享。
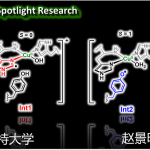
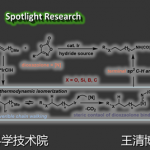
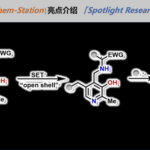
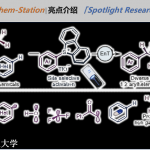
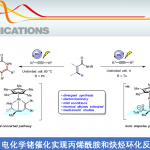
2023年6月1日,Angew. Chem. Int. Ed.在线发表了来自西安交通大学李鹏飞教授和石河子大学徐亮教授团队合作的题为「Additive-Free Transfer Hydrogenative Direct Asymmetric Reductive Amination Using a Chiral Pyridine-Derived Half-Sandwich Catalyst」的研究论文。本文在2010年肖建良教授报道的消旋转移氢化还原胺化反应的基础上,结合本课题组最近在新型手性吡啶配体方面的研究成果,合理设计并合成了手性吡啶衍生半夹心铱催化剂。在温和、操作简单的条件下,成功催化了无添加剂的转移氢化不对称还原胺化反应,以良好到优异的收率和对映选择性制备了一系列包含多种极性官能团和杂环结构的α-手性(杂)芳基胺类化合物。通过密度泛函理论的计算,作者发现含“内松外紧”手性吡啶的催化剂结构使得底物与配体之间产生协同的p/p堆积和多个C–H‧‧‧p弱相互作用,从而有效实现了该立体决定步骤的对映选择性。
该反应在很大程度上解决了现有报道中使用大量添加剂,极性官能团和杂环难以兼容,反应条件苛刻等难题。本文提供了一种合成手性胺的新方式,为解决具有强配位能力杂环和官能团底物在过渡金属催化不对称反应中难以耐受提供了新蓝图,进一步显示出新型手性吡啶骨架在不对称催化反应中具有巨大的潜力。

“Additive-Free Transfer Hydrogenative Direct Asymmetric Reductive Amination Using a Chiral Pyridine-Derived Half-Sandwich Catalyst”
Yuan Gao, Zhijun Wang, Xinyu Zhang, Min Zhao, Shuai Zhang, Chao Wang, Liang Xu,* and Pengfei Li*
Angew. Chem. Int. Ed., 2023, ASAP, doi: 10.1002/anie.202303709
Q1. 请对“Additive-Free Transfer Hydrogenative Direct Asymmetric Reductive Amination Using a Chiral Pyridine-Derived Half-Sandwich Catalyst”作一个简单介绍。
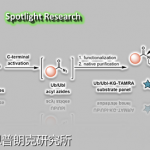
手性胺是广泛存在于天然产物、合成药物和功能材料中重要的结构单元。人们迫切需要新的方法来高效广谱地合成手性胺。在已知的策略中,胺和酮之间的直接不对称还原性胺化反应被公认为是最实用的策略。然而,到目前为止,仍然存在明显的局限性,包括使用当量添加剂,反应条件严苛,极性官能团和杂环难以耐受的问题。我们通过使用手性吡啶衍生半夹心铱催化剂成功解决了上述还原胺化反应中存在的问题,本文成功的关键是以我们小组开发的具有刚性稠环骨架和“内松外紧”空间特征的手性吡啶单元为核心设计出新型手性铱催化剂,克服了外球机制、单点作用以及铱中心立体选择性不易控制的问题。
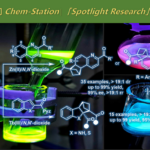
归功于配位饱和的金属中心,催化剂中毒现象被很大程度解决。因此反应对杂原子、杂环和极性官能团显示出优异的兼容性。作为氢原的甲酸/三乙胺共沸物提供酸性环境,促进了亚胺生成,故而无需额外使用添加剂。我们对60多种带有不同官能团和杂环结构的(杂)芳基酮和(杂)芳基胺的底物进行了考察。实验结果显示,在近乎室温、无需水氧处理的简单条件下,反应广泛耐受多种活性官能团以及多种五元和六元杂环底物,包括弱亲核性双杂原子杂芳胺,并以良好到优异的收率和对映选择性得到目标手性胺产物。此外,该反应还被成功用于一些具有杂环结构和活性官能团的较复杂药物分子的后期衍生化,充分展示了该策略的应用潜力。
Q2. 有关本次研究的时候遇到过怎样的困难呢?又是怎样克服的呢
受益于我们组所开发手性吡啶的刚性稠环骨架,我们设计合成的新型手性吡啶衍生的半夹心铱催化剂具有完美的非对映选择性(>99:1),避免了常见的半夹心结构中金属手性中心对后续催化反应对映选择性的干扰。因此,该课题的首次不对称探索就以中等的立体选择性获得了目标产物,这也给予了我们极大的信心。尽管我们的手性吡啶骨架结构高度可调,但相对于吡啶一侧,配体的苯基部分则过于空旷,好比手性口袋仅仅完成了一半,因此我们对立体选择性的优化并不顺利。对于配体芳环部分的改造收效甚微,位阻小了就实现不了整个手性口袋的构建,位阻大了就会大幅影响反应活性和立体选择性。经过两年的探索,产物的ee值提升并不理想,依旧是中等偏高的立体选择性。
得益于李鹏飞教授的悉心教导,我们受本组开发的手性吡啶骨架本身启发,设计出文中最优配体。由于手性吡啶骨架具有“内松外紧”的空间特征,有着中心金属近程位阻最小化和远端侧链结构的高度可调性,因此手性吡啶配体在保证金属催化剂活性的同时,实现了手性环境的构建。参考手性吡啶的特征,我们设计出具有手性联萘结构的新型催化剂,其中在铱中心远端与吡啶部分近似垂直的萘环部分,在铱中心的外围提供了“内松外紧”的手性空间,与手性吡啶部分相互结合,提供了完整的手性口袋环境。正如我们设计的一样,该催化剂在转移氢化不对称还原胺化反应中提供了优异的立体选择性。
Q3. 本次研究主体,有没有什么让您感觉特别辛苦和烧脑呢?
手性配体的设计与合成是一个比较辛苦且烧脑的过程,幸好有李鹏飞教授的耐心指导以及不断鼓励,让我在科研的探索过程中始终充满信心。
Q4. 将来想继续研究化学的哪个方向呢?
在接下来的研究工作中,我们将基于我们在转移氢化不对称还原胺化领域已有的研究基础,以我们的手性吡啶骨架为核心,进一步设计合成更加高效高立体选择性的新型催化剂,并在不对称还原胺化领域深入研究,继续努力。
Q5. 最后,有什么想对各位读者说的吗?
人生有如科研,坚持不懈,积极思考,不断尝试,即使面临困境永不言弃,突破瓶颈后,会取得更大的收获。
作者教育背景简介

教育背景:
2013-2017 吉林大学唐敖庆理科试验班化学方向 学士 (导师:林英杰 教授;段海峰 教授)
2017-2020 吉林大学化学学院 硕士 (导师:林英杰 教授;段海峰 教授)
Since 2020 西安交通大学前沿科学技术研究 博士 (导师:李鹏飞 教授)
相关介绍:
高原,出生并成长于吉林四平。2013-2017 在吉林大学唐敖庆理科试验班化学方向获得学士学位。 2017-2020年在吉林大学化学学院林英杰教授和段海峰教授的指导下进行手性有机小分子催化剂的合成及其在不对称Friedel-Crafts反应和不对称Nitro-Mannich 反应中的应用研究,并获得硕士学位。2020至今,在西安交通大学前沿科学技术研究李鹏飞课题组攻读博士学位,研究方向为手性吡啶衍生半夹心铱催化剂的设计合成和转移氢化不对称还原胺化反应的研究。














No comments yet.