本文作者:asymmboy
概要
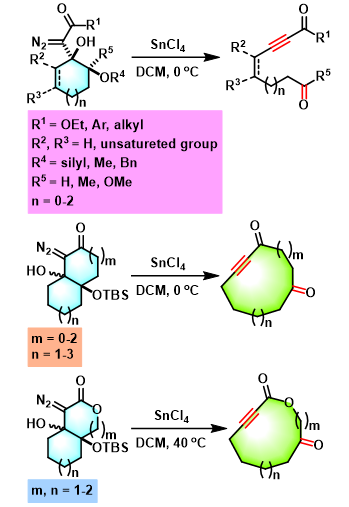
Brewer 碎片化 (Brewer fragmentation) 是在SnCl4 (Lewis酸)存在下,单环γ-硅氧基-β-羟基-α-重氮羰基化合物[1] 、γ-含氧取代-β-羟基-α-重氮羰基化合物[2]与双环γ-硅氧基-β-羟基-α-重氮酮[3]以及双环γ-硅氧基-β-羟基-α-重氮内酯[4]通过炔键生成碎片化 (alkynogenic fragmentation)过程,分别获得炔基羧酸酯、炔酮、中环2-炔酮与ynolide的反应[1]-[4]。该反应由美国Vermont大学化学系 (The University of Vermont, Department of Chemistry)的M. Brewer研究室在2008年首次报道[1]。
Brewer 碎片化反应条件温和,具有较高的产率与优良的官能团兼容性。目前,该反应已经开始应用于部分杂环化合物的合成[5]以及天然产物全合成[6]-[7]中的关键步骤。
基本文献
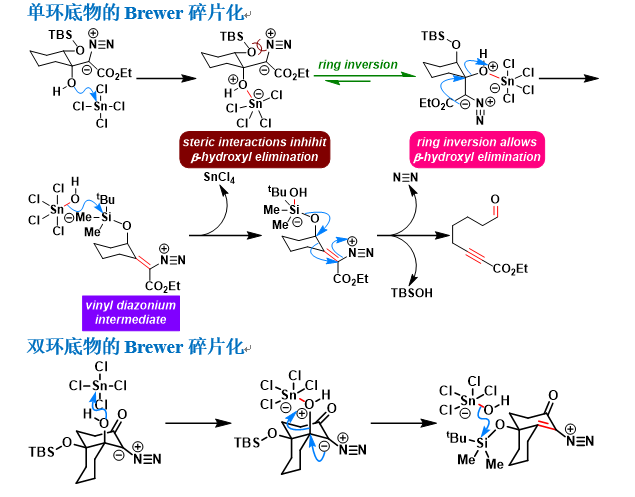
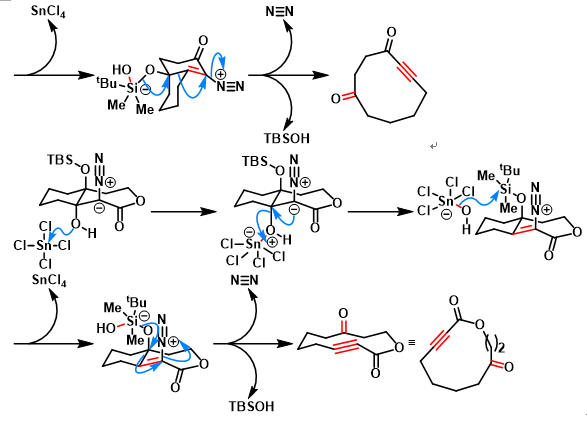
[1] M. Brewer, C. Draghici. J. Am. Chem. Soc. 2008, 130, 3766. doi: 10.1021/ja801004d. [2] A. Bayir, C. Draghici. M. Brewer, J. Org. Chem. 2010, 75, 296. doi: 10.1021/jo902405f. [3] N. P. Tsvetkov. A. Bayir, S. Schneider, M. Brewer, Org. Lett. 2012, 14, 264. doi: 10.1021/ol2030422. [4] A. Bayir, M. Brewer, J. Org. Chem. 2014, 79, 6037. doi: 10.1021/jo500634d. [5] C. Draghici, Q. Huang, M. Brewer, J. Org. Chem. 2009, 74, 8410. doi: 10.1021/jo901978y. [6] Z. Zhang, G. M. Giampa, C. Draghici, Q. Huang, M. Brewer, Org. Lett. 2013, 15, 2100. doi: 10.1021/ol4004993. [7] N. D. Jabre, T. Watanabe, M. Brewer, Tetrahedron 2014, 55, 197. doi: 10.1016/j.tetlet.2013.10.152.反应机理
参考文献
[1] R. Pellicciari, B. Natalini, B. M. Sadeghpour, M. Marinozzi, J. P. Snyder, B. L. Williamson, J. T. Kuethe, A. Padwa, J. Am. Chem. Soc. 1996, 118, 1. doi: 10.1021/ja950971s. [2] N. D. Jabre, M. Brewer, J. Org. Chem. 2012, 77, 9910. doi: 10.1021/jo301944t. [3] E. Wenkert, C. A. McPherson, Synth. Commun. 1972, 2, 331. doi: 10.1080/00397917208061990.反应实例
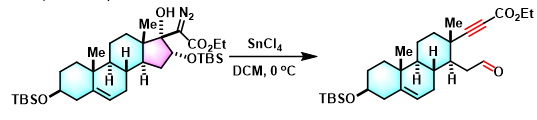
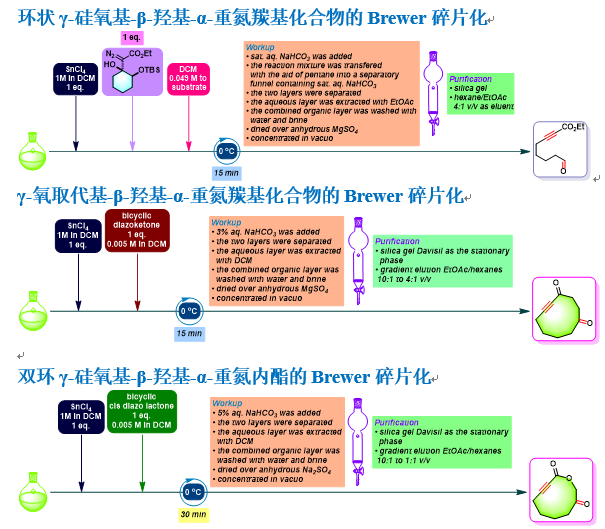
环状γ-硅氧基-β-羟基-α-重氮羰基化合物的Brewer碎片化[1]
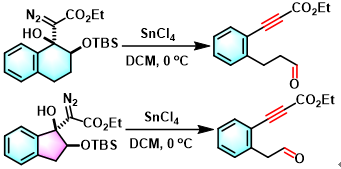
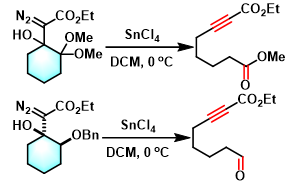
γ-氧取代基-β-羟基-α-重氮羰基化合物的Brewer碎片化[2]
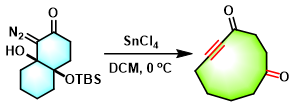
双环γ-硅氧基-β-羟基-α-重氮酮的Brewer碎片化[3]
双环γ-硅氧基-β-羟基-α-重氮内酯的Brewer碎片化[4]
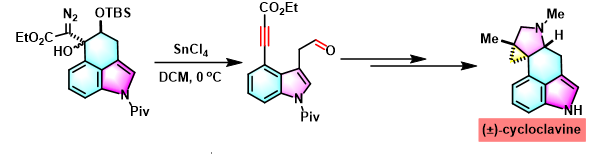
(±)-cycloclavine的全合成[5]
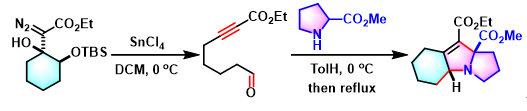
多环2,5-二氢吡咯的合成[6]
实验步骤
参考文献
[1] M. Brewer, C. Draghici. J. Am. Chem. Soc. 2008, 130, 3766. doi: 10.1021/ja801004d. [2] A. Bayir, C. Draghici. M. Brewer, J. Org. Chem. 2010, 75, 296. doi: 10.1021/jo902405f. [3] N. P. Tsvetkov. A. Bayir, S. Schneider, M. Brewer, Org. Lett. 2012, 14, 264. doi: 10.1021/ol2030422. [4] A. Bayir, M. Brewer, J. Org. Chem. 2014, 79, 6037. doi: 10.1021/jo500634d. [5] Jabre, N. D. Watanabe, T. Brewer, M. Tetrahedron 2014, 55, 197. doi: 10.1016/j.tetlet.2013.10.152. [6] C. Draghici, Q. Huang, M. Brewer, J. Org. Chem. 2009, 74, 8410. doi: 10.1021/jo901978y.



















No comments yet.