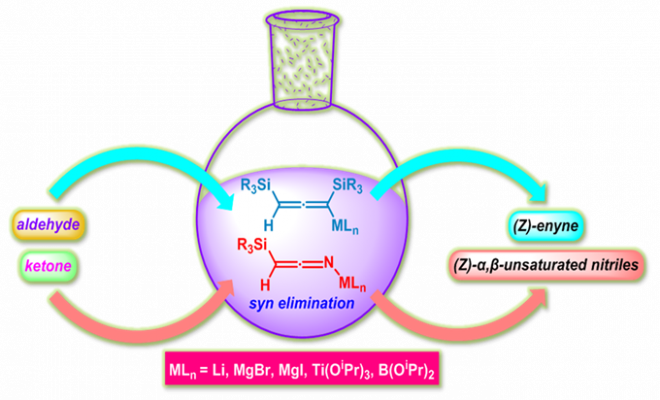
概要
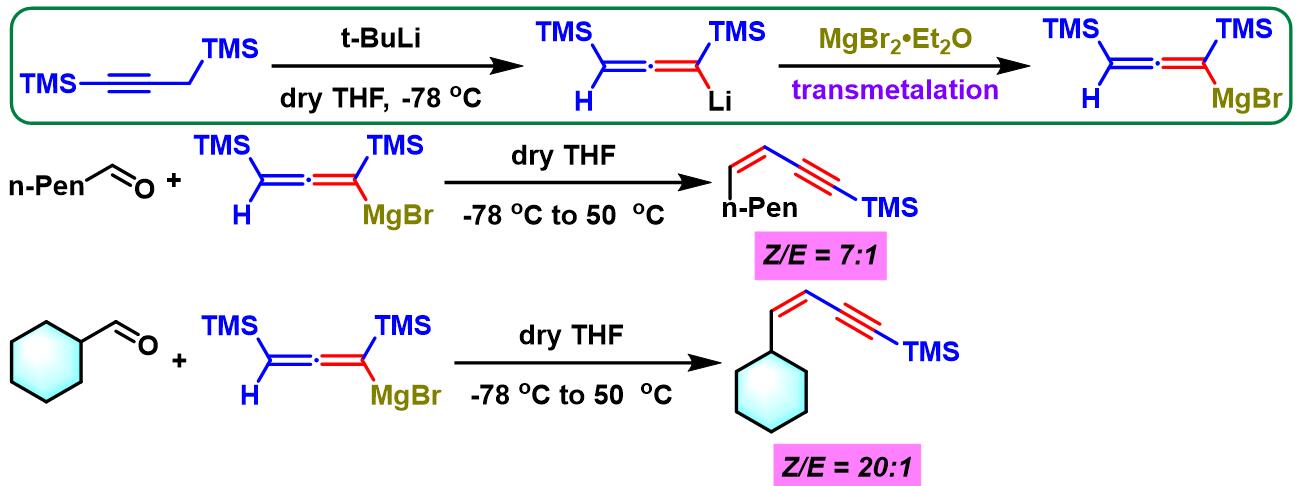
1981年,日本名古屋大学应用化学系的(名古屋大学応用化学科, Department of Applied Chemistry, Nagoya University)山本尚 (山本 尚, Yamamoto Hisashi)研究组通过1,3-双(三甲硅基)丙炔在强碱性条件下(如叔丁基锂)形成的联烯基锂试剂与醛或酮的反应,获得(Z)-烯炔类化合物,反应具有中等程度的立体选择性[1]。
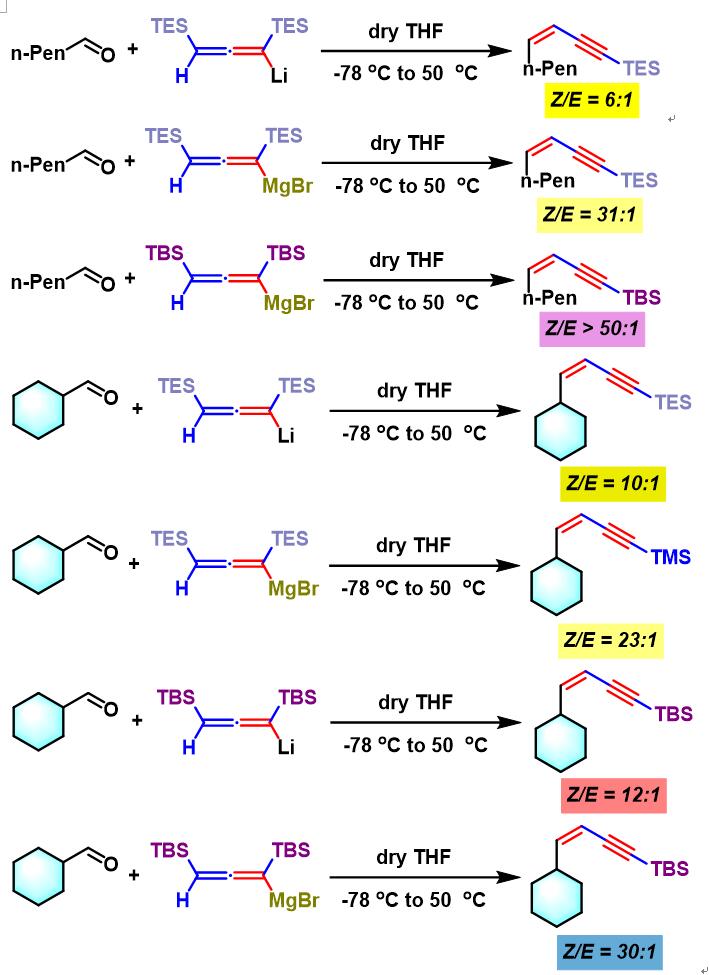
之后, Yamamoto通过加入溴化镁与联烯基锂试剂进行转金属化(transmetalation)过程,形成的联烯基镁试剂再与醛或酮反应,研究表明可以获得更高程度的(Z)-选择性。
同时,Yamamoto发现增大硅基团的立体位阻 (如采用TBS取代的炔烃),可极大提高反应的立体选择性。
随后,Yamamoto将底物进一步扩展至各类α-硅基乙腈 (α-silylated acetonitrile),完成(Z)-α, β-不饱和腈类化合物的构建。反应同样具有优良的立体选择性。
1982年,Yamamoto课题组进一步采用四异丙氧基钛、三异丙氧基硼分别与联烯基锂及由α-硅基乙腈形成的锂试剂进行转金属化 (transmetalation)反应,发现生成的相应硼及钛试剂同样可以参与上述反应,并以较好的立体选择性获得(Z)-烯炔及(Z)-α, β-不饱和腈类化合物[2]。
由于该方法成功将Peterson烯基化反应 (Peterson olefination)中的硅基金属试剂扩展至烯炔类化合物的立体选择性合成[1]。因此,文献中将该方法学称为Yamamoto-Peterson烯基化 (Yamamoto-Peterson olefination)[1]。该反应具有优良的立体选择性,为(Z)-烯炔及(Z)-α, β-不饱和腈类化合物的立体选择性合成开辟了全新的途径。同时,也为一些重要天然产物的全合成提供了一种更为简化的路线[3]。
基本文献
- [1] Y. Yamakado, M. Ishiguro, N. Ikeda, H. Yamamoto, J. Am. Chem. Soc. 1981, 103, 5568. doi: 10.1021/ja00408a049.
- [2] R. Haruta, M. Ishiguro, K. Furuta, A. Mori, N. Ikeda, H. Yamamoto, Chem. Lett. 1982, 18, 1093. doi: 10.1246/cl.1982.1093.
- [3] D. J. Hart, K. Kanai, J. Am. Chem. Soc. 1983, 105, 1255. doi: 10.1021/ja00343a030.
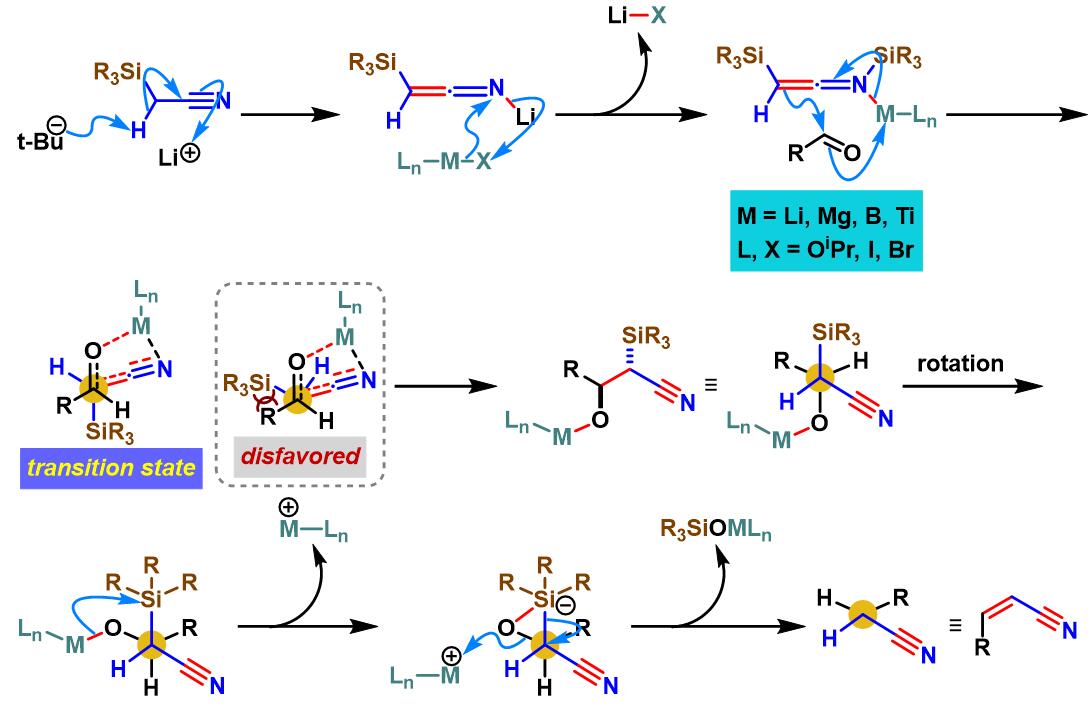
反应机理
(Z)-烯炔的生成
(Z)-α, β-不饱和腈的生成
参考文献
- [1] E. J. Corey, C. Riicker, Tetrahedron Lett. 1982, 23, 719. doi: 10.1016/S0040-4039(00)86930-0.
- [2] I. Ojima, M. Kumagai, Y. Nagai, Tetruhedron Lett. 1974,15, 4005. doi: 10.1016/S0040-4039(01)92069-6.
- [3] J. B. Moffat, J. Chem. Soc. Chem. Commun. 1980, 1108. doi: 10.1039/C39800001108.
反应实例
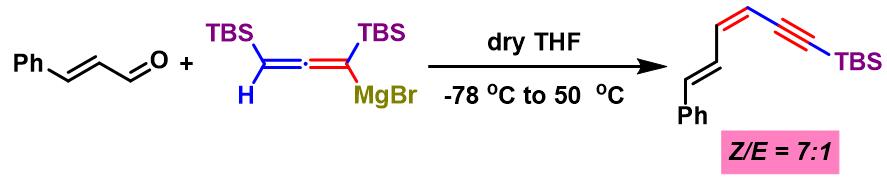
(Z)-烯炔的合成[1]
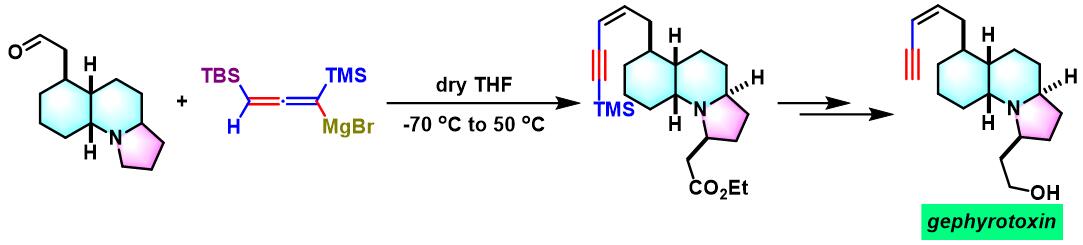
gephyrotoxin的全合成[2]
实验步骤
(Z)-烯炔的合成
在-78 oC,氩气气氛下,将叔丁基锂 (1.8 M 正戊烷溶液, 1.25 eq.)滴加至二硅基丙炔 (1.25 eq.)的无水四氢呋喃溶液 (二硅基丙炔浓度为0.33 M)中。维持-78 oC,将上述混合物搅拌1 h后,加入新制备的溴化镁-乙醚配合物 (1.38 eq.),继续搅拌15 min。之后,加入羰基化合物 (1 eq.)。搅拌5 min后,将上述反应混合物逐渐升温至50 oC,继续搅拌,直至反应结束。反应结束后,加入稀盐酸淬灭反应。淬灭完成后,将反应液加入乙醚萃取,合并的有机相依次采用稀盐酸与水洗涤及无水硫酸钠干燥。减压除去溶剂后,将残余物通过硅胶柱色谱分离纯化 (正己烷作为洗脱剂)获得相应(Z)-烯炔产物。
(Z)-α, β-不饱和腈的合成
在-20 oC,氩气气氛下,将叔丁基锂 (1.8 M 正戊烷溶液, 1.25 eq.)滴加至二硅基乙腈 (1 eq.)的无水四氢呋喃溶液 (二硅基乙腈浓度为0.33 M)中。维持-20 oC,将上述混合物搅拌30 min后,加入新制备的碘化镁-乙醚配合物 (1.1 eq.),继续搅拌5 min。之后,将上述反应混合物冷却至-78 oC,再加入羰基化合物 (1 eq.)。搅拌5 min后,将上述混合物升温至-20 oC,继续搅拌15 min后,再升温至50 oC,继续搅拌,直至反应结束。反应结束后,加入稀盐酸淬灭反应。淬灭完成后,将反应液加入乙醚萃取,合并的有机相依次采用稀盐酸与水洗涤及无水硫酸钠干燥。减压除去溶剂后,将残余物通过硅胶柱色谱分离纯化 (正己烷作为洗脱剂)获得相应(Z)-α, β-不饱和腈产物。
参考文献
- [1] Y. Yamakado, M. Ishiguro, N. Ikeda, H. Yamamoto, J. Am. Chem. Soc. 1981, 103, 5568. doi: 10.1021/ja00408a049.
- [2] D. J. Hart, K. Kanai, J. Am. Chem. Soc. 1983, 105, 1255. doi: 10.1021/ja00343a030.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

























No comments yet.