概要
酞阴离子和α,β-不饱和羰基化合物通过迈克尔反应→狄克曼缩合反应合成萘氢醌的手法,同时这也是聚酮化合物的合成常用的手法之一。
底物中苄基位置是磺酰基取代的时候进行的反应被称为Hauser环化、当是氰基取代的话进行的反应称为Kraus环化。后者的立体位阻比较小,所以产率一般比较高。
底物酞被o-甲基安息香酸的乙酯替代的时候被称为Staunton-Weireb环化。该反应通常生成萘酚产物。
基本文献
- Hauser, F. M.; Rhee, R. J. Am. Chem. Soc. 1977, 99, 4533. DOI: 10.1021/ja00455a069
- Hauser, F. M.; Rhee, R. J. Org. Chem. 1978, 43, 178. DOI: 10.1021/jo00395a048
- Kraus, G. A.; Sugimoto, H. Tetrahedron Lett. 1978, 19, 2263. doi:10.1016/S0040-4039(01)91508-4
- Evans, G. E.; Leeper, F. J.; Murphy, J. A.; Staunton, J. J. Chem. Soc., Chem. Commun. 1979, 205. DOI: 10.1039/C39790000205
- Leeper, F. J.; Staunton, J. J. Chem. Soc. Chem. Commun. 1979, 206. DOI: 10.1039/C39790000206
- Dodd, J. H.; Weinreb, S. M. Tetrahedron Lett. 1979, 20, 3593. doi:10.1016/S0040-4039(01)95472-3
<review>
- Mitchell, A. S.; Russell, R. A. Tetrahedron 1995, 51, 5207. doi:10.1016/0040-4020(95)00247-6
- Mal, D.; Pahari, P. Chem. Rev. 2007, 107, 1892. DOI: 10.1021/cr068398q
- Rathwell, K.; Brimble, M. A. Synthesis 2007, 643. DOI: 10.1055/s-2007-965915
- Karmakar, R.; Pahari, P.; Mal, D. Chem. Rev. 2014, 114, 6213. DOI: 10.1021/cr400524q
- Donner, C. D. Tetrahedron 2013, 69, 3747. doi:10.1016/j.tet.2013.03.034
反应机理
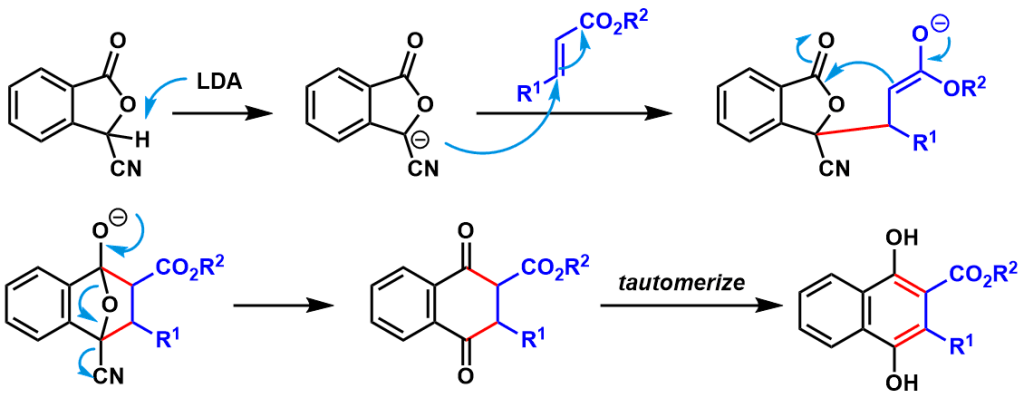
反应实例
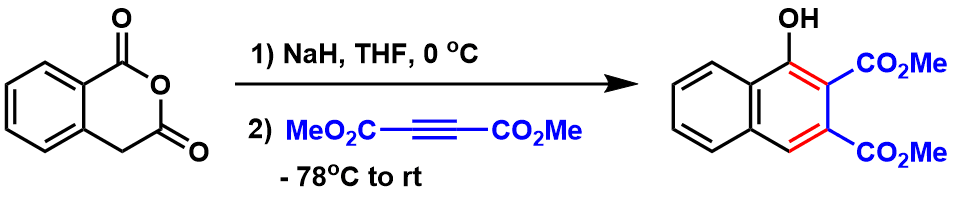
homophthalide作为底物的反应[1]
含有五个环的四环素衍生物的全合成[2]
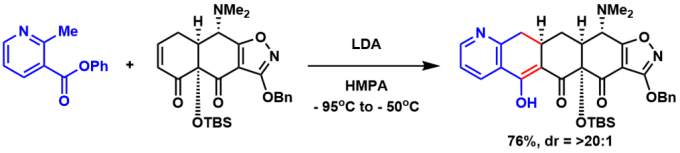
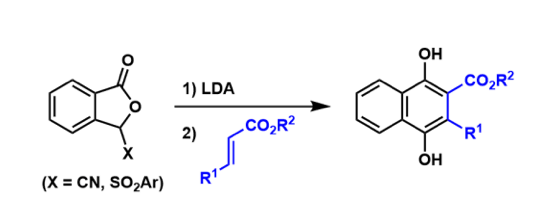
参考文献
- Tamura, Y.; Sasho, M.; Nakagawa, K.; Tsugoshi, T.; Kita, Y. J. Org. Chem. 1984, 49, 473. DOI: 10.1021/jo00177a017
- Charest, M. G.; Lerner, C. D.; Brubaker, J. D.; Siegel, D.; Myers, A. G. Science 2005, 308, 395. DOI:10.1126/science.1109755


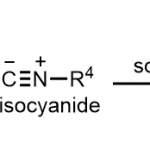












No comments yet.