- 概要
赫克反应(Heck反应)是利用Pd(0)催化剂、使芳基卤化物或烯基卤化物和末端烯烃偶联的一种偶联反应。官能团的选择性和收率非常好。
本反应对不发生烯烃位置异构的底物非常有效。如果反应底物里含丙烯醇,反应的过程中会出现烯烃的异构化生成羰基化合物。
烯烃的一端有烷氧基羰基或芳基等吸电子基团时、反应会从另一端的碳(=CH2)进行。如果烯烃的一端是烷氧基醚等供电子基团时,控制反应的位置选择性会非常难。
分子内的赫克反应和狄尔斯–阿尔德反应是少有的能合成不对称季碳的方法(反应例参考)。
- 基本文献
・Mizoroki, T.; Mori, K.; Ozaki, A. Bull. Chem. Soc. Jpn. 1971, 44, 581.
・Heck, R. F.; Nolley, Jr., J. P. J. Org. Chem. 1972, 37, 2320. DOI:10.1021/jo00979a024
・Heck, R. F. Org. React. 1982, 27, 345.
・de Meijere, A.; Meyer, F. E. Jr.; Angew. Chem. Int. Ed. Engl. 1994, 33, 2379.[Abstract]
・足森厚之, Overman, L. E. 有機合成化学協会誌 2000, 58, 718.
・Beletskaya, I. P.; Cheprakov, A. B. Chem. Rev. 2000, 100, 3009. DOI: 10.1021/cr9903048
・Dounay, A. B.; Overman, L. E. Chem. Rev. 2003, 103, 2945. DOI: 10.1021/cr020039h
・Link, J. T. Org. React. 2003, 103, 2945.
- 反应机理
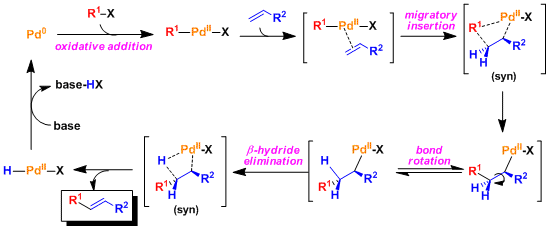
迁移插入和β-氢消除是在Pd原子的syn位置发生。这个事实事实是理解Heck反応的立体化学的非常重要的一点。(特别是在合成缩环化合物时)
- 反应实例
Arenastatin A的合成[1]
芳香胺的Heck反応。
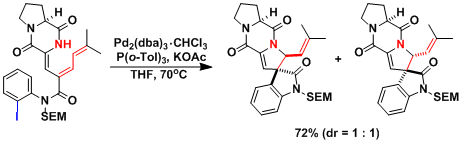
π-烯丙基钯的反应中间体[2]:酰胺的N原子从背面攻击钯
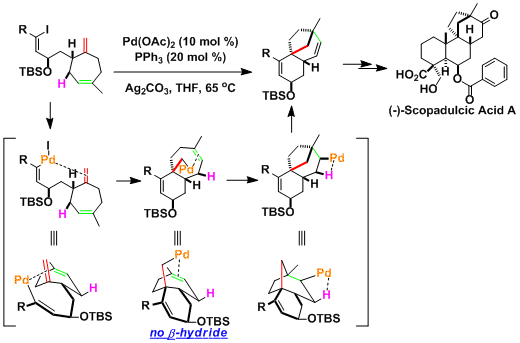
Scopadulcic Acid A合成是利用的Domino-Heck反応[3]: 如果syn位置(从Pd原子看)没有可消去的β-氢,同分子内的第二个烯基就会开始反应而得到多环化合物。
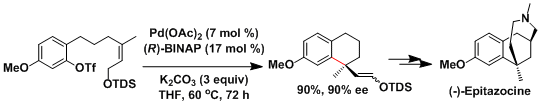
不对称Heck反応的Epitazocine合成[4]:利用双齿手性膦配体能应用在不对称合成。实现高选择性需要阳离子钯的帮助。根据反应底物不同有时需要三氟甲磺酸酯或卤化物和氯化银。
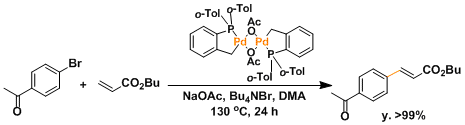
用从醋酸钯和P(o-Tol)3调配的稳定的环状钯催化剂可使TON提高到约100万次。
- 实验步骤
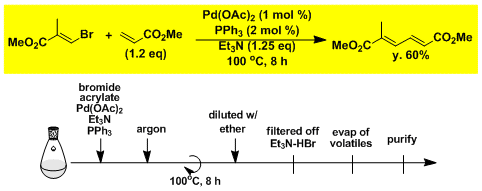
烯基溴和丙烯酸甲酯的Heck反応
- 实验技巧
- 参考文献
[2] Waterlot, C; Couturier, D. et.al. Tetrahedron Lett. 2000, 41, 317. doi:10.1016/S0040-4039(99)02082-1
[3] Fox, M. E.; Li, C; Marino, J. P.; Overman, L. E. J. Am. Chem. Soc. 1999, 121, 5467. DOI:10.1021/ja990404v
[4] Takemoto, T.; Sodeoka, M.; Sasai, H.; Shibasaki, M. J. Am. Chem. Soc. 1993, 115, 8477. DOI:10.1021/ja00071a079
[5] Dieck, H. A.; Heck, R. F. J. Org. Chem. 1975, 40, 1083. DOI: 10.1021/jo00896a020
- 相关书籍
- 相关链接
・Heck Reaction
・The Heck Reaction (A. Myer’s Group, PDF)
・Heck reaction (Wikipedia)
・Heck Reaction (organic-chemistry.org)


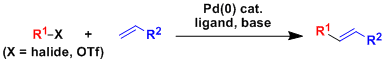
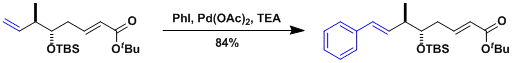
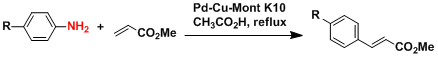












No comments yet.